Molekulární šroubovice
Chiralita je jedním z důležitých konceptů v chemii. Představuje vlastnost molekul, které jsou neschopné překrýt svůj zrcadlový obraz, což znamená, že mají stejnou molekulární strukturu, ale odlišné prostorové uspořádání. Takovéto dvě molekuly pak nazýváme enantiomery a jejich vzájemný vztah si lze jednoduše představit jako levou a pravou ruku. Ačkoliv mají enantiomery obvykle stejné fyzikální vlastnosti, chiralita často hraje klíčovou roli v biologických a biochemických systémech, kde jedna chirální forma může být biologicky aktivní, zatímco jiná chirální forma téže sloučeniny biologicky aktivní být nemusí, anebo může být její účinek na systém výrazně odlišný, někdy až fatální.1) Výzkum chirálních látek se v poslední době soustřeďuje nejenom na biochemické systémy, ale rovněž se snaží využít vlastnosti chirálních sloučenin v materiálových vědách. [1] Chiroptické materiály (interagující s kruhově polarizovaným zářením) jsou předmětem značného zájmu v aplikacích, jako je např. vývoj 3D-displejů, kvantových informačních technologií, bioimagingu/biosensingu či technologií pro ochranu proti padělání apod. V tomto kontextu odborníci studují několik skupin slibných látek, jednou z nich jsou i sloučeniny nazývané heliceny (obr. 1). [2]
Heliceny jsou organické polycyklické sloučeniny, které jsou tvořeny ortho kondenzovanými benzenovými kruhy. Ačkoliv se jedná o aromatické látky, nejsou heliceny planární, ale kvůli sterické repulzi koncových jader zaujímají tvar připomínající šroubovici. Ta může být levotočivá (značí se M) nebo pravotočivá (P), a heliceny se tak řadí mezi chirální sloučeniny. Důsledkem chirality a přes celou šroubovici vysoce delokalizovaného systému π-elektronů jsou pak výjimečné optické a elektronické vlastnosti těchto sloučenin. Heliceny vykazují enormní hodnoty specifické optické otáčivosti, cirkulárně polarizovanou fotoluminiscenci a elektroluminiscenci, nelineárně optické vlastnosti nebo silný cirkulární dichroismus. Díky těmto vlastnostem mohou být tyto sloučeniny využity v různých oblastech chemie. Své uplatnění již nalezly například v molekulárním rozpoznávání, materiálové chemii, aktivních vrstvách senzorů, kapalných krystalech, jako katalyzátory v asymetrických reakcích a celé řadě dalších aplikací.
Ačkoliv jsou heliceny známy již více než 110 let, jejich většímu rozšíření a aplikaci donedávna bránila absence účinných metod jejich přípravy. Šlo o složité a zdlouhavé syntetické postupy, které bylo obtížné realizovat ve větším měřítku. Díky značnému úsilí několika vědeckých skupin máme dnes k dispozici řadu robustních syntetických cest, které vedou k helicenům. Kromě reakcí katalyzovaných přechodnými kovy lze zmínit i fotochemické postupy, speciálně pak fotochemické syntézy prováděné v průtočném reaktoru, pomocí kterých lze získat relativně velká množství helicenů a jejich funkčních derivátů. Díky tomu je možné studovat tyto látky podrobněji a zaměřit se tak i na jejich budoucí využití.
Až na výjimky jsou heliceny získávané ve formě racemátu, to znamená ve směsi, která obsahuje obě chirální helicenové formy, tedy jak levotočivou, tak i pravotočivou šroubovici. Aby bylo možné naplno využít potenciál helicenů, je nutné od sebe tyto optické formy (enantiomery) oddělit. K tomu vědci vyvinuli několik postupů. Nejmodernější z nich využívají sofistikované kovové katalyzátory, které umožňují vést organické transformace ke směsi, kde výrazně převažuje jeden enantiomer helicenu. Bohužel však tento postup není obecný a pro některé helicenové deriváty je třeba zvolit jiné přístupy. Těmi mohou být například krystalizace s jinou chirální látkou anebo – dnes prozatím nejpoužívanější – separace enantiomerů pomocí vysokoúčinné kapalinové chromatografie s chirální stacionární fází, kdy se využívá rozdílně silné interakce jednotlivých enantiomerů s chirálním činidlem vázaným v chromatografické koloně.
Při práci s heliceny, stejně jako i s jinými chirálními sloučeninami, je třeba brát v potaz ještě další důležitý aspekt. Některé chirální látky totiž mohou takzvaně racemizovat. To znamená, že za určitých podmínek jedna chirální forma přechází na druhou a opačně. Výsledkem je vznik racemátu a ztráta chiroptických vlastností původní látky. U helicenů se odolnost vůči racemizaci řídí počtem benzenových kruhů, které tvoří šroubovici. U nejmenšího obecně uznávaného [5]helicenu (číslo v hranaté závorce udává, kolika aromatickými kruhy je helicen tvořen) je energie potřebná pro racemizaci ještě poměrně nízká (24 kcal ∙ mol–1). Důsledkem toho chirální formy [5]helicenu snadno přecházejí jedna v druhou a za běžných podmínek jsou tak od sebe neizolovatelné. Nicméně už enantiomer [6]helicenu je za běžných podmínek stabilní (racemizace začíná až při vyšších teplotách) a s přibývajícím počtem kruhů v molekule helicenu pak odolnost vůči racemizaci významně roste až do chvíle, kdy se uzavře celá jedna otočka šroubovice. Vliv dalších jader na racemizační bariéru pak už není dramatický a konverguje k hodnotě 44 kcal ∙ mol–1. Za zmínku rozhodně stojí i mechanismus racemizace helicenu, protože poměrně překvapivě se tak děje (navzdory intramolekulárnímu sterickému bránění a bez přerušení stávajících vazeb) pouhým konformačním přesmykem. Z toho vyplývá, že helicenový skelet je mnohem flexibilnější, než lze na první pohled očekávat.
Studium helicenů odhalilo, že ideální vlastnosti lze jen zřídka nalézt u karbohelicenů, tedy helicenů, jejichž šroubovice je tvořena pouze atomy uhlíku, a pro jejich lepší zacílení na možné aplikace je nutné jejich skelet dále opracovat. Zde se vědci soustředili na dvě možné cesty. V první z nich je do samotné šroubovice zaveden další atom odlišný od uhlíku. Nejčastěji se jedná o atomy dusíku nebo síry, ale díky značné snaze vědecké komunity můžeme dnes nalézt ve struktuře helicenů rovněž atomy boru, kyslíku, fosforu nebo třeba křemíku. Zavedení takového heteroatomu do helicenové šroubovice má přímý vliv na optické a elektronické vlastnosti daného helicenu a zároveň často umožňuje interakce s jinými molekulami, kterých karboheliceny jinak nejsou schopny. To opět chemikům umožňuje lépe ovlivňovat vlastnosti celého systému.
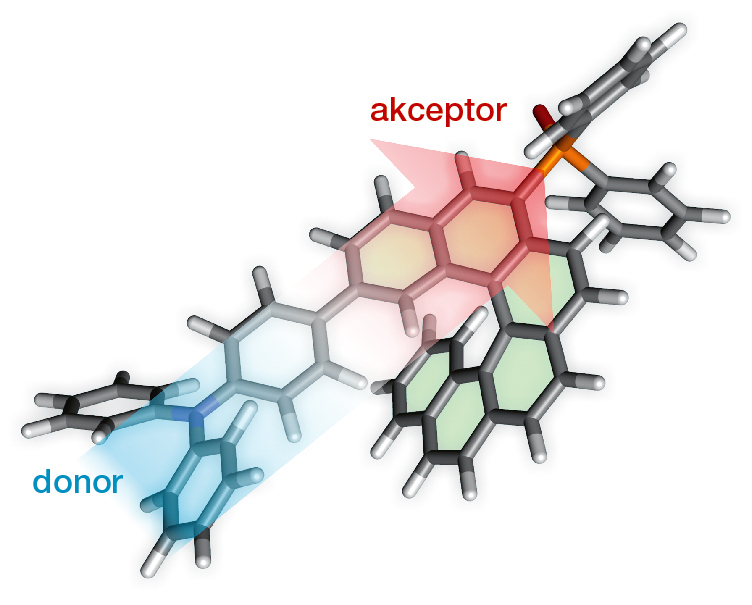
Druhou možností, jak zlepšit vlastnosti helicenů, je zachování uhlíkaté šroubovice, na kterou jsou připojeny další funkční skupiny, které jsou pak zodpovědné za finální vlastnosti celé molekuly. Pěkným příkladem může být tvorba takzvaných push-pullových systémů. [3] To jsou systémy, které na jednom konci obsahují silně elektrondonorní skupinu a na druhém konci silně elektronakceptorní skupinu. Přes spojku v podobě helicenu pak tyto skupiny vzájemně komunikují, což v důsledku opět umožňuje jemně ladit např. optoelektronické vlastnosti finálních helicenových derivátů (obr. 2).
Příkladem push-pullového helicenového systému jsou sloučeniny, které byly v nedávné době vyvinuty ve výzkumné skupině pokročilých materiálů a organické syntézy v Ústavu chemických procesů AV ČR. Připravené helicenové deriváty vykazovaly silný solvatochromismus, to znamená, že barva emise těchto látek silně závisí na polaritě rozpouštědla, ve kterém je měření prováděno.
Maximum emise v nepolárním rozpouštědle (heptanu) bylo detekováno u 431 nm, což odpovídá fialové barvě. Zatímco v polárním acetonitrilu došlo k posunu o velmi neobvyklých 107 nm k výsledným 538 nm, a roztok se tak jevil jako žlutozelený. Toho lze v budoucnu využít při konstrukci různých senzorických zařízení pro stanovení malého množství polárních molekul v nepolárním prostředí, například metanolu v naftě. Připravený helicenový derivát byl proto otestován v modelovém systému toluen/metanol. Na obrázku (obr. 3) je znázorněna postupná změna poměru toluenu a metanolu od čistého toluenu (vlevo) až po čistý metanol (vpravo).
S tím, jak se bude dále posunovat efektivita získávání chirálních forem helicenů a hloubka poznání v oblasti studia jejich vlastností, budou rovněž přibývat další příklady jejich praktického použití. Lze se domnívat, že tyto fascinující šroubovicové molekuly postupně naplní svůj enormní aplikační potenciál.
Článek s podporou Ústavu chemických procesů AV ČR
Poznámky
1) Např. nechvalně proslulým je lék thalidomid, který se předepisoval v šedesátých letech na ranní nevolnost těhotných žen. Jeho R-enantiomer působí jako sedativum, zatímco S-enantiomer (jak se zjistilo dodatečně) působí teratogenně.
Literatura
[1] Crassous J. et al., Nature reviews materials, 2023, DOI: 10.1038/s41578-023-00543-3.
[2] Crassous J. et al. (eds.), Helicenes: Synthesis, Properties and Applications, 1st ed.; Wiley, 2022, DOI: 10.1002/9783527829415.
[3] Beránek T. et al., Dyes and Pigments, 2023, DOI: 10.1016/j.dyepig.2022.111039.
Ke stažení
 článek ve formátu pdf [410,02 kB]
článek ve formátu pdf [410,02 kB]