Dvojí život ATP
Jako jednu z prvních informací se všichni studenti biologie dovídají, že molekuly ATP (adenosin 5´-trifosfátu) jsou nepostradatelnou součástí všech buněk – jsou univerzálním zdrojem energie. Méně se však ví, že ATP se vyskytuje i mimo buňky, kde slouží při mezibuněčné komunikaci a vyvolává řadu fyziologických účinků. Univerzální buněčné palivo funguje i jako posel.
ATP jako signál
Signalizační úloha mimobuněčného ATP dlouho unikala pozornosti fyziologů. Nepředpokládali totiž, že by ATP, který byl dosud vnímán pouze jako molekula s ryze nitrobuněčnou funkcí, mohl mít ještě jinou důležitou úlohu. Nyní však již s jistotou víme, že molekuly ATP uvolněné z jedné buňky se vážou na specifické membránové proteiny na povrchu jiných buněk. Tyto dynamické proteiny, označované jako purinergní P2 receptory, mění po navázání mimobuněčného ATP svou strukturu, čímž je mezibuněčný signál přijat.
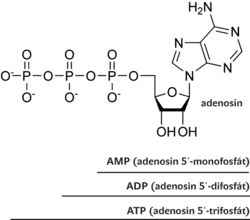 Signalizační úloha je velkou měrou založena na zvýšení koncentrace vápenatých iontů uvnitř aktivované buňky. K navýšení dochází vstupem iontů z mezibuněčného prostředí (skrze aktivované P2X receptory) nebo uvolněním z vlastních buněčných zdrojů (při aktivaci metabotropních P2Y receptorů). Na rozdíl od enzymů či membránových transportních systémů, které z ATP získávají energii jeho štěpením, je ATP pro purinergní P2 receptory pouze signalizační molekula a není hydrolyzován. Z mezibuněčného prostředí je ATP odstraňován všudypřítomnými enzymy ektonukleotidázami a jeho koncentrace je v mezibuněčném prostředí řádově menší než uvnitř buňky. Produkty enzymatického štěpení ATP (ADP – adenosindifosfát, AMP – adenosinmonofosfát či adenosin) mohou být však v mezibuněčné signalizaci paradoxně účinnější než sám ATP.
Signalizační úloha je velkou měrou založena na zvýšení koncentrace vápenatých iontů uvnitř aktivované buňky. K navýšení dochází vstupem iontů z mezibuněčného prostředí (skrze aktivované P2X receptory) nebo uvolněním z vlastních buněčných zdrojů (při aktivaci metabotropních P2Y receptorů). Na rozdíl od enzymů či membránových transportních systémů, které z ATP získávají energii jeho štěpením, je ATP pro purinergní P2 receptory pouze signalizační molekula a není hydrolyzován. Z mezibuněčného prostředí je ATP odstraňován všudypřítomnými enzymy ektonukleotidázami a jeho koncentrace je v mezibuněčném prostředí řádově menší než uvnitř buňky. Produkty enzymatického štěpení ATP (ADP – adenosindifosfát, AMP – adenosinmonofosfát či adenosin) mohou být však v mezibuněčné signalizaci paradoxně účinnější než sám ATP.
Purinergní receptory, na které se mezibuněčný ATP a produkty jeho štěpení vážou, byly popsány nedávno – v devadesátých letech minulého století. V současné době prudce roste zájem o studium účinků mimobuněčného ATP, jeho receptorů a možností léčebného využití purinergních látek. Ukazuje se totiž, že purinergní mezibuněčná signalizace je zásadní mechanismus při vnímání a přenosu bolesti, při zánětlivých procesech, při úpravě synaptického přenosu, regulaci apoptózy, uvolňování hormonů, stahu hladkých svalů, tvorbě kostí a při mnoha dalších procesech. Novým purinergním lékem je například ticagrelor, orální P2Y12 antagonista, který byl vyvinut jako alternativa clopidogrelu proti srážení krevních destiček a který inhibuje aktivaci destiček stimulovanou ADP. Neustále se objevují nové a překvapivé informace o funkcích P2 receptorů. Podrobná znalost struktury a funkce těchto proteinů vzbuzuje naději, že by mohly být objeveny nové léky účinné u řady onemocnění, například tišící chronickou neuropatickou bolest nebo potlačující proliferaci některých typů nádorů.



















