Parazit Toxoplasma a Rh-faktor
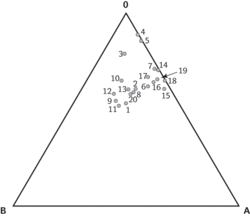
Proč se v lidské populaci vyskytují všechny čtyři krevní typy systému AB0 (viz rámeček „Krevní skupiny“), není jasné. Je ovšem pravděpodobné, že z hlediska obrany celé populace před parazity je výhodné, když se její příslušníci liší zaprvé v tom, podle čeho rozpoznávají cizorodost parazita (zásadní roli zde hrají molekuly hlavního histokompatibilního komplexu, viz Vesmír 69, 274, 1990/5), zadruhé v tom, na které povrchové struktury parazitů jejich protilátky útočí nejdřív (významnou roli zde mohou hrát řetězce cukrů navázaných na některé proteiny buněčného povrchu). V různých populacích je zastoupení krevních typů nápadně podobné (viz obr. 1). Z toho vyplývá, že při udržování všech čtyř krevních skupin v populaci se téměř jistě uplatňuje frekvenčně závislá selekce. Jakmile z nějakých důvodů zastoupení nositelů určitého krevního typu v populaci klesne, získají selekční výhodu a jejich zastoupení začne stoupat. Naopak jakmile zastoupení nositelů určité skupiny překročí rovnovážnou hodnotu, stane se příslušnost k danému typu nevýhodnou a zastoupení nositelů té skupiny začne klesat. Zatím se zdá nejpravděpodobnější, že činitelem snižujícím biologickou zdatnost nositelů hojnějšího typu budou paraziti. Ti se totiž dokážou rychle adaptovat na složení populace a zpravidla se specializují na to, aby přednostně napadali nejhojnější typ. Tento mechanismus určitě udržuje vysokou různorodost (polymorfismus) v genech hlavního histokompatibilního komplexu (viz Vesmír 78, 565, 1999/10) a s velkou pravděpodobností se uplatňuje i při udržování rovnovážného zastoupení čtyř krevních typů systému AB0.
Rh-faktor je evoluční záhada
 Evoluční biologové již od padesátých let minulého století upozorňují, že výskyt dvou hlavních krevních typů systému Rh je záhada, pro kterou nemají žádné přijatelné vysvětlení. Gen RHD, který je odpovědný za přítomnost či nepřítomnost antigenu D, a tedy za rozdíl mezi pozitivním a negativním Rh-faktorem, se vyskytuje ve dvou hlavních formách, v normální formě a ve formě poškozené. Rhnegativním lidem, kteří mají pouze poškozenou formu RHD genu, chybí na povrchu červených krvinek příslušný protein, na němž se vytváří antigen D. Imunitní systém Rh-negativních osob, které se setkaly s Rh pozitivní krví, vytváří při příštím setkání s Rh pozitivní krví velké množství protilátek. Při transfuzích se samozřejmě hlídá, aby osoba s negativním Rh dostala výhradně Rh-negativní krev. Problém nastává, když žena s negativním a muž s pozitivním Rh mají dítě, jež od otce zdědí gen pro pozitivní Rh. Při prvním porodu se zpravidla matce ani dítěti nic tak strašného nestane, nejpozději při porodu se však matka imunizuje proti červeným krvinkám novorozence a červené krvinky příštích dětí s pozitivním Rh-faktorem jsou protilátkami z jejího těla ničeny stále více. Novorozenci jsou postiženi hemolytickou nemocí, což v minulosti končívalo smrtí. Dnes se tato situace řeší tím, že se matce s negativním Rh‑faktorem podávají po porodu protilátky proti krvinkám s pozitivním Rh, čímž se z velké části zabrání její imunizaci.
Evoluční biologové již od padesátých let minulého století upozorňují, že výskyt dvou hlavních krevních typů systému Rh je záhada, pro kterou nemají žádné přijatelné vysvětlení. Gen RHD, který je odpovědný za přítomnost či nepřítomnost antigenu D, a tedy za rozdíl mezi pozitivním a negativním Rh-faktorem, se vyskytuje ve dvou hlavních formách, v normální formě a ve formě poškozené. Rhnegativním lidem, kteří mají pouze poškozenou formu RHD genu, chybí na povrchu červených krvinek příslušný protein, na němž se vytváří antigen D. Imunitní systém Rh-negativních osob, které se setkaly s Rh pozitivní krví, vytváří při příštím setkání s Rh pozitivní krví velké množství protilátek. Při transfuzích se samozřejmě hlídá, aby osoba s negativním Rh dostala výhradně Rh-negativní krev. Problém nastává, když žena s negativním a muž s pozitivním Rh mají dítě, jež od otce zdědí gen pro pozitivní Rh. Při prvním porodu se zpravidla matce ani dítěti nic tak strašného nestane, nejpozději při porodu se však matka imunizuje proti červeným krvinkám novorozence a červené krvinky příštích dětí s pozitivním Rh-faktorem jsou protilátkami z jejího těla ničeny stále více. Novorozenci jsou postiženi hemolytickou nemocí, což v minulosti končívalo smrtí. Dnes se tato situace řeší tím, že se matce s negativním Rh‑faktorem podávají po porodu protilátky proti krvinkám s pozitivním Rh, čímž se z velké části zabrání její imunizaci.
Je obtížné vysvětlit, jak před nástupem moderní medicíny mohla v genu RHD vzniknout taková různorodost a dlouhodobě se udržovat v lidské populaci. Představme si, že by se v populaci lidí s negativním Rh objevil mutant s pozitivním Rh. Jeho mužští potomci s pozitivním Rh by nutně museli mít menší biologickou zdatnost, neboť jejich novorozenci by byli postihováni hemolytickou nemocí. Obdobná situace ovšem platí i v opačném směru. V populaci osob s pozitivním Rh budou postihováni ženští potomci mutanta s negativním Rh, neboť část jejich dětí (s převahou otců s pozitivním Rh) bude postihována hemolytickou nemocí. Obecně bude platit, že hemolytickou nemocí jsou vždy více postihováni nositelé vzácnější varianty genu RHD. V důsledku toho by se různorodost v tomto genu vůbec neměla v populaci udržet, měly by zcela převládnout buď osoby s pozitivním Rh, nebo osoby s negativním Rh. Tak tomu ovšem přinejmenším v evropské populaci zdaleka není, zastoupení Rh-negativních se zde pohybuje kolem 16 %. Již v roce 1954 C. C. Li předpověděl, že různorodost v genu RHD, a tedy i v Rh krevním typu bude nejspíš udržována selekcí ve prospěch heterozygotů, tj. jedinců, kteří od jednoho rodičů zdědili normální a od druhého poškozenou variantu genu RHD. Až do loňského roku však nebylo jasné, v čem by mohla výhoda heterozygotů spočívat. Teprve nedávno se podařilo ze struktury proteinu kódovaného genem RHD odvodit, že jde s největší pravděpodobností o molekulární pumpu, která přenáší přes membránu buď oxid uhličitý, nebo amonné ionty. Jakákoli fyziologická funkce či biologické projevy této pumpy však zůstávaly neznámé. Zdálo se, že osoby s pozitivním Rh se od osob s Rhnegativním ničím (kromě rozdílného rizika hemolytické choroby novorozenců) neliší.
Na scénu vstupuje Toxoplasma gondii
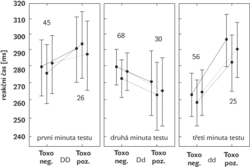 Řešení padesát let starého evolučního paradoxu naznačily poznatky, které jsme náhodně získali v roce 2000 na Přírodovědecké fakultě UK v Praze. Při studiu vlivu nákazy prvokem Toxoplasma gondii na reakční rychlost jsme zjistili, že Rh-pozitivní a Rh-negativní osoby se liší svým výkonem v testech reakčních dob. Rozsáhlé studie, které prováděli diplomanti a doktorandi ve spolupráci s pracovníky Ústavu hematologie a krevní transfuze a Ústřední vojenské Nemocnice v Praze na dobrovolných dárcích krve, vojácích základní vojenské služby a studentech Přírodovědecké fakulty, ukázaly, že se reakční rychlost osob s pozitivním a s negativním Rh skutečně liší. Aby se však rozdíly mohly projevit, je třeba studovat zvlášť osoby nakažené a nenakažené toxoplazmou. V České republice se takové studie provádějí snadno, protože doživotně je toxoplazmou nakaženo zhruba 30 % obyvatelstva. Výsledky dnes již asi osmi nezávislých studií provedených na několika tisících dobrovolníků ukázaly, že mezi osobami nenakaženými mají jedinci s negativním Rh-faktorem významně lepší výsledky v testech reakčních dob (na jednoduché podněty reagují mnohem rychleji). U osob nakažených je však situace opačná – lidé s negativním Rh mají úplně nejhorší reakční časy, zatímco reakce lidí s pozitivním Rh zůstávají zhruba stejné jako u nenakažených. Ve studii provedené na dobrovolných dárcích krve jsme měli k dispozici data umožňující rozdělit osoby s pozitivním Rh na homozygoty s dvěma normálními variantami genu RHD a na heterozygoty s jednou normální variantou genu a jednou poškozenou variantou genu, tj. s variantou, která v homozygotním stavu způsobuje negativní Rh. Jak předpověděl před 50 lety Li, nejlépe jsou chráněni právě heterozygoti (viz obr. 2), u kterých jsou reakční časy osob infikovaných toxoplazmou dokonce mírně lepší než reakční časy osob neinfikovaných. Další analýzy ukázaly, že hlavní rozdíl mezi heterozygoty a homozygoty nejspíš spočívá v tom, že reakční časy Rh-pozitivních heterozygotů zůstávají dobré i dlouho po nákaze, zatímco reakční časy homozygotů s pozitivním Rh se s dobou od infekce postupně zhoršují. Reakční časy osob s negativním Rh se nejspíš zhorší skokem brzy po nákaze.
Řešení padesát let starého evolučního paradoxu naznačily poznatky, které jsme náhodně získali v roce 2000 na Přírodovědecké fakultě UK v Praze. Při studiu vlivu nákazy prvokem Toxoplasma gondii na reakční rychlost jsme zjistili, že Rh-pozitivní a Rh-negativní osoby se liší svým výkonem v testech reakčních dob. Rozsáhlé studie, které prováděli diplomanti a doktorandi ve spolupráci s pracovníky Ústavu hematologie a krevní transfuze a Ústřední vojenské Nemocnice v Praze na dobrovolných dárcích krve, vojácích základní vojenské služby a studentech Přírodovědecké fakulty, ukázaly, že se reakční rychlost osob s pozitivním a s negativním Rh skutečně liší. Aby se však rozdíly mohly projevit, je třeba studovat zvlášť osoby nakažené a nenakažené toxoplazmou. V České republice se takové studie provádějí snadno, protože doživotně je toxoplazmou nakaženo zhruba 30 % obyvatelstva. Výsledky dnes již asi osmi nezávislých studií provedených na několika tisících dobrovolníků ukázaly, že mezi osobami nenakaženými mají jedinci s negativním Rh-faktorem významně lepší výsledky v testech reakčních dob (na jednoduché podněty reagují mnohem rychleji). U osob nakažených je však situace opačná – lidé s negativním Rh mají úplně nejhorší reakční časy, zatímco reakce lidí s pozitivním Rh zůstávají zhruba stejné jako u nenakažených. Ve studii provedené na dobrovolných dárcích krve jsme měli k dispozici data umožňující rozdělit osoby s pozitivním Rh na homozygoty s dvěma normálními variantami genu RHD a na heterozygoty s jednou normální variantou genu a jednou poškozenou variantou genu, tj. s variantou, která v homozygotním stavu způsobuje negativní Rh. Jak předpověděl před 50 lety Li, nejlépe jsou chráněni právě heterozygoti (viz obr. 2), u kterých jsou reakční časy osob infikovaných toxoplazmou dokonce mírně lepší než reakční časy osob neinfikovaných. Další analýzy ukázaly, že hlavní rozdíl mezi heterozygoty a homozygoty nejspíš spočívá v tom, že reakční časy Rh-pozitivních heterozygotů zůstávají dobré i dlouho po nákaze, zatímco reakční časy homozygotů s pozitivním Rh se s dobou od infekce postupně zhoršují. Reakční časy osob s negativním Rh se nejspíš zhorší skokem brzy po nákaze.
Že toto zhoršení reakčních časů může mít i podstatný vliv na život jednotlivce, ukazují výsledky rozsáhlé studie provedené na 3900 vojenských řidičích. Při nástupu na základní vojenskou službu byli vojáci otestováni na toxoplazmózu a Rh a po jejím skončení se ze záznamů vojenské policie zjišťovalo, zda měli, nebo neměli dopravní nehodu. Výsledky byly zcela v souladu s výsledky laboratorních testů reakčních dob. Mezi řidiči s pozitivním Rh nebyl v riziku dopravní nehody prakticky žádný rozdíl mezi nakaženými a nenakaženými. Zato mezi řidiči s negativním Rh bylo riziko nehody u nakažených toxoplazmou více než dvakrát vyšší než u nenakažených. U řidičů s negativním Rh-faktorem, jejichž vysoké hladiny protilátek ukazovaly, že se nakazili teprve nedávno, bylo riziko havárie dokonce šestkrát vyšší.
Jakým způsobem ovlivňují Rh-faktor a toxoplazmóza reakční čas, není zatím jasné. Je však vysoce pravděpodobné, že reakční časy nejsou jediná fyziologická proměnná, před jejímž zhoršováním v důsledku toxoplazmózy pozitivní Rh-faktor chrání. Při studiu vlivu toxoplazmózy na pohlavní index člověka jsme zjistili, že ženám dlouhodobě nakaženým tímto parazitem se s výrazně větší pravděpodobností narodí syn než dcera (viz Vesmír 85, 724, 2006/12) a že jejich těhotenství trvá v průměru o 1,5 dne déle. V tom se neliší ženy s pozitivním Rh-faktorem od žen s Rh-faktorem negativním. Když jsme však u těchto žen sledovali průběh těhotenství, zjistili jsme, že ženy s negativním Rh infikované toxoplazmou mají abnormálně vysoké váhové přírůstky. V 16. týdnu těhotenství byly jejich váhové přírůstky zhruba o polovinu vyšší než u ostatních žen a statisticky významný rozdíl přetrval až do konce těhotenství. Je známo, že abnormálně vysoké váhové přírůstky signalizují vliv nějakého negativního činitele (například kouření) na průběh těhotenství. Opět se zdá, že pozitivní Rh chrání osoby před negativním vlivem toxoplazmózy.
A co z toho vlastně plyne
To, že 60 let po objevu Rh-faktoru byly konečně popsány rozdíly ve vlastnostech osob s Rh‑faktorem pozitivním a negativním (tj. projev genu RHD), snad v budoucnu pomůže odhalit funkci příslušného proteinu. Již nyní nám ovšem poskytuje možné vysvětlení tří záhadných jevů spojených s Rh-systémem. Zaprvé nám ukazuje, jak mohla vzniknout a dlouhodobě se udržet různorodost v genu RHD (Rh‑polymorfismus). V populacích, kde je vysoká promořenost toxoplazmou, jsou na tom nejlépe jedinci heterozygotní, kteří mají obě formy genu RHD, a jen o něco hůře homozygoti s pozitivním Rh-faktorem. Zadruhé nám rozdílná promořenost populací toxoplazmou může vysvětlit i nápadné rozdíly v zastoupení osob s negativním Rh v různých populacích. V závislosti na klimatických podmínkách, hygienických a stravovacích zvycích a výskytu kočkovitých šelem (jediných zvířat, ve kterých se toxoplazma může rozmnožovat pohlavně) se zastoupení osob infikovaných toxoplazmou pohybuje v různých oblastech od nuly (na ostrovech, kde nejsou kočkovité šelmy) až po téměř 100 %. Je proto pochopitelné, že se v jednotlivých oblastech drasticky liší i zastoupení osob s negativním Rh-faktorem. V Africe se i v současné době pohybuje promořenost vesnické populace toxoplazmou nad 90 % a není divu, že je zde zhruba 99 % lidí s pozitivním Rh-faktorem. Zatřetí výborné reakční časy lidí s negativním Rh-faktorem nenakažených toxoplazmou nám umožňují vysvětlit i samotné rozšíření genu pro Rh‑negativitu v evropské populaci. Na rozdíl od ostatních kontinentů se zde až do příchodu domácí kočky prakticky nevyskytovaly kočkovité šelmy, s jejichž trusem obsahujícím cysty parazita by se mohl člověk dostávat častěji do styku. Na rozdíl od sousedovy kočky se vám rys ostrovid do záhonu ředkviček nejspíš nevykálí. V takových podmínkách vykazovaly největší zdatnost osoby s negativním Rh a zastoupení příslušné varianty genu v populaci tak mohlo podstatně stoupnout. Že mají naše zjištění nejspíš i praktický význam, je myslím dost zřejmé. Například jedinci s negativním Rh by měli být po prodělané toxoplazmóze minimálně několik let velice opatrní při řízení automobilů a třeba dispečeři letového provozu či profesionální řidiči s negativním Rh by měli být pravidelně a nejspíš několikrát do roka testováni na toxoplazmózu.
Muška jenom zlatá…
K objevu vlivu Rh-faktoru na odolnost osob vůči působení toxoplazmózy na reakční časy došlo v podstatě náhodou. Původně nás pouze zajímalo, zda se manipulační aktivita prvoka Toxoplasma gondii, která v přírodě prostřednictvím prodloužení reakčních časů myší zvyšuje šanci na jejich ulovení kočkou, a tedy na přenos parazita z myši do kočky, projevuje i u nakažených lidí. Byla to víceméně náhoda, že jsme část studií prováděli na dárcích krve, pro které jsou samozřejmě dostupné údaje o krevních skupinách. A když už jsme tato data měli, proč si je pořádně neprohlédnout a neotestovat na nich několik pochybných hypotéz týkajících se třeba vlivu krevní skupiny na psychiku a výkonnost osoby? To už jistě napadlo řadu lidí před námi (například v Japonsku se považuje souvislost mezi krevní skupinou AB0 a psychikou za hotovou věc a určitě se ji tam mnoho psychologů pokoušelo prokázat na skutečných datech), zatím však nikdo neměl možnost zahrnout do analýzy současně údaje o krevní skupině a o infekci toxoplazmou (v Japonsku by jim asi ani to nepomohlo, podle našich výsledků systém AB0 zřejmě s psychikou ani výkonností nesouvisí a Rh-faktor mají téměř všichni Japonci pozitivní). Inu, občas má člověk štěstí. Laskavý čtenář si možná v té souvislosti vzpomene na poučku, že štěstí přeje připraveným, my ostatní asi spíše na úsloví o tom, na koho že si to občas štěstí sedne.
Články vznikly s podporou grantů 0021620828 MŠMT a 206/07/0360 GAČR.
Literatura
Flegr J., Novotná M., Lindová J., Havlíček J.: Neurophysiological effect of the Rh factor. Protective role of the RhD molecule against Toxoplasma-induced impairment of reaction times in women, Neuroendocrinology Letters 29, 475–481, 2008/4
Li C. C.: Is the Rh facing a crossroad? A critique of the compensation effect, Am. Natural. 87, 257–261, 1953
Novotná M., Havlíček J., Smith A. P., Kolbeková P., Skallová A., Klose J., Gašová Z., Písacka M., Sechovská M., Flegr J.: Toxoplasma and reaction time: Role of toxoplasmosis in the origin, preservation and geographical distribution of Rh blood group polymorphism, Parasitology 135, 1253–1261, 2008
Flegr J., Klose J., Novotná M., Berenreitterová M., Havlíček J.: Increased incidence of traffic accidents in Toxoplasma-infected military drivers and protective effect RhD molecule revealed by a large‑scale prospective cohort study, BMC Infect. Dis. 9, 72, 2009
Slovníček
genotyp – unikátní kombinace genů jedince
fenotyp – soubor všech pozorovatelných znaků jedince, pozorovatelný výsledek spolupůsobení genotypu a prostředí
heterozygot – jedinec obsahující ve dvou odpovídajících místech chromozomového páru dvě různé varianty určitého genu
homozygot – má varianty daného genu v obou místech stejné
KREVNÍ SKUPINY
Když se řekne krevní skupina, většinou se nám vybaví AB0 a rhesus faktor (Rh). Systém AB0 rozděluje osoby do čtyř typů – A, B, AB a 0. Červené krvinky jednotlivých typů se liší řetězci cukrů navázanými na některé proteiny a lipidy buněčných membrán. Tento znak má velký význam při transfuzi krve, neboť osoby krevního typu A mohou přijmout krvinky od osob typu A nebo 0, osoby typu B od osob typu B nebo 0, osoby typu AB (univerzální příjemci) mohou přijmout krvinky od osoby kteréhokoli typu a osoby typu 0 (univerzální dárci) mohou přijmout krvinky pouze od osob typu 0. Stejné řetězce cukrů, jaké určují krevní typ, se vyskytují i na buněčné stěně některých bakterií. Osoby s krevním typem A proto nemohou vytvářet protilátky proti těm bakteriím, které nesou na povrchu stejné řetězce cukrů, neboť by tyto protilátky v jejich těle ničily i jejich vlastní červené krvinky. Obdobně to platí pro osoby s krevním typem B, pouze druhy bakterií nesoucí příslušný řetězec cukrů (proti kterým osoby s krví typu B nemohou vytvářet některé protilátky) jsou jiné. Nejhůře jsou na tom osoby s krevním typem AB, neboť ty nesou na povrchu červených krvinek oba typy řetězců cukrů, a proto je počet struktur, proti nimž nemohou vytvářet protilátky, největší. Naopak nejlépe jsou na tom osoby s krevním typem 0. I v našich studiích se ukázalo, že osoby s krevní skupinou 0 mají nejmenší a osoby s krevní skupinou AB největší pravděpodobnost nákazy T. gondii.
Ke stažení
 článek ve formátu pdf [263,46 kB]
článek ve formátu pdf [263,46 kB]
O autorovi
Jaroslav Flegr





















