Směrování cytostatik
Léčba vážně nemocných pacientů představuje pro lékaře vždycky odpovědný a nesnadný úkol. Jak intenzivně léčit, a přitom život pacienta neohrozit? Tuto otázku si občas kladou i současní onkologové, odpovědět se na ni snažil už v roce 1906 nositel Nobelovy ceny Paul Ehrlich. Agresivní léčba totiž může ohrozit životně důležité tkáně a orgány. Teoretické řešení je na první pohled jednoduché. Je třeba připravit takové léčivo nebo léčivo v takové formě, aby působilo pouze na nemocnou tkáň/orgán. Tedy léčivo směrované. Praktické řešení je ale svízelné a věnují se mu stovky laboratoří po celém světě.1)
Základem směrovaných léčiv bývá vysokomolekulární polymerní nosič, vodorozpustný nebo micelární, na který je vybranou kovalentní vazbou připojeno klasické léčivo. Chemická vazba je volena tak, aby směrované léčivo bylo během transportu neaktivní a aktivovalo se až kontrolovaným uvolňováním v místě svého působení. Proto se nerozštěpeným polymerním derivátům léčiv také někdy říká proléčiva nebo polymerní proléčiva.
Jak takové transportní makromolekuly vůbec najdou místo, kam mají léčivo doručit, a jak ho v místě žádoucího účinku uvolňují? První úkol se dá řešit dvěma způsoby, jednodušším a složitějším. Tím jednodušším je využití tzv. EPR (Enhanced Permeation and Retention; zvýšený průnik a zadržování) efektu, který byl popsán v polovině osmdesátých let profesorem Maedou z Japonska. EPR efekt je důsledkem překotně vytvořené, a proto i defektní neovaskularizace nádorů, která spolu s nedokonalou lymfatickou drenáží umožňuje v solidních nádorech pasivní nahromadění látek s vyšší molekulovou vahou, typicky polymerních proléčiv. Druhý způsob, aktivní směrování, je účinnější, ale technicky mnohem složitější. Vyžaduje, aby na cílové buňce nádoru byl jedinečný znak – něco jako poštovní schránka. A do té je třeba doručit dopis s adresou, tedy polymerní proléčivo obsahující ligandu, tj. něco jako unikátní poštovní adresu. Některé jedinečné znaky na nádorových buňkách už známy jsou, ale problém je, že je většinou nemají na svých površích všechny nádorové buňky, a tak část z nich může přežít i tak sofistikovanou léčbu, jako je léčba směrovanými cytostatiky. Jako liganda, tj. poštovní adresa, jsou v současné době kromě protilátek (většinou monoklonálních) využívány i další látky, jako jsou cukry, lektiny (bílkoviny vázající cukry), hormony, růstové faktory, transferin (cirkulující proteinový nosič železa), enzymy, vitaminy, polysacharidy a nejrůznější peptidy; prostě molekuly, pro které má cílová buňka specifický znak – receptor.
 Kontrolované uvolňování léčiva v místě jeho účinku (in situ) řeší zvolená chemická vazba mezi ním a nosičem. Odštěpit léčivo z vysokomolekulárního polymerního nosiče mohou jak extracelulární enzymy, které nádory produkují (proteázy, glukuronidázy, karboxyesterázy nebo metalloproteázy), tak intracelulární enzymy (většinou proteázy) nebo se využívá specifického vnitrobuněčného prostředí (hydrolýza při nízkém pH probíhající v endosomech a lysosomech). Výběr kovalentní vazby mezi nosičem a transportovaným léčivem je zásadní pro farmakologickou účinnost a bezpečnost celého polymerního proléčiva.
Kontrolované uvolňování léčiva v místě jeho účinku (in situ) řeší zvolená chemická vazba mezi ním a nosičem. Odštěpit léčivo z vysokomolekulárního polymerního nosiče mohou jak extracelulární enzymy, které nádory produkují (proteázy, glukuronidázy, karboxyesterázy nebo metalloproteázy), tak intracelulární enzymy (většinou proteázy) nebo se využívá specifického vnitrobuněčného prostředí (hydrolýza při nízkém pH probíhající v endosomech a lysosomech). Výběr kovalentní vazby mezi nosičem a transportovaným léčivem je zásadní pro farmakologickou účinnost a bezpečnost celého polymerního proléčiva.
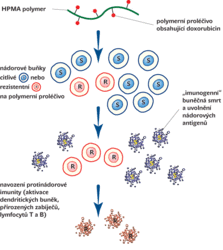
V současné době se ale ve hře o osud pacienta dostává ke slovu další hráč. A tím je imunitní systém, jehož protektivní protinádorová úloha byla sice teoreticky definována již v padesátých letech minulého století nositelem Nobelovy ceny sirem Macfarlanem Burnetem, ale od té doby mnohokrát zpochybňována. Dnes jsme ale přesvědčeni o tom, že imunitní systém skutečně může léčbu podstatným způsobem pozitivně ovlivnit. Proto je nesmírně důležité naše prioritní zjištění, že směrovaná léčiva na bázi HPMA (N-2[hydroxypropyl]methakrylamid; syntetický nosič vyvinutý na ÚMCH AV ČR, v. v. i., a československý patent) majíduální aktivitu, tj. jsou cytotoxická a imunostimulační zároveň (obr. 1). Je to možné, protože jsou směrovaná, a tak nepoškozují imunitní systém. A navíc mechanismus, kterým tato léčiva zabíjejí nádorové buňky, vede k aktivaci dendritických buněk a k zahájení protinádorové reakce. Léčba směrovanými léčivy na bázi HPMA byla doposud vždy doprovázena také vytvořením protinádorové rezistence, která chrání zvířata proti růstu experimentálního nádoru. Pokud by směrovaná léčiva měla podobný účinek i na lidské pacienty, mohla by je ochránit před potenciálním metastatickým procesem.
Léčiva na bázi HPMA jsou patentově chráněná a klinické testy byly původně přislíbeny českou, nyní mezinárodní farmaceutickou firmou.
Poznámky
1) Vývoj takových léčiv, nazývaných směrovaná polymerní léčiva (nanoterapeutika), probíhá i ve společných projektech laboratoře Nádorové imunologie v Mikrobiologickém ústavu AV ČR, v. v. i., a v oddělení Biomedicínských polymerů Ústavu makromolekulární chemie AV ČR, v. v. i.
Ke stažení
 článek ve formátu pdf [763,3 kB]
článek ve formátu pdf [763,3 kB]



















