Regenerace jater
 Chirurgická léčba zhoubných ložiskových procesů jater se v posledních letech rozvíjí díky novým operačním technikám a pooperační péči. Ne vždy je ale možno tento pokrok využít. Jestliže je objem odstraněné jaterní tkáně – parenchymu – s patologickým ložiskem příliš velký, hrozí akutní selhání jater. Ponechaný zbytkový parenchym není schopen zajistit všechny funkce jater (syntézu, detoxikaci a vylučování) a ani sám od sebe neregeneruje do té míry, aby všechen odstraněný parenchym nahradil.
Chirurgická léčba zhoubných ložiskových procesů jater se v posledních letech rozvíjí díky novým operačním technikám a pooperační péči. Ne vždy je ale možno tento pokrok využít. Jestliže je objem odstraněné jaterní tkáně – parenchymu – s patologickým ložiskem příliš velký, hrozí akutní selhání jater. Ponechaný zbytkový parenchym není schopen zajistit všechny funkce jater (syntézu, detoxikaci a vylučování) a ani sám od sebe neregeneruje do té míry, aby všechen odstraněný parenchym nahradil.
Chceme-li chirurgické možnosti léčby zhoubných ložisek v játrech rozšířit, měli bychom pochopit mechanizmus přirozené regenerace jaterního parenchymu. V malém rozsahu probíhá vlastně po celý život, průběžně nahrazuje buňky, které byly odstraněny.
Jaterní buňky lze rozdělit na hepatocyty (vlastní jaterní buňky) a cholangiocyty (buňky žlučových cest). Krom toho jsou v parenchymu ještě Kupfferovy buňky, které mají charakter tkáňových makrofágů. Parenchym můžeme pro naše potřeby rozdělit na parenchym levého laloku a pravého laloku – každý má vlastní vývodný žlučový systém a cévní zásobení jak větví portální žíly, tak větví jaterní tepny. Portální žíla zásobuje játra neokysličenou krví s vysokým obsahem vstřebaných metabolitů z nepárových orgánů dutiny břišní (žaludku, tenkého a tlustého střeva, sleziny). Jaterní tepna přináší okysličenou krev.
Embolizace portální žíly
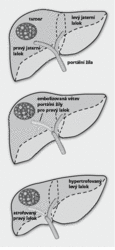
Již v roce 1920 poukázal P. Rous na to, že jaterní parenchym musí být nezbytně zásoben portální krví. Jestliže je jedna větev portální žíly vyřazena, začne v postiženém laloku ubývat parenchym (ale nedojde k nekróze), druhý lalok naopak zbytní. A právě toto kompenzační zbytnění využil r. 1984 M. Makuuchi. Nějaký čas před operací záměrně uzavřel (embolizoval) větev portální žíly (obrázek 1) v tom laloku, který obsahoval patologické ložisko. Když zdravý lalok zbytněl, bylo možno z nemocného laloku odebrat větší část tkáně, aniž hrozilo pooperační jaterní selhání.Jak zbytnění zdravého laloku vzniká? Jaterní lalok, který přestane být zásobován portální krví, podléhá atrofii, ale hepatocyty neodumřou – alespoň do jisté míry jsou zásobovány krví z jaterní tepny, i když svou funkci neplní dostatečně. Mezitím ve zdravém laloku vzrůstá průtok portální krve a v průběhu 2 až 4 týdnů se lalok zvětší do té míry, že je schopen zajistit veškeré jaterní funkce. Přesněji řečeno, vzroste v něm počet buněk. Poté tento parenchym kolonizují již zmíněné Kupfferovy buňky.
Kmenové buňky
Co je zdrojem množivé aktivity (proliferace) buněk? Starší práce hovoří o trvalé mitotické 1) aktivitě hepatocytů, která však při větším poškození není schopna zajistit náhradu jaterní masy. V parenchymu se nacházejí oválné buňky, které jsou považovány za buňky progenitorové,2 schopné diferencovat v hepatocyty a cholangiocyty. A právě u těchto buněk byla v období regenerace parenchymu zaznamenána zvýšená množivá aktivita. Nejnovější publikace však poukazují na skutečnost, že progenitorové buňky přítomné v jaterním parenchymu nemají kapacitu na to, aby zajistily dostatečnou regeneraci právě v případě velkých ztrát parenchymu, a fakticky je lze považovat jen za zdroj hepatocytů průběžně se obměňujících. Jsou zde však ještě kmenové buňky, a to jednak krvetvorné, jednak mezenchymální. O jejich významu při regeneraci jater již dnes málokdo pochybuje. Různí se však názor na vlastní mechanizmus, jímž kmenové buňky přispívají (obrázek 2).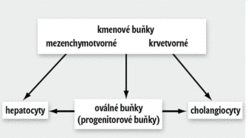 V prvé řadě mohou doplnit počet progenitorových buněk, a tím zvýší jejich množivou kapacitu. Zároveň se však mohou přímo při své množivé aktivitě diferencovat ve vlastní jaterní buňky (hepatocyty), nebo v buňky žlučovodů (cholangiocyty). Navíc mají kmenové buňky jednu zvláštní schopnost, která je však více než diskutabilní. Jsou schopny fúzovat jak se zdravou, tak s poškozenou buňkou jater, a tím jí jednak vrátí její funkci, jednak předají schopnost množit se. Kmenové buňky nejsou jen předmětem studií, ale byly již použity k zesílení účinku opravného „zvětšení“ právě po embolizaci větve portální žíly.
V prvé řadě mohou doplnit počet progenitorových buněk, a tím zvýší jejich množivou kapacitu. Zároveň se však mohou přímo při své množivé aktivitě diferencovat ve vlastní jaterní buňky (hepatocyty), nebo v buňky žlučovodů (cholangiocyty). Navíc mají kmenové buňky jednu zvláštní schopnost, která je však více než diskutabilní. Jsou schopny fúzovat jak se zdravou, tak s poškozenou buňkou jater, a tím jí jednak vrátí její funkci, jednak předají schopnost množit se. Kmenové buňky nejsou jen předmětem studií, ale byly již použity k zesílení účinku opravného „zvětšení“ právě po embolizaci větve portální žíly.
Cytokiny
Co nutí buňky, aby zvyšovaly svůj počet (proliferovaly), a tím zahájily regeneraci? Připomeňme P. Rouse, který předpokládal, že faktor vyvolávající chorobu jater je obsažen v portální krvi. Vlastní regenerace jater se však účastní řada cytokinů a růstových faktorů, které se z větší části tvoří právě v játrech, a to v několika etapách. Již několik hodin po vyřazení části jaterního parenchymu vzroste sérová hladina interlukinu 6 a jednoho z faktorů nekrotizujících tumor (TNF-alfa). Podle toho, jak dalece hladina vzroste, lze odhadnout i rozsah poškození. Předpokládá se, že se tyto dva cytokiny podílejí na zahájení regenerace. Pokud jsou však exprimovány v menším množství (například v důsledku jaterního selhání po rozsáhlé resekci), regenerace jaterního parenchymu se zpomalí. Začátek proliferace je provázen vzestupem růstového faktoru hepatocytů (HGF), epidermálního růstového faktoru (EGF) a transformujícího růstového faktoru alfa (TGF-alfa). Růstový faktor hepatocytů je produkován neparenchymovými jaterními buňkami a podněcuje tvorbu parenchymových buněk, zatímco transformující růstový faktor alfa produkují parenchymové buňky k své vlastní stimulaci. Konec proliferace je naopak provázen vzestupem sérové hladiny transformujícího růstového faktoru beta (TGF-beta), který produkují hepatocyty, když dosáhnou dostatečné celkové funkční kapacity. Většinu zmíněných faktorů ovšem produkují nejen vyjmenované buňky, ale – jak je u cytokinů a růstových faktorů zvykem – v menším množství i ostatní buňky. Je to pochopitelné, neboť některé cytokiny se účastní i jiných procesů (například zánětů).Regenerace – komplex dějů
Pro hlubší porozumění těmto dějům je nezbytné dále tyto procesy studovat. Zaměřit se nejen na jednotlivé děje, ale i na komplex regenerace jater. Jestliže plně pochopíme mechanizmus regenerace, můžeme zvýšit rozsah, počet i efektivitu resekčních výkonů v chirurgické léčbě ložiskových procesů jater.Práce byla podpořena granty IGA MZ CR 8860/1-3, 8301-3/2005 a výzkumným záměrem MSM 0021620819.
Literatura
Rous P., Larimore L. D.: Relation of the portal flow to liver maintenance. A demonstration of liver atrophy conditional on compensation, J. Exp. Med. 31, 609–632, 1920Makuuchi M., Takayasu K., Takayama T.: Preoperative transcatheter embolization of portal venous branch for patient receiving extended lobectomy due to the bile duct carcinoma, J. Jpn. Soc. Clin. Surg. 45, 14–20, 1984
Jiang Y., Jahagirdar B. N., Reinhardt R. L., Schwartz R. E., Keene C. D., Ortiz-Gonzales X. R. et al.: Pluripotency of mesenchymal stem cells derived from adult marrow, Nature 418, 41–49, 2002
Poznámky
Ke stažení
 článek ve formátu pdf [564,69 kB]
článek ve formátu pdf [564,69 kB]



















