Teorie deprese
Víme již, že deprese není jen „mizerná nálada“, ale porucha vyznačující se chorobnou změnou nálady. Tímto onemocněním se Vesmír nezabývá poprvé. O rozdílu mezi normální a patologickou náladou a o různých typech patologických nálad jsme psali ve Vesmíru 76, 125, 1997/3, o okolnostech, za nichž chorobné nálady vznikají, ve Vesmíru 76, 665, 1997/12. Proto se následující text bude zabývat pouze „velkou depresí“, a nikoli kombinovanými onemocněními, která byla zmíněna v předchozích článcích. Naším cílem je stručně shrnout vše podstatné, co je o teoriích deprese známo, zejména pak nejnovější poznatky. Čtenáři s hlubším zájmem o toto téma si mohou přečíst nezkrácenou verzi článku na našich www stránkách. Red.
Jak se deprese pozná
Čím se deprese liší od špatné nálady? Při depresi jakožto onemocnění se příznaky projevují po řadu týdnů až měsíců. Míra a struktura těchto příznaků se vyhodnocuje pomocí posuzovacích stupnic, například Hamiltonovy stupnice. 1) Diagnóza se stanovuje podle kritérií uvedených v rámečku.- Laboratorní nálezy. U části depresivních nemocných se mimo jiné zjišťují patologické hodnoty neuroendokrinních testů v oblasti řízení osy hypotalamus-hypofýza-štítná žláza a osy hypotalamus-hypofýza-nadledvinky.
- Výskyt a genetika. První fáze afektivní poruchy se vyskytne většinou před 30. rokem věku. Depresivní porucha může přijít v kterémkoli životním období. Průměrný věk výskytu deprese je 40 let (mánie 30 let). Mezi spouštěcí faktory patří alkohol, chronická tělesná onemocnění, ztráta rodiče v dětství a různá zátěž. Způsob dědičnosti není znám. Je-li jeden z rodičů postižen bipolárním onemocněním (střídá se deprese a mánie), je u dítěte asi 25% pravděpodobnost výskytu. Jsou-li postiženi oba rodiče, je pravděpodobnost výskytu 50–75 %. Pro jednovaječné dvojče je při výskytu u druhého pravděpodobnost 40–70 %, u dvojvaječných je to 20 %. U depresivní poruchy (unipolární, bez výskytu mánie) je při postižení jednoho rodiče pravděpodobnost výskytu u dítěte 10–13 %. V celé populaci trpí depresí 2–3 % mužů a 5–10 % žen (mánií 1 % mužů i žen).
Co je příčinou deprese
- Psychoanalytické teorie. Deprese je promítnutí milovaného objektu do sebe a jeho trestání za to, že nás opustil. Jestliže objekt je nenávratně ztracen, zármutek může nabýt podoby „velké deprese“ s pocity viny, beznaděje atd.
- Kognitivní teorie. U poruch nálady jde o zobecnění nežádoucích kognitivních pochodů na základě nějakého emočního traumatu, což se projevuje jako:
- záporný pohled na sebe („věci jsou špatně, protože já jsem špatný“),
- záporné chápání zkušenosti („všechno vždycky bylo špatně“),
- záporný pohled do budoucna („nic nemá cenu, všechno stejně špatně dopadne“).
- Teorie naučené bezmocnosti vysvětluje depresi jako důsledek ztráty vlivu na události. Naučená bezmocnost je termín odvozený z experimentů na zvířatech, která dostávala šoky v takovém uspořádání, že nemohla ani ovlivnit jejich podávání, ani utéci.
- Sociobiologická teorie vysvětluje evoluční úlohu deprese jako jevu, který provází pád ve společenském žebříčku (hierarchii dominance) a chrání tak jedince před zabitím (depresivní jedinci nebojují o svou příčku). Deprese pomáhá udržovat hierarchii dominance ve společenství.
- Teorie vleklého stresu poukazuje na degenerativní změny v některých částech mozku vlivem dlouhodobého nadměrného působení kortikoidních hormonů, které se vyplavují při stresu.
- Biologické hypotézy zahrnující mozkové neurotransmitery (viz dále).
Katecholaminová hypotéza
Zatímco dnes je rozšířena i na serotonin, původní verze byla noradrenalinová – při depresi je ho nedostatek. Z toho by vyplývalo, že receptory jsou málo stimulovány a přenos vzruchu je snížen. V duchu hypotézy by agonisté (látky stimulující noradrenalinový receptor) měli mít antidepresivní účinky, antagonisté (blokující účinek agonistů) by měli depresi vyvolávat. V moči depresivních nemocných by mělo být méně produktů této látky. Vzhledem k předpokládanému nedostatku noradrenalinu a serotoninu by při depresi mohla být relativní převaha acetylcholinu.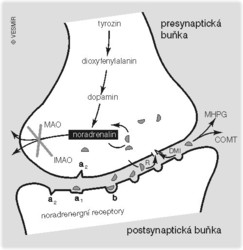 Řada těchto předpokladů do sebe skutečně logicky zapadá, jenže žádný systém zprostředkujících látek nelze uvažovat samostatně. Mezi jednotlivými okruhy je komplikované funkční spojení, kdy se např. dopaminergní a noradrenergní systémy vzájemně podporují, kdežto kyselina γ-aminomáselná ostatní systémy tlumí. Navíc mozek prochází kritickými obdobími, kdy má setkání různých systémů nezvratné následky. Tak je pro rozvoj noradrenergních struktur nezbytná přítomnost hormonů štítné žlázy v časném poporodním období, na činnost neuropřenašečových systémů má vliv věk, pohlaví ad.
Řada těchto předpokladů do sebe skutečně logicky zapadá, jenže žádný systém zprostředkujících látek nelze uvažovat samostatně. Mezi jednotlivými okruhy je komplikované funkční spojení, kdy se např. dopaminergní a noradrenergní systémy vzájemně podporují, kdežto kyselina γ-aminomáselná ostatní systémy tlumí. Navíc mozek prochází kritickými obdobími, kdy má setkání různých systémů nezvratné následky. Tak je pro rozvoj noradrenergních struktur nezbytná přítomnost hormonů štítné žlázy v časném poporodním období, na činnost neuropřenašečových systémů má vliv věk, pohlaví ad.
Koncem 70. let byli mnozí badatelé názorností katecholaminové hypotézy oslněni natolik, že odmítali přijmout řadu nálezů, které výše uvedeným předpokladům odporovaly. Časem se ale zjistilo, že ačkoli antidepresiva imipraminového typu zvyšují nabídku noradrenalinu na synaptické štěrbině, přesto nezvyšují, nýbrž naopak snižují přenos vzruchu cestou noradrenergních β-receptorů, které znecitlivují (viz P. Jirounek, Vesmír 75, 65, 1996/2 a následující díly jeho seriálu). Pohlédněme letmo, jak jednotlivé mediátorové hypotézy vypadají dnes.
- Noradrenergní systém. Výchozími látkami jsou aminokyselina DL-fenylalanin a L-dopa. Byly popsány euforizující a aktivující účinky fenylalaninu u parkinsoniků (viz tabulku Neurodegenerativních onemocnění, Vesmír 78, 330, 1999/6) a antidepresivní účinky. V některých zemích se DL-fenylalanin distribuuje do obchodů jako antidepresivum. Novější studium fenylketonurie (nemoci způsobené defektem jaterního enzymu fenylalanin-hydroxylázy) však naznačuje, že fenylalanin může antidepresivní účinky mařit. Sporné jsou i výsledky L-dopa. Někteří badatelé neshledali antidepresivní účinky Ldopa v dávce 150–1000 mg/den a ti, kteří je shledali, je nepovažují za výrazné.
Z původní představy, že výsledný produkt (metabolit noradrenalinu) v moči a mozkomíšním moku nemocných by měl být snížen, zbývá snad jen to, že jeho průměrná koncentrace v moči je vyšší u monopolárních depresí než u depresí bipolárních. Jelikož pouze 20 % výsledného produktu v moči je mozkového původu, neobjasňují tyto studie vztah afektivních poruch a katecholaminového metabolizmu.
Důležitým enzymem noradrenergního metabolizmu je tyrozin-hydroxyláza. Histochemickou metodou se ukázal osm týdnů přetrvávající vzestup poselské m-RNA, která kóduje tyrozin-hydroxylázu v mozku po aplikaci elektrokonvulzí, vyvolávajících cosi jako umělý epileptický záchvat s křečemi. Mělo se za to, že žádná jiná procedura nepůsobí tak dlouhodobé změny v genové expresi na úrovni centrálního nervstva. Změny ostatních enzymů se jako charakteristické znaky afektivních poruch nepotvrdily.
- Serotonergní systém. Výchozí látkou je jednak 5-hydroxy-tryptofan, jehož příjem přes mozkomíšní bariéru je u depresivních pacientů snížen. Tento prekurzor serotoninu vykazuje ve spodní střední prefrontální kůře zvýšené využití, čímž místně vyrovnává povšechný nedostatek serotoninu. Dalším prekurzorem je L-tryptofan, který má ne zcela doložené antidepresivní účinky. Navíc jsou prokázány jeho účinky hypnotické. L-tryptofan je také obchodně rozšiřován.
Výsledným produktem metabolizmu serotoninu je kyselina hydroxyindoloctová. Našla se nepřímá závislost koncentrace této kyseliny v mozkomíšním moku a depresivních příznaků (včetně sebevražedných pokusů). Podobných nálezů je řada, ale je také dost zjištění normálních hladin při depresi. Současné výsledky tedy nepodporují katecholaminovou ani serotoninovou hypotézu deprese v její původní podobě.
Serotoninová hypotéza však koncem 80. let opět ožila, protože je v souladu nejen s nedostatkem tryptofanu vyvolávajícím depresi, ale i s příznivým působením 5-hydroxy-tryptofanu na spánek, s pozitivní rolí serotoninu při útlumu bolesti, s bolestmi jakožto příznakem deprese, a zejména s antidepresivní účinností inhibitorů zpětného příjmu serotoninu do nervových zakončení (tzv. SSRI, jako fluoxetin) ad.
Desenzibilizační hypotéza
Na první pohled by se zdálo, že důraz na receptorovou plasticitu obrátil původní dogma v opak: u deprese je noradrenergní převaha. Zvýšená citlivost presynaptických receptorů bránících výdeji vede k přecitlivělosti postsynaptických receptorů a nakonec ke zvýšenému přenosu signálu cestou noradrenalin-β-receptor v mozkových neuronech. Tomu by nasvědčovala i skutečnost, že nejenom léčba antidepresivy, ale i elektrokonvulzivní léčba působí zřejmě na receptory mechanizmem „down-regulation“. Některé autory tyto skutečnosti vedly k pokusům o logické sloučení nálezů: Ať již je deprese spojena s nedostatkem, nebo s přebytkem noradrenergního přenosu, příznivé ovlivnění tymoleptiky se dá vždy vysvětlit mechanizmem jejich zásahu do tohoto přenosu.Fridolin Sulser a Jerzy Vetulani se v 80. letech pokusili formulovat hypotézu, podle které není pro antidepresivní účinky léku rozhodující jeho schopnost vazby na receptory pro neuropřenašeče, nýbrž to, že působí (ať už jakkoli) snížení citlivosti adenylcyklázového přenosového systému spřaženého s noradrenalinovými receptory, anebo „down-regulation“ těchto receptorů. Přitom se snižuje přenos signálu. Tyto účinky jsou společné antidepresivům s různými farmakodynamickými vlastnostmi, a dokonce i nefarmakologickým postupům, jako je léčba světlem, nespavostí a elektrokonvulzemi. Rozhodující tedy není, jak se dosud soudilo, zvýšená nabídka noradrenalinu na štěrbině.
- Dysregulační hypotéza. Blokátor zpětného příjmu noradrenalinu demetylimipramin působí na citlivost adenylátcyklázy či hustotu receptorů pouze tam, kde se serotoninergní a noradrenergní vlákna prolínají, nikoliv třeba v periferních tkáních. Hypotéza svědčí pro těsné funkční spřažení serotoninergního a noradrenergního systému v mozku. Její autoři původní katecholaminovou hypotézu přirovnávají k modelu cukrovky I. typu, kde je nedostatek inzulinu, zatímco dysregulační hypotézu přirovnávají k cukrovce II. typu, kde hladiny inzulinu mohou být zvýšeny, sníženy i nezměněny. Onemocnění tedy není manifestací nějakého nadbytku či nedostatku přenašeče, nýbrž mnohorozměrné poruchy rovnováhy.
- Omezení desenzibilizační hypotézy. Ani sám J. Vetulani, autor desenzibilizační hypotézy, není s jejím výkladem spokojen. Říká, že je málo pravděpodobné, aby se působení psychofarmaka omezovalo pouze na jedinou podskupinu receptorů. Vetulani se domnívá, že vlivem antidepresivní léčby se v noradrenergním systému usnadní přenos signálu cestou jednoho typu postsynaptických receptorů, zatímco u jiného typu dochází k znecitlivění. Podle této verze je „regulace dolů“ vyrovnávacím mechanizmem cíleným obzvláště k udržení homeostázy gliových (podpůrných) buněk. Studium jedné podskupiny receptorů nemůže tedy pominout vzájemné propojení různých receptorů a druhotných přenašečových systémů. Spřažení receptorů s G-proteiny či G-proteinů s enzymy syntezujícími druhé posly je řízeno zase jinými receptory, a tak dlouhodobá aplikace antidepresivních látek může ovlivňovat nitrobuněčné děje postsynaptických neuronů rozmanitými způsoby.
Onemocnění samo je možná důsledkem pokleslé schopnosti organizmu přizpůsobit se vnitřním změnám a lék pouze pomůže opět této schopnosti dosáhnout. Tak lze vysvětlit, proč antidepresiva nemění náladu zdravých lidí.
- Ostatní systémy. Pro úplnost vyjmenujme ještě dřívější ojedinělé nálezy změn v ostatních přenašečových systémech u deprese: dopaminergní přenos, cholinergní přenos, endorfiny, kortikoliberin.
Nedávno se původní teorie deprese začala rozpadat. Na jedné straně se zdá, že antidepresivní postupy zdaleka nemusí zahrnovat pouze monoaminergní systémy, na druhé straně se mechanizmus působení dosavadních antidepresiv může vysvětlovat zcela novým způsobem. Z tohoto hlediska je velice zajímavý vztah deprese a bolesti.
Deprese a bolest
Jedním z hlavních mediátorů bolesti je látka P (dekapeptid), vyskytující se v zadních provazcích míšních. Zjistilo se, že je zastoupena také v mozku, kde obsazuje neurokininové NK1-receptory. Ty jsou vysoce exprimované právě v limbickém systému, který řídí emotivitu. Nedávno se ukázalo, že antidepresiva snižují syntézu látky P. Jestliže aktivujeme centrální dráhy zprostředkované látkou P, vyvoláme averzivní chování (morčata například vydávají zvuky, které jsou obdobou lidského naříkání). Antagonista látky P, morfolin MK-869, a příbuzné látky blokují u morčat „nářek“ způsobený látkou P nebo odloučením od matky. Tento účinek je závislý na afinitě k NK-receptorům a na dostupnosti té které látky v mozku. V Science se loni objevila práce zásadního významu, která je výsledkem výzkumu zahrnujícího část biochemickou, zvířecí modely, preklinické studie a srovnávací studii látky v psychiatrii předtím nepoužité, jež naznačuje zcela nový mechanizmus antidepresivního působení. Antagonista látky P (blokující její činnost), MK-869, totiž prokázal ve srovnání s placebem a paroxetinem výrazné antidepresivní účinky ve studii zahrnující celkem téměř 200 pacientů a kontrolních osob (obrázek).
V Science se loni objevila práce zásadního významu, která je výsledkem výzkumu zahrnujícího část biochemickou, zvířecí modely, preklinické studie a srovnávací studii látky v psychiatrii předtím nepoužité, jež naznačuje zcela nový mechanizmus antidepresivního působení. Antagonista látky P (blokující její činnost), MK-869, totiž prokázal ve srovnání s placebem a paroxetinem výrazné antidepresivní účinky ve studii zahrnující celkem téměř 200 pacientů a kontrolních osob (obrázek).
Lze tedy říci, že deprese a bolest spolu souvisejí. Antagonisté látky P působí výrazně protidepresivně. Protože neovlivňují noradrenergní a serotonergní funkce, znamená to zřejmě objev nového mechanizmu antidepresivního působení. Z tohoto pohledu není nikterak přehnané hovořit o depresi jako o psychické bolesti.
Molekulární a buněčná hypotéza deprese
U zdravých lidí nelze nedostatkem noradrenalinu nebo serotoninu spolehlivě vyvolat depresi. Zároveň je však téměř jisté, že u těch, kteří chorobnou depresi mají nebo měli, lze manipulací s monoaminergními systémy její projevy výrazně ovlivnit. Deprese může vzniknout i jinak než nedostatkem katecholaminu, ale dodáním katecholaminu ji lze tlumit. Předpokládá se úbytek hipokampálních neuronů dlouhodobým působením stresu. Dále je zřejmé, že k antidepresivnímu působení není nezbytně nutné znecitlivění β-adrenoreceptorů či receptorů serotoninu (S2). Navíc nástup klinického účinku antidepresiv je přece jenom delší než rozvoj desenzibilizace. A do třetice – koncentrace S2-receptorů je po elektrokonvulzích zvýšena, ne snížena. Můžeme se na to ovšem dívat opět tak, že „regulace nahoru a dolů“ různých receptorových populací je pouze odezvou na změněné aktivity neuropřenašečů, a je tedy důsledkem dlouhodobého ovlivnění neuropřenosu antidepresivní léčbou. Přitom nikdy úplně nevymizí vazebná místa, takže vždy zbývá dost receptorů pro zprostředkování účinku (obrázek). To znamená, že dlouhodobé užívání antidepresiv má za následek přece jen trvalou aktivaci nitrobuněčných převodních systémů, které zprostředkovávají přenos signálu od monoaminergních receptorů. Nitrobuněčné převodní systémy jsou zhruba dvojího druhu: jednak závislé na druhotných poslech a ovládané klasickými neuropřenašeči, jednak řízené takovými receptory, které zahrnují protein-tyrozinkinázy nebo s nimi interagují a jsou ovládány většinou neurotrofními faktory a cytokiny. Aktivace těchto receptorů ovlivňuje další nitrobuněčné kaskády, např. mitogenem aktivovanou proteinkinázovou cestu. Právě tyto nedávno probádané struktury hrají zřejmě dosud netušenou roli ve zprostředkování antidepresivního účinku léků. Mozek se na zevní prostředí významným dílem adaptuje opětným utvářením nervových větvení a synaptických spojení. Přitom dochází jak k oslabení při poškozujících vlivech, tak k rašení působením vlivů podporujících růst. Zdá se, že tyto mechanizmy se uplatňují při rozvoji deprese i při její léčbě. Jako první začal systematicky obracet pozornost k možné poruše exprese genů u depresivního onemocnění R. Post (1992), který s poukazem na to, že pro rozvoj deprese jsou rizikem zejména předchozí fáze onemocnění, přirovnal neuronální děje při afektivní poruše k situaci, kdy se podprahovým drážděním neuronu snižuje práh pro odpověď na další dráždění (tzv. kindling).
Nitrobuněčné převodní systémy jsou zhruba dvojího druhu: jednak závislé na druhotných poslech a ovládané klasickými neuropřenašeči, jednak řízené takovými receptory, které zahrnují protein-tyrozinkinázy nebo s nimi interagují a jsou ovládány většinou neurotrofními faktory a cytokiny. Aktivace těchto receptorů ovlivňuje další nitrobuněčné kaskády, např. mitogenem aktivovanou proteinkinázovou cestu. Právě tyto nedávno probádané struktury hrají zřejmě dosud netušenou roli ve zprostředkování antidepresivního účinku léků. Mozek se na zevní prostředí významným dílem adaptuje opětným utvářením nervových větvení a synaptických spojení. Přitom dochází jak k oslabení při poškozujících vlivech, tak k rašení působením vlivů podporujících růst. Zdá se, že tyto mechanizmy se uplatňují při rozvoji deprese i při její léčbě. Jako první začal systematicky obracet pozornost k možné poruše exprese genů u depresivního onemocnění R. Post (1992), který s poukazem na to, že pro rozvoj deprese jsou rizikem zejména předchozí fáze onemocnění, přirovnal neuronální děje při afektivní poruše k situaci, kdy se podprahovým drážděním neuronu snižuje práh pro odpověď na další dráždění (tzv. kindling).
Na obrázku je schematický souhrn zcela nových představ o genomických účincích antidepresiv. V pokusech na krysách se ukázalo, že dlouhodobé podávání látek bránících zpětnému příjmu serotoninu a noradrenalinu do presynaptického zakončení vede cestou receptor-G-protein-adenylátcykláza-cAMP-proteinkináza k aktivaci CREB (=cAMP Response Element Binding Protein) mj. v hipokampu. To má za následek expresi genů, které kódují mozkové růstové faktory. Přitom doba nutná k vyvolání odpovědi CREB odpovídá době nástupu klinického účinku antidepresiv (zhruba 1 až 3 týdny). Nutnost ovlivnění CREB by tedy vysvětlovala rozpor mezi rychlou aktivací cAMP a dlouhou dobou nástupu klinického účinku antidepresiv.
Ovšem ne všechny geny, které jsou řízeny elementem odpovědi na cAMP, se exprimují působením antidepresiv. K zvýšení činnosti cAMP systému a CREB také nedochází ve všech mozkových oblastech. Navíc exprese genů závisí na vzájemném působení více promotorů (úseků DNA obsahujících signály pro započetí transkripce) a transkripčních faktorů. Zatím se neví, které geny se vlastně působením antidepresiv uplatní. Dosud se podařilo identifikovat BDNF (Brain Derived Neurotrophic Factor) a jeho receptor trkB.
BDNF patří mezi mozkové růstové faktory, které jsou nezbytné nejenom pro rozvoj a diferenciaci mnoha neuronů ve vývoji mozku, ale také k udržování a přežití neuronů v mozku dospělém. Působení těchto faktorů je zprostředkováno vazbou na receptory trkB, které aktivují protein tyrozinkinázu na nitrobuněčné části receptoru. Jsou první zprávy o tom, že BDNF má antidepresivní účinky. BDNF a trkB jsou v hipokampu zvýšeny vlivem různých antidepresivních modalit a elektrokonvulzí. Navíc BDNF podporuje růst serotonergních a noradrenergních vláken a chrání je před neurotoxickým poškozením. Zde se otevírá pole k testování řady dílčích hypotéz (např. vztah různých antidepresiv a jiných látek k růstovým nervovým faktorům) a ke zkoumání neurotropních faktorů v psychiatrii.
Neurotropiny patrně hrají důležitou roli při rozvoji deprese. Stres ze znemožnění pohybu vede k drastickému snížení exprese BDNF v krysím hipokampu. Bylo by na místě zkoumat, zda podobný dopad má i stres psychosociální. Trvalá zátěž spojená s hyperkortikalizmem (zvýšenou hladinou hormonů kůry nadledvin) působí ochabnutí nebo i smrt zranitelných hipokampálních neuronů u krys a primátů. Podobné účinky má nedostatek kyslíku, cytokiny, omezení cukru (hypoglykemie) aj. Schopnost hipokampu tlumit hypotalamo-hypofýzo-adrenální osu je u depresivních nemocných často snížena. Podle ojedinělých zpráv mají depresivní nemocní vskutku mírně zmenšený objem hipokampu a jiných struktur. Tato atrofie by mohla být důsledkem útlumu BDNF při přetrvávajícím stresu. Otázkou ovšem je, zda tomu tak není pouze u některých typů depresí.
 Na pozadí deprese je tedy drobná neurodegenerativní porucha mozku, způsobená hromaděním drobných „stresových“ nebo i jiných defektů (např. po prodělaném infarktu) u citlivého jedince, viz též schéma v článku Poznamenáni ohněm, Vesmír 76, 125, 1997/3. Zopakujme pouze stručně, že biologická zátěž, genetická vloha, psychologická zátěž a negativní událost ve vývoji osobnosti (ztráta rodiče) společně změní hladiny neuropřenašečů, změní receptory, růst synapsí ad., v důsledku čehož vznikne deprese a ta zas zpětně působí změny hladin neuropřenašečů atd.
Na pozadí deprese je tedy drobná neurodegenerativní porucha mozku, způsobená hromaděním drobných „stresových“ nebo i jiných defektů (např. po prodělaném infarktu) u citlivého jedince, viz též schéma v článku Poznamenáni ohněm, Vesmír 76, 125, 1997/3. Zopakujme pouze stručně, že biologická zátěž, genetická vloha, psychologická zátěž a negativní událost ve vývoji osobnosti (ztráta rodiče) společně změní hladiny neuropřenašečů, změní receptory, růst synapsí ad., v důsledku čehož vznikne deprese a ta zas zpětně působí změny hladin neuropřenašečů atd.
Zdá se tedy, že antidepresiva díky svým genomickým účinkům chrání, či dokonce „vyživují“ neurony v hipokampu a jiných strukturách mozku. Neuronální rašení se objevuje také po elektrokonvulzích. Molekulární hypotéza deprese by mohla podnítit vývoj nových antidepresivních prostředků. Mělo by jít především o látky zasahující celý systém příčin a rozvoje depresivního onemocnění. Jednou z možností je např. pomocné použití látek tlumících fosfodiesterázu, která rozkládá cAMP. Není vyloučeno, že exprese genů může být ovlivněna magnetickou stimulací.
Nová, „molekulární“ teorie deprese jistě povede k řadě nápadů, jak hlouběji proniknout do příčin a mechanizmu rozvoje tohoto skličujícího onemocnění a jak vylepšit léčebné možnosti.
/redakčně kráceno a upraveno/
Literatura
Höschl C.: Teorie deprese, Psychiatrie 1998/2, 78–85Höschl C., Stárka L., Roth Z., Vokálková J., Jaššová J.: A specific laboratory test for primary depression, Acta Univ. Carolinae Medica, Praha 1985
Höschl C.: Neuroendokrinologie v psychiatrii, Avicenum, Praha 1989
Poznámky
DIAGNÓZA VELKÉ DEPRESE
Pacient má zároveň všechny hlavní příznaky (zvýrazněné písmo):
- Nejméně pět z následujících příznaků bylo přítomno během téhož 2týdenního období a jejich výskyt představuje změnu oproti předchozímu období; alespoň jedním z nich je buď depresivní nálada, nebo ztráta zájmu či potěšení. Nepatří sem příznaky způsobené celkovým onemocněním či bludy a halucinace vyvolané něčím jiným než poruchou nálady.
- Depresivní nálada po většinu dne téměř každý den, ať již subjektivně sdělovaná (např. pocity smutku či prázdnoty), či pozorovaná jinými (např. uplakanost).
- Nápadně snížený zájem či potěšení v téměř všech činnostech po většinu dne a téměř každý den, ať již subjektivně sdělovaný, nebo pozorovaný jinými.
- Významný hmotnostní úbytek, který není dán dietou, nebo hmotnostní přírůstek (např. změna tělesné hmotnosti o více než 5 % za měsíc), nebo změna chuti k jídlu téměř každý den.
- Nespavost či nadměrná spavost téměř každý den.
- Psychomotorický neklid či útlum téměř každý den (pozorovatelný jinými).
- Únava či ztráta energie téměř každý den.
- Pocity zbytečnosti či nadměrné nebo nepřiměřené viny (které mohou být bludné) téměř každý den.
- Snížená schopnost myslet a soustředit se, popř. nerozhodnost, téměř každý den, ať již subjektivně sdělovaná, či pozorovaná jinými.
- Vracející se myšlenky na smrt (nikoli pouze strach ze smrti).
- Příznaky nesplňují kritéria pro smíšený stav (jiná kategorie).
- Příznaky působí klinicky významný škodlivý stres či narušení v sociálních, pracovních a jiných důležitých oblastech činnosti.
- Příznaky nejsou důsledkem přímého působení nějaké látky (např. drogy) nebo obecně medicínského stavu (např. snížené funkce štítné žlázy).
- Příznaky nelze připsat na vrub zármutku např. po ztrátě milované osoby, přetrvávají déle než dva měsíce či jsou provázeny nápadným funkčním narušením, chorobným zaobíráním se beznadějí, myšlenkami na sebevraždu, psychotickými příznaky či psychomotorickým zpomalením.
Miloš Kopecký
trpěl řadou závažných chorob, které překonával s nesmrtelností kocoura. Jedna však mezi nimi dominovala a tu sám považoval za nejhorší, za torturu, proti níž zlomená končetina nebo resekce žaludku jsou jen drobné nepříjemnosti: maniodepresivita. Trpěl jako málokterý z českých umělců naší doby. Ještě před svou smrtí mi dal písemný souhlas, že mohu o jeho chorobě psát. Činím tak rád, ve službách jeho památky.
Otec Miloše Kopeckého celý život trpěl depresemi, ale nikde se neléčil. Miloš měl raději matku, ta zahynula v koncentračním táboře. Udávají-li se jako důležití činitelé při rozvoji maniodepresivity jak dědičnost, tak ztráta blízkého jedince v mládí, pak Miloš Kopecký splňoval předpoklady k tomuto onemocnění měrou vrchovatou. Byl jedináčkem, vychováván rodiči celkem v harmonii, nikam do školky nechodil... V r. 1944 (dvaadvacetiletý) byl po 7 měsíců vězněn v koncentračním táboře... Rodinných tragédií a rozkolů si užil dost. Dcera z prvního manželství v 16 letech spáchala sebevraždu.
Onemocnění u něho probíhalo tak, že několikaměsíční deprese se střídaly s poněkud kratšími mániemi. Mezitím bývala i období bez příznaků, tzv. remise. Kopecký byl otrokem svých fází: žádný závazek, žádné angažmá (ve filmu, v televizi), žádný zájezd nemohl slíbit s jistotou. Nikdy nevěděl, kdy přijde to strašlivé depresivní ochromení, ve kterém pak setrvával v hodině mezi vlkem a psem, ani živ ani mrtev, ani bdělý ani spící, celé dny v pyžamu a nevycházel. Dělat nemohl nic, ale nedělat něco nesnesl. Chtěl nežít. Možná to byla právě násilná smrt první dcery, hrůzný skon matky a vědomí toho, že jednou přijde ona blažená mánie, co ho uchránilo od sebevraždy. A byly chvíle, kdy i v tomto stavu vyšel večer do divadla a hrál. Jiří Hrzán mi kdysi řekl, že profesionalita je, když vám zemře otec a vy ten večer hrajete v komedii tak, že se sál za břicha popadá...
V obdobích manických (nebo spíše hypomanických) lékaře nevyhledával, to raději tvořil. Sám jsem jej v hypománii zažil snad jen dvakrát. To bez ustání mluvil, hýřil humorem, perlil vtípky, stáčel hovor k dámám, ptal se na intimní vztahy svého lékaře se sekretářkami a sestrami. Jednou, až budu mít narozeniny, pane doktore, zajedeme ke mně na chalupu (pozn.: u Křemže v jižních Čechách), sedneme si vedle sebe do křesel, zapálíme si doutníky a já vobjednám baletky a ty před náma budou vyhazovat nohama a my budeme koukat a popíjet whisky a pokuřovat ty doutníky. K mé veliké lítosti na to bohužel nikdy nedošlo, deprese vždy vše zavčasu zmařila.
Za léta styku s Milošem Kopeckým jsem postřehl, že větší publicita (například televizní uvedení filmu s ním v hlavní roli) měla paradoxně na jeho zdravotní stav záporný vliv. Jakmile reprízovali dr. Strossmayera, věděl jsem dopředu, že mi bude volat a hlásit, že je zle. A vskutku tomu tak bylo. Dalo se to předvídat. Po uznání nesmírně toužil, ale přišla-li náhle široká publicita, jako by se zastyděl a valem se ubíral do ulity své melancholie. Také ho přiváděly do rozpaků prosby televizních divaček Dietlova seriálu Nemocnice na kraji města, aby jim operoval koleno. Tváří v tvář slabomyslné naivitě byl bezradný jak z kotce vypuštěný králík. Věděl, že ti lidé ho milují jako pánaboha, a to, že jsou takhle hloupí, mu kazilo pocit ze sebe i z toho, co dělá. Nemohl z toho mít radost. Trpěl za paní, která se v Dušní ulici divila: Jak to, že tady vystupujete z auta, když ještě před pěti minutama jste operoval a měl starosti s dr. Cvachem?
/redakčně kráceno - delší text/
Ke stažení
 Článek ve formátu PDF [179,07 kB]
Článek ve formátu PDF [179,07 kB]




















