40 let imunologické tolerance
| 5. 6. 1994Základní charakteristika specifické imunitní odpovědi je, že je namířena pouze proti té cizorodé makromolekule, tzv. antigenu, kterou byla vyvolána. Specifická imunita vyvolaná antigeny mikroorganizmů nebo virů je příčinou toho, že u některých infekčních chorob jedinci, kteří je prodělali, jsou proti nim odolní, imunní. Získání podobné odolnosti mají za účel různá očkování.
Před čtyřiceti lety vstoupil do povědomí imunologů jev, který by bylo možné nazvat imunita naruby – imunologická tolerance. Je to potlačení imunitní odpovědi pouze proti určitému antigenu. Podnětem, který ho vyvolává, je rovněž antigen, který by za „normálních“ podmínek vyvolal imunitní odpověď. K tomu, aby vyvolal imunologickou toleranci, musí být podán buď ve vyšší, nebo v nižší dávce, nežli je ta, která imunitní reakci vyvolává, v pozměněné formě anebo jiným způsobem než obvykle. Jako zvláště vhodný způsob pro navození imunologické tolerance se ukázalo podání antigenu mladým jedincům, u nichž již vznikly lymfoidní orgány, které uskutečňují imunitní odpověď, ale jejich funkční schopnost ještě nedozrála.
Této poslední situace, nedozrálosti lymfoidního systému, bylo využito při experimentálním navození imunologické tolerance, která tomuto jevu dala název. Roku 1953 se v Londýně podařilo P. B. Medawarovi a jeho spolupracovníkům navodit imunologickou toleranci na kožní štěp od antigenně odlišného jedince stejného druhu tím, že příjemci byly během zárodečného vývoje vstříknuty dárcovy buňky. Když příjemce dospěl do stáří, kdy by se už normálně dárcův štěp odhojil, štěp, který na něj byl přenesen, přežíval, byl tolerován, ačkoliv štěpy od jiných jedinců byly tímto příjemcem normálně odhojovány. Medawar a spolupracovníci nazvali tento jev imunologická tolerance. Když se ukázalo, že jde o obecný jev, který lze navodit i na jiné antigeny a také u dospělých zvířat, byl tento název rozšířen i na ně.
Současně s Medawarovou skupinou a nezávisle na ní zjistil Milan Hašek z Biologického ústavu ČSAV v Praze, že kuřata, jejichž krevní oběhy spojil během zárodečného vývoje, nejsou v dospělosti schopna tvořit protilátky proti krvinkám partnera, ačkoliv proti krvinkám jiných slepic je tvoří normálně. Spojení ptačích zárodků, původně jen slepičích, ale později i různých druhů, prováděl technikou embryonální parabiózy uskutečněné srůstem plodových obalů. Využíval při ní toho, že v pokročilejších stadiích vývoje rostou bohatě cévami zásobené plodové obaly pod skořápku, kde proniká do krve kyslík, jehož potřeba u rychle rostoucího zárodku prudce stoupá. Po seznámení s výsledky Medawarovy skupiny zjistil M. Hašek, že mezi slepičími partnery z embryo–nální parabiózy přežívají i jejich kožní štěpy (Vesmír 32, 115, 1953/2; Vesmír 33, 291, 1954/5).
M. Hašek a jím vedený tým studium této problematiky rozvinuli a v Praze vzniklo významné centrum výzkumu. Velmi brzy došlo také k navázání pracovních i přátelských kontaktů s londýnskou skupinou. Podrobněji jsem o objevech obou skupin a o současném stavu této problematiky psal při příležitosti 25. výročí publikace zmíněných objevů (Vesmír 57, 179, 1978/3). Letošní desáté výročí úmrtí Milana Haška (Vesmír 64, 234, 1985/4; Vesmír 69, 288, 1990/5) je příležitostí podívat se na tuto problematiku znovu. Odstup dovoluje zhodnotit přínos zmíněných objevů. Byly učiněny v oblasti imunologie, o kterou se právě medicína začínala zajímat – transplantaci tkání a orgánů. Chirurgie v té době vyřešila nebo byla schopna vyřešit transplantaci řady orgánů, ale většina transplantátů od jiného člověka byla přes prvotní přihojení zničena imunitní reakcí příjemce proti antigenům, v nichž se dárce od něho lišil. Tyto geneticky podmíněné rozdíly jsou i u sourozenců – jak u lidí, tak u jiných živočišných druhů – tak značné, že téměř vždy vedou k odhojení štěpu. O poznání procesů transplantační imunity se ve čtyřicátých letech zasloužil P. B. Medawar. Začal se touto problematikou zabývat za druhé světové války, když britské letectvo zadalo výzkumný úkol, jak umožnit krýt u letců popáleniny kůže štěpy od jiných jedinců, aniž by docházelo k jejich časnému odhojení. Ve čtyřicátých letech se mu tento úkol nepodařilo splnit, ale experimentální navození imunologické tolerance bylo jeho prvním řešením, i když ho nebylo možné využít přímo v praxi.
V začlenění imunologické tolerance do imunologických představ, a hlavně v pochopení jeho významu, sehrál rozhodující úlohu australský virolog a imunolog F. M. Burnet. Povšiml si toho, že při rozdílech v antigenech jedinců téhož druhu, které vznikají náhodnou kombinací genů obou rodičů, není možné, aby neschopnost imunologicky reagovat na vlastní antigeny byla vrozená, ale organizmus ji teprve musí získat. Koncem čtyřicátých let vyslovil hypotézu, že setká-li se vyvíjející se organizmus s antigeny, není sice ještě schopen na ně odpovědět imunitní reakcí, ale toto setkání neprojde bez následků a potlačí imunitní reakci proti těmto antigenům i v době, kdy už organizmus dozraje. Vzhledem k izolaci zárodků od okolí navozují takový útlum za normálních podmínek jen vlastní antigeny. Burnetův pokus o experimentální ověření této hypotézy byl však neúspěšný a teprve Medawarovy a Haškovy výsledky ji potvrdily. V padesátých letech Burnet formulací klonální teorie tvorby protilátek, do níž začlenil i imunologickou toleranci, způsobil v imunologických představách zásadní převrat a měl i významný vliv na rozvoj genetiky živočišné buňky.
 Burnetův podíl na pochopení a ocenění významu imunologické tolerance byl tedy velmi významný a je oprávněné, že mu byla spolu s Medawarem za její objev r. 1960 udělena Nobelova cena. Různé stavy imunologické tolerance byly sice navozeny nebo pozorovány již dříve, ale v žádném z těchto případů to nemělo srovnatelný dopad. Tak již čtvrt století před pokusy Medawara a Haška zjistil vratislavský dermatolog W. Frei (1928), že u pacientů, kteří byli léčeni injekcemi neosalvarsanu do žíly, nelze navodit na tento lék přecitlivělost jeho injekcí do kůže. Mladý americký dermatolog M. B. Sulzberger, který byl ve Vratislavi na studijním pobytu, reprodukoval tento fenomén u morčat (1929). Chtěl v jeho studiu pokračovat i po návratu do New Yorku, ale u místních morčat nemohl jeho kožními injekcemi vyvolat přecitlivělost na neosalvarsan. Později se M.W. Chaseovi podařilo potlačit nebo alespoň snížit přecitlivělost na některé kožní alergeny, jestliže před vyvoláním přecitlivělosti potíráním kůže jim tyto látky vpravil do zažívacího traktu. Zmíněný fenomén byl nazván Sulzbergerův-Chaseův. Jeho plný význam byl doceněn teprve v padesátých letech, když se ukázalo, že jde o jeden z jevů imunologické tolerance.
Burnetův podíl na pochopení a ocenění významu imunologické tolerance byl tedy velmi významný a je oprávněné, že mu byla spolu s Medawarem za její objev r. 1960 udělena Nobelova cena. Různé stavy imunologické tolerance byly sice navozeny nebo pozorovány již dříve, ale v žádném z těchto případů to nemělo srovnatelný dopad. Tak již čtvrt století před pokusy Medawara a Haška zjistil vratislavský dermatolog W. Frei (1928), že u pacientů, kteří byli léčeni injekcemi neosalvarsanu do žíly, nelze navodit na tento lék přecitlivělost jeho injekcí do kůže. Mladý americký dermatolog M. B. Sulzberger, který byl ve Vratislavi na studijním pobytu, reprodukoval tento fenomén u morčat (1929). Chtěl v jeho studiu pokračovat i po návratu do New Yorku, ale u místních morčat nemohl jeho kožními injekcemi vyvolat přecitlivělost na neosalvarsan. Později se M.W. Chaseovi podařilo potlačit nebo alespoň snížit přecitlivělost na některé kožní alergeny, jestliže před vyvoláním přecitlivělosti potíráním kůže jim tyto látky vpravil do zažívacího traktu. Zmíněný fenomén byl nazván Sulzbergerův-Chaseův. Jeho plný význam byl doceněn teprve v padesátých letech, když se ukázalo, že jde o jeden z jevů imunologické tolerance.
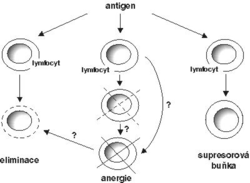
Když jsem r. 1978 psal svůj článek, bylo už známo, že imunologická tolerance není způsobována jedním mechanizmem, jak se to většinou dříve předpokládalo. Bylo dost nálezů, které ukazovaly, že v některých případech se útlum lymfocytů uskutečňuje přímým působením antigenu na ně. V jiných případech však antigen vyvolával aktivaci lymfocytů, které působily tlumivě na lymfocyty, jež by mohly imunitní reakci uskutečnit. Tyto tlumivé lymfocyty byly nazvány supresorové buňky. Otevřena zůstávala otázka, zda přímý útlum lymfocytů antigenem je způsoben jejich smrtí (klonální eliminací nebo delecí), anebo zda je pouze zbavuje funkční schopnosti, ale nechává je přežít. Tuto otázku se podařilo vyřešit v uplynulých deseti letech, kdy bylo možné vnést do organizmu gen pro antigenní receptor a dosáhnout jeho exprese ve značné části lymfocytární populace transgenního jedince. Vzhledem k tomu, že každý lymfocyt má jen receptory jedné specifity a každý buněčný klon má receptor jiné specifity, je za normálních podmínek počet lymfocytů s týmž receptorem jen nepatrným zlomkem celkové populace. Za této situace bylo velmi obtížné rozlišit mezi eliminací klonu a jeho přežitím v utlumeném stavu. U transgenních jedinců však bylo možné získat na tuto otázku odpověď. Ukázalo se, že oba mechanizmy se při imunologické toleranci mohou uplatnit. Zvláště podrobně byla studována klonální eliminace tolerovaným antigenem, která nastává v thymu při zrání T-lymfocytů (kam patří lymfocyty zodpovědné za buněčnou imunitu, lymfocytární cytotoxicitu a za regulaci imunitní odpovědi). Pokud však tolerovaný antigen není přítomen v thymu, lymfocyty mající pro něj receptor mohou při navození tolerance přežít, ale ztrácejí schopnost proti němu reagovat. Tento stav byl nazván anergie. Vytvoření takových jasných situací bylo umožněno tím, že do organizmu byly vneseny geny kódující cizí antigeny spolu s regulačními geny, určujícími, že zavedený antigen bude exprimován jen v určitém orgánu (např. v pankreatu).
Zdá se, že anergie není jen jeden stav, ale větší množství nejspíše stupňovitých útlumů, které snad mohou vyústit v deleci anergické buňky. Zda anergické stadium, třeba krátké, předchází eliminaci lymfocytu antigenem, zůstává rovněž otevřenou otázkou. Anergie i eliminace byly u transgenních zvířat prokázány rovněž u B-lymfocytů (lymfocytů tvořících protilátky).
V oblasti supresorových buněk je v současnosti méně jasno, než se zdálo být před deseti lety. Tehdy byly popisovány v různých experimentálních modelech celé kaskády různých supresorových buněk. Na rozdíl od linií cytotoxických T-buněk (T-lymfocytů schopných usmrtit buňky, jež nesou antigen, pro který mají tyto lymfocyty specifický receptor) a pomocných T-buněk (pomáhajících uskutečňovat imunitní reakci jiným lymfocytům, nebo aktivujících makrofágy) nebyly získány podobné linie supresorových T-buněk, přesněji řečeno existující linie nelze za ně bez jakýchkoliv pochyb pokládat. Fenomény aktivního útlumu zprostředkované T-buňkami nepochybně existují, ale zodpovědné buňky se nepodařilo uspokojivě identifikovat a málo objasněný je i mechanizmus jejich působení.
V současnosti existuje sice řada projektů, které se snaží o praktické uplatnění imunologické tolerance, ale žádný dosud nedospěl do konečné fáze. Zatím je kupř. při klinických transplantacích dále nutné spoléhat na léky, které nespecificky potlačují transplantačně imunitní reakci, ale současně tlumí i obranné reakce proti mikroorganizmům. Medicína však cítí potřebu potlačení nežádoucích imunitních reakcí velmi naléhavě nejen v stoupajícím výskytu alergií, ale i po poznání škodlivého vlivu některých typů imunitních reakcí v řadě infekcí.
MECHANIZMY VZNIKU SPECIFICKÉHO IMUNITNIHO ÚTLUMU
Centrální mechanizmy na úrovni buněk reagujících s antigenem
- delece specifických klonů lymfocytů
- anergie lymfocytů
- blokáda receptorů lymfocytů antigenem (imobilizace, zmrazení receptorů)
- klonální aborce apoptotická diferenciace
- exhaustivní diferenciace (vznik funkční buňky bez proliferace)
- defekty v reexpresi receptoru (down-regulation)
- defekt kaskády přenosu antigenního signálu
Periferní mechanizmy
- zpětně vazebný útlum protilátkou
- protilátky proti epitonům antigenů
- anti-idiotypové protilátky
- útlumové buňky a sekretované supresorové faktory
- fenomén marné práce (tred-mill)















