Nanopórové sekvenování genetické informace
| 3. 3. 2026Možnost číst genetickou informaci patří k velkým úspěchům moderní biologie. Technologie, která to zvládá rychle a třeba i přímo v terénu, využívá miniaturní póry, jimiž čtené řetězce DNA nebo RNA procházejí z jedné strany membrány na druhou.
Největší rozmach metod sekvenování DNA přišel na konci 20. století s projektem lidského genomu, jehož ambicí bylo přečíst kompletní lidskou DNA – tedy každou z přibližně tří miliard bází DNA.
Od té doby se sekvenování DNA a také RNA stalo jedním ze základních nástrojů biologického a lékařského výzkumu. Pomáhá nám rekonstruovat evoluční historii organismů, diagnostikovat dědičná onemocnění a sledovat šíření virů i jejich mutací. Uplatnění nachází také v kriminalistice, vývoji vakcín a objevování dosud neznámých druhů organismů.
V posledních letech se do tohoto rychle se rozvíjejícího oboru výrazně zapsalo nanopórové sekvenování, které patří mezi sekvenační metody třetí generace (viz rámeček). Jeho hlavní předností je délka tzv. čtení: zatímco předchozí metody sekvenace dokážou přečíst úseky DNA dlouhé desítky až stovky písmen, nanopórové technologie zvládají číst najednou desetitisíce až statisíce bází. Díky tomu čteme dlouhé, nepřerušené úseky DNA, které lze snadno a jednoznačně zařadit do genomu. Už z malého množství dat tak často získáme přehled o celé genetické informaci organismu.
„Genetická informace se čte v reálném čase, je dostupná okamžitě a lze na ni průběžně reagovat. Sekvenování se tak přibližuje spíše měření než analýze.“
Dalšími výhodami jsou rychlost, relativně nízké náklady a také přenosnost zařízení. Zatímco dřívější sekvenátory zabíraly celý laboratorní stůl (nebo připomínaly spíše lednici), nanopórový sekvenátor se dnes vejde do kapsy a velikostí se blíží mobilnímu telefonu. Za tyto výhody se však platí vyšší chybovostí, která klade zvýšené nároky na zpracování a interpretaci dat.
Právě kombinace jednoduchosti a flexibility umožnila nasazení nanopórového sekvenování v prostředích, kde by to ještě nedávno znělo jako science fiction. Používá se například na Mezinárodní vesmírné stanici (ISS),1) přímo na operačním sále při diagnostice mozkových nádorů,2) během epidemií (včetně pandemie covidu-19) nebo při výzkumu mikroorganismů na polárních expedicích.3)
Sekvenování dlouhých čtení dnes hraje důležitou roli i ve velkých genomických iniciativách, jako je evropský projekt 1+ Million Genomes, jehož cílem je rozvoj personalizované medicíny, nebo UK Biobank, dosud největší genomický projekt s více než půl milionem účastníků, který zásadně přispívá k výzkumu stárnutí, nemocí a jejich prevence.
Čtení DNA skrz otvor
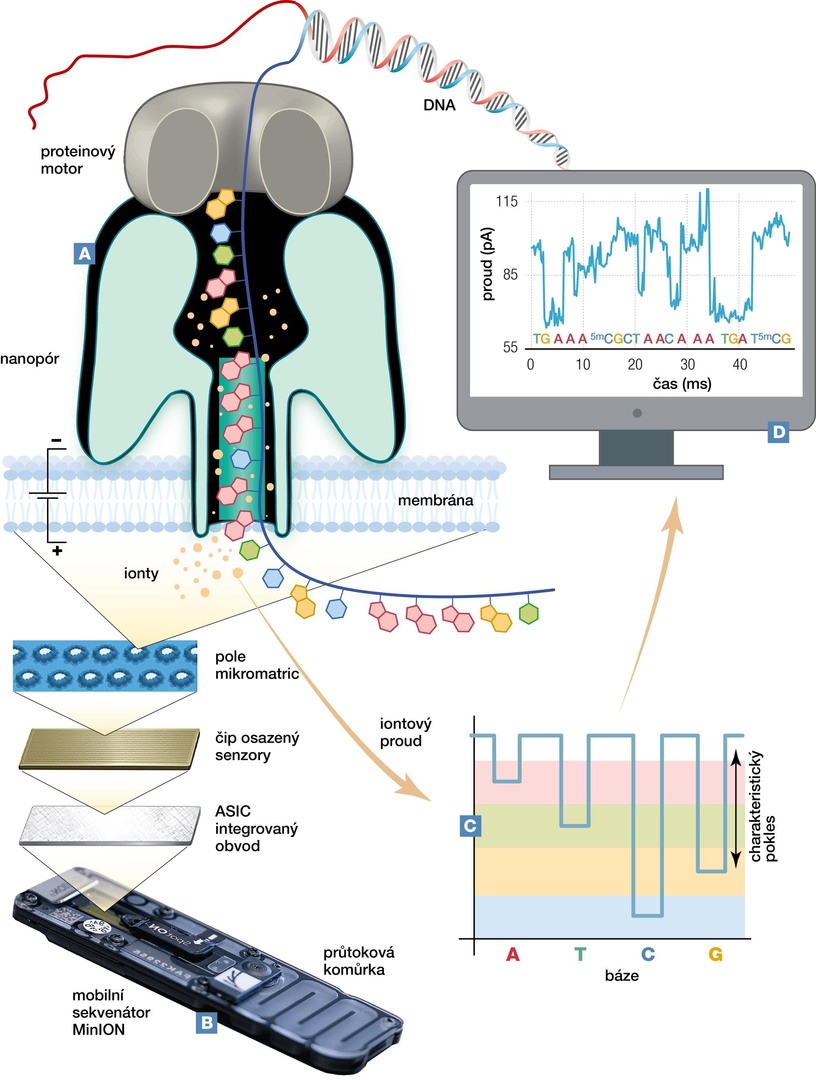
Základním stavebním prvkem nanopórového sekvenování je proteinový pór velký jen několik nanometrů, zasazený do umělé lipidové membrány, která odděluje dvě prostředí s jiným elektrickým potenciálem. Jeho princip vychází z chování iontových kanálů: pokud skrz úzký otvor procházejí ionty, lze měřit elektrický proud. Jakmile se v kanálu objeví překážka, například molekula procházející pórem, proud se částečně omezí. Po jejím odstranění se opět vrátí na původní hodnotu. Takto pór funguje jako velmi citlivý biosenzor.
Nanopórové sekvenování využívá přesně tento jev. Skrz nanopór je postupně protahován jeden řetězec DNA nebo RNA. Jednotlivé stavební kameny nukleových kyselin (báze) se liší velikostí i tvarem, a proto každá z nich pór „ucpává“ trochu jiným způsobem. Výsledkem je charakteristická změna iontového proudu, kterou měříme v čase (obr. 1). Z průběhu těchto drobných poklesů a návratů pak pomocí výpočetních algoritmů rekonstruujeme původní pořadí bází, tedy genetickou informaci.
Důležité je, co se zde nemusí dělat. Na rozdíl od většiny starších metod není nanopórové sekvenování založené na syntéze komplementárního vlákna k templátu a není ani nutné DNA předem namnožit pomocí polymerázové řetězové reakce (PCR), která je častým zdrojem systematických chyb. DNA se také nemusí syntetizovat ani fluorescenčně značit. Čteme jednotlivé molekuly tak, jak skutečně v buňce existují, a to v úsecích často dlouhých desítky až stovky tisíc bází.
Další zásadní vlastností je práce s daty v reálném čase. Sekvenátor zapisuje signál průběžně, takže k datům máme přístup okamžitě a sekvenaci lze kdykoliv ukončit. To otevírá dveře zcela novým přístupům. Pokud nás například nezajímá celý genom, ale jen konkrétní gen nebo oblast DNA, můžeme využít tzv. adaptivní vzorkování. Sekvenátor se nejprve „podívá“ na krátký začátek každé čtené molekuly DNA, rychle jej porovná s referenční DNA a rozhodne se, zda má smysl pokračovat. Pokud ano, v čtení pokračuje; pokud ne, molekula je z nanopóru vysunuta a zařízení se věnuje jinému úseku. Tímto způsobem lze cíleně vybírat jen oblasti zájmu bez složité a časově náročné laboratorní přípravy.
Výsledkem je technologie, která v sobě spojuje fyzikálně jednoduchý princip s překvapivou flexibilitou. Právě tato kombinace stojí za tím, že nanopórové sekvenování, vyvíjené firmou Oxford Nanopore Technologies, našlo uplatnění jak v základním výzkumu, tak v klinické praxi a v terénních podmínkách.