Velký význam malých RNA
| 1. 11. 2012„Co když nejde o antisense ale o dsRNA?“ Tahle myšlenka stála na počátku cesty k revolučnímu objevu RNA interference (RNAi, čtěte árenejáj) [viz také Vesmír 86, 110, 2007/2]. Podle Craiga Mello, jednoho z objevitelů RNAi, se tak stalo na konferenci ve Wisconsinu v roce 1997. Podle legendy, kterou jsem několikrát zaslechl, to bylo v baru. Není to úplně nepravděpodobné. Po mnoha vyčerpávajících hodinách přednášek zahlcujících mysl množstvím nových dat potřebuje mozek nové informace roztřídit a dát je do správných souvislostí. Posezení s kolegy v baru je k tomu vítanou příležitostí. Nikoliv vzácně se stává, že se v tu chvíli objeví nová myšlenka nebo nové řešení starého problému. Avšak vzhledem k tomu, že barový moment osvícení nelze ověřit z žádného zdroje, jde nejspíš jen o legendu.
 V roce 1998 způsobil článek Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans v časopise Nature [1] revoluci v manipulaci s geny u červa Caenorhabditis elegans, který léta slouží biologům jako jednoduchý studijní model mnohobuněčného organismu. A nezůstalo u červa. Tento článek spustil lavinu studií, které během několika let objevily obrovský svět malých RNA, jenž léta unikal naší pozornosti, přestože fragmenty tohoto světa jsme nacházeli již dříve. Následující text představuje jen miniaturní okénko do světa malých RNA. Pro představu: letos jsme do knihy o regulačních RNA přispěli kapitolou o fungování přirozené RNAi u živočichů [2], která citovala 259 prací a měla přes 120 000 úhozů, tj. zhruba desetinásobný rozsah než tento článek.
V roce 1998 způsobil článek Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans v časopise Nature [1] revoluci v manipulaci s geny u červa Caenorhabditis elegans, který léta slouží biologům jako jednoduchý studijní model mnohobuněčného organismu. A nezůstalo u červa. Tento článek spustil lavinu studií, které během několika let objevily obrovský svět malých RNA, jenž léta unikal naší pozornosti, přestože fragmenty tohoto světa jsme nacházeli již dříve. Následující text představuje jen miniaturní okénko do světa malých RNA. Pro představu: letos jsme do knihy o regulačních RNA přispěli kapitolou o fungování přirozené RNAi u živočichů [2], která citovala 259 prací a měla přes 120 000 úhozů, tj. zhruba desetinásobný rozsah než tento článek.
RNA interference (RNAi)
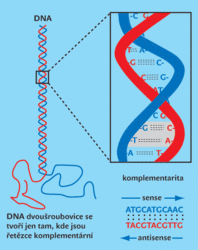
Co vlastně Andy Fire a Craig Mello objevili a v čem je RNAi tak revoluční? RNAi je elegantně jednoduchý přirozený mechanismus, který je možné využít pro zablokování jakéhokoliv genu. Pro vědce je objev téhle technologie srovnatelný se získáním autorizace ke všem účtům v bance. V dobách, kdy se z pionýrů stávali skauti a ze svazáků vrcholní manažeři, vědce trápilo, jak spolehlivě umlčet vybraný gen (DNA a gen – viz obr. 1 a obr. 2). V osmdesátých a devadesátých letech se za tímto účelem rozvíjela technologie tzv. antisense RNA. Jejím principem bylo vytvořit RNA molekulu (antisense RNA), která by se navázala na mRNA. Tím by se mRNA zablokovala a gen by byl umlčen.
Antisense RNA metoda byla problematická, protože někdy fungovala, někdy ne. V devadesátých letech si několik laboratoří pracujících s Caenorhabditis elegans povšimlo různých neočekávaných výsledků v antisense RNA experimentech, které naznačovaly, že existuje nějaký typ RNA molekuly, který blokuje vybraný gen mnohem účinněji než antisense RNA. A v roce 1998 Andy Fire a Craig Mello ukázali, že molekulou, která tak skvěle spouští umlčení, je dvouvláknová RNA (dále jen dsRNA, obr. 3).
 V té době působil jejich výsledek jako zjevení. U myšího modelu v té době vyžadovalo zablokování vybraného genu pracnou manipulaci s genomovou DNA obnášející v lepším případě rok až dva práce a zhruba 25 000 dolarů. A najednou Andy Fire a Craig Mello ukázali, že u Caenorhabditis elegans stačí pro vypnutí libovolného genu vzít jeho mRNA, doplnit ji párujícím se vláknem a dopravit výslednou dsRNA injekcí kamkoliv do těla Caenorhabditis elegans. A cena? Prakticky pár desítek dolarů na jeden gen.
V té době působil jejich výsledek jako zjevení. U myšího modelu v té době vyžadovalo zablokování vybraného genu pracnou manipulaci s genomovou DNA obnášející v lepším případě rok až dva práce a zhruba 25 000 dolarů. A najednou Andy Fire a Craig Mello ukázali, že u Caenorhabditis elegans stačí pro vypnutí libovolného genu vzít jeho mRNA, doplnit ji párujícím se vláknem a dopravit výslednou dsRNA injekcí kamkoliv do těla Caenorhabditis elegans. A cena? Prakticky pár desítek dolarů na jeden gen.
Vzhledem k potenciálu RNAi začalo mnoho laboratoří okamžitě testovat, co dělá dsRNA v jejich modelovém systému. A seznam organismů, kde dsRNA funguje jako specifický blokátor genů, začal utěšeně růst. V tomto okamžiku začalo být také zřejmé, že mechanismy podobné RNAi se nacházejí u všech mnohobuněčných organismů a že úkazy dříve popsané u rostlin a hub jsou důsledkem velmi podobného molekulárního mechanismu.
Když v roce 2006 obdrželi Andy Fire a Craig Mello Nobelovu cenu za fyziologii a medicínu, bylo některým kolegům pracujícím na rostlinných modelech trochu líto, že se nedostalo i na ně, neboť úplně první fenomén příbuzný RNAi (tzv. co-suppression) byl popsán již v roce 1990 na petúniích.
Osobně jsem se k RNAi poprvé dostal během doktorských studií na jaře 1999 – v době, kdy RNAi byla známá u červů Caenorhabditis elegans a u mušek Drosophila melanogaster, ale její existence u savců se neočekávala, protože už čtvrt století byly známé silně toxické účinky dsRNA na savčí buňky. Spekulace jsou jedna věc a experimentální ověření druhá. Proto jsem během mého semestrálního projektu zkoušel vyvolat RNAi efekt v myším vajíčku. A fungovalo to! Nutno říci, že první RNAi experimenty (kromě nás na nich pracovala i laboratoř Magdaleny Zernicka-Goetz v Cambridge) si vybraly velkou dávku začátečnického štěstí, protože se po letech ukázalo, že u savců klasická RNAi (vyvolaná dlouhou dsRNA) dobře funguje právě jen ve vajíčku. V roce 2001 pak laboratoř Toma Tuschla ukázala, že pro vyvolání RNAi v savčích buňkách stačí krátká dvouvláknová RNA molekula (siRNA = short interfering RNA, viz obr. 4), která není toxická. Tím odstartoval revoluci ve studiu savčích genů a ve vývoji možných terapeutických strategií, které snad v budoucnu umožní cíleně blokovat vybrané geny, kdykoliv to bude potřeba – například virové geny v infikovaných buňkách.
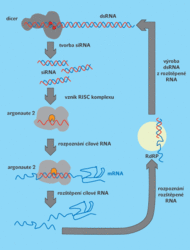
Mechanismus RNAi ( obr. 4) byl rozluštěn relativně rychle. Klíčovým poznatkem bylo, že blokující efekt zajišťují malé RNA molekuly nasekané z původní dsRNA, které vyhledávají v buňce komplementární mRNA molekuly podobně, jako Google vyhledá všechny dokumenty obsahující identický kus textu. Malá RNA obsahuje obvykle 20 až 25 nukleotidů (písmen DNA abecedy), což je pro rozpoznání mRNA molekul jednoho genu dostatečné. A v tom právě spočívá kouzlo RNAi. K umělému zablokování genu dnes stačí vybrat v jeho mRNA malý úsek, vytvořit z něj malou RNA a dodat ji do buňky.
 Jádro mechanismu bylo rozluštěno již v roce 2001. Poslední díl skládačky (jaký mechanismus likviduje cílovou RNA) byl vyřešen v roce 2004. Neznamená to, že bychom znali vše, protože příroda je plná překvapení a variací nejen na téma mechanismu RNA interference. Dnes existuje celá zoologická zahrada malých RNA a příbuzných mechanismů. Je až s podivem, že jsme si existenci tohoto světa malých RNA nedokázali uvědomit dříve.
Jádro mechanismu bylo rozluštěno již v roce 2001. Poslední díl skládačky (jaký mechanismus likviduje cílovou RNA) byl vyřešen v roce 2004. Neznamená to, že bychom znali vše, protože příroda je plná překvapení a variací nejen na téma mechanismu RNA interference. Dnes existuje celá zoologická zahrada malých RNA a příbuzných mechanismů. Je až s podivem, že jsme si existenci tohoto světa malých RNA nedokázali uvědomit dříve.
Hlavní důvod byl technický – tyto RNA jsou tak malé, že při běžné analýze uniknou pozornosti. Obdiv si proto zaslouží kolegové, kteří byli první, koho napadlo během devadesátých let zaměřit pozornost na malé RNA. Například Victor Ambros, jehož laboratoř objevila v roce 1993 první mikroRNA, jež byla ve své době považována za zvláštní hříčku přírody. Po roce 2000 se pak ukázalo, že takových mikroRNA jsou tisíce, že jsou blízké příbuzné malých RNA v RNAi procesu a mají je všichni živočichové a rostliny. Ale o mikroRNA, piRNA, rasiRNA, 2° siRNA, 21U RNA, tasiRNA a dalších zvířátkách ze zoologické zahrady malých RNA až někdy jindy.
Výzkum malých RNA v Ústavu molekulární genetiky AV ČR
Laboratoř epigenetických regulací v ÚMG pokračuje ve studiu RNAi v modelu myšího vajíčka. Tato pohlavní buňka se liší od tělních buněk v tom, že RNAi je v ní velmi aktivní a získala nové funkce. Studujeme proto molekulární mechanismus, který je za tuto situaci zodpovědný. V loňském roce jsme objevili, že ve vajíčku je velmi aktivní Dicer protein, který produkuje vysoké množství siRNA z dsRNA (viz obr. 4), čímž zvyšuje aktivitu RNAi. Nyní zjišťujeme, proč tomu tak je právě ve vajíčku.
 Možná se ptáte, k čemu to je dobré? Proč utrácet miliony korun za studium titěrných RNA v myším vajíčku? Může to mít vůbec nějaký širší význam? Moje odpověď je, že jednoznačně ano, a mám pro tuto odpověď dva důvody.
Možná se ptáte, k čemu to je dobré? Proč utrácet miliony korun za studium titěrných RNA v myším vajíčku? Může to mít vůbec nějaký širší význam? Moje odpověď je, že jednoznačně ano, a mám pro tuto odpověď dva důvody.
Prvním důvodem jsou doložitelné úspěchy studia obranných biologických mechanismů, které zcela zásadně změnily medicínu a biotechnologie. Jedním takovým mechanismem jsou protilátky. Význam studia protilátek pro prevenci a léčbu nejrůznějších onemocnění je zbytečné zdůrazňovat. Co veřejnost možná neví, je, že protilátky jsou také hlavním nástrojem pro zobrazování a izolaci konkrétních proteinů a stojí na nich prakticky celý současný biomedicínský výzkum.
Jiným typem obranného mechanismu, jehož studium nenápadně a zásadně změnilo svět, jsou restrikční endonukleázy, které se v laboratořích používají k cílenému přestřižení DNA molekul. RNAi je také příkladem obranného mechanismu, jehož studium způsobilo revoluci v tom, jak dokážeme manipulovat s geny. V laboratořích je dnes RNAi rutinní metoda pro studium genů, která urychlila studium jejich funkcí o možná i desítky let. Mimochodem, jak bylo zmíněno výše, myší vajíčka byla první savčí model, na kterém bylo ukázáno, že RNAi je v savčích buňkách přítomná a experimentálně využitelná. Takže tento výzkum smysl měl a jsem si jistý, že má a dost dlouho ještě mít bude.
Do budoucnosti také směřuje můj druhý důvod. Když pochopíme, jak vajíčko posiluje RNAi, budeme moci dosáhnout podobného efektu v jiných buňkách. K čemu by mohlo být dobré využít přirozené posílení aktivity enzymu Dicer? Například při hledání nových způsobů terapie makulární degenerace. To je degenerativní choroba oka, kterou trpí obvykle staří lidé a kvůli které přicházejí o zrak. Nedávný výzkum ukázal, že nízká aktivita enzymu Dicer může přispívat k makulární degeneraci, protože se v buňce hromadí nerozštěpená dsRNA [3]. Pokud pochopíme, jak štěpení dsRNA funguje v myších a jiných savčích vajíčkách, možná v budoucnu najdeme způsob, jak jej posílit v oku pacienta. Nedokážu předpovědět, jestli toho nakonec dosáhneme. Mohu ale čtenáře ujistit, že i když provádíme základní výzkum jednoho procesu na speciálním buněčném typu, nespouštíme ze zřetele, jak by se naše výsledky daly uplatnit v biotechnologiích a medicíně.
Literatura
[1] Fire A. et al.: Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans. Nature 391, 806–811, 1998.
[2] Nejepinska J., Flemr M., Svoboda P.: The Canonical RNA Interference Pathway in Animals. In: Mallick B., Ghosh Z. (eds.): Regulatory RNAs. Springer, Berlin – Heidelberg 2012, s. 111–149.
[3] Kaneko H. et al.: DICER1 deficit induces Alu RNA toxicity in age-related macular degeneration. Nature 471, 325–330, 2011.
[4] Carver R., Waldahl R., Breivik J.: Frame that gene. A tool for analysing and classifying the communication of genetics to the public. EMBO Rep 9, 943– 947, 2008.
Poznámky
1) Vladimír Vondrejs: Co je to gen?, Vesmír 90, 685, 2011/12; 91, 77, 2012/2; 91, 238, 2012/4; 91, 359, 2012/6; 91, 600, 2012/10; 91, 673, 2012/11.
SLOVNÍČEK
Dicer – RNáza III, enzym štěpící dvouvláknovou RNA na kratší úseky
Drosha – RNáza, enzym upravující prekurzorovou miRNA na aktivní formu
dsRNA – dvouvláknová RNA (ds, double-stranded)
mRNA – mediátorová neboli messenger RNA přenáší informaci z DNA na proteiny
miRNA – mikroRNA, malé molekuly RNA, které nenesou informaci o pořadí aminokyselin v proteinu, ale slouží buňce k regulaci exprese jiných genů
palindrom, palindromová sekvence – vlákno RNA nebo DNA symetrické v pořadí párujících nukleotidů. Např. úsek RNA s nukleotidy AGAAUA/UAUUCU je palindromem, který se v ose symetrie (lomítko) „přeloží“ a vznikne tak molekula dsRNA, tvořená za sebou následujícími páry bází: A–U, G–C, A–U, A–U, U–A, A–U. Pokud je palindrom přerušen úsekem nepárujících nukleotidů, vznikne dvouvláknová molekula se smyčkou na konci, tzv. vlásenková RNA (shRNA).
RNAi – interference RNA
shRNA – krátká vlásenková RNA (sh, short hairpin), viz palindrom
siRNA – malá interferující RNA (si, small interfering)



















