Dendritická buňka v imunitě
Jakým způsobem je zajištěno, že organizmus rozpozná přítomnost patogenu a zneškodní jej, aniž při tom poškodí vlastní tkáň? Když je organizmus napaden patogenem, musí nejdříve rozhodnout, zda má vůbec aktivovat imunitní reakci, a poté musí zvolit takovou imunitní odpověď, aby byla účinná právě proti mikrobu, který jej ohrožuje. K tomu, aby mohl tento úkol splnit, má imunitní systém obratlovců k dispozici jednak přirozenou nespecifickou obranu (tu zajišťují především leukocyty, makrofágy a dendritické buňky), jednak obranu antigenně specifickou (díky ní se tvoří různé typy T-lymfocytů a protilátky produkované B-lymfocyty). Na likvidaci patogenů se podílejí oba mechanizmy, přičemž specifické složky jsou odpovědné za vznik imunitní paměti.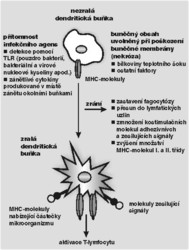
K aktivaci specifické imunity je potřeba, aby části patogenu byly předloženy buňkami prezentujícími antigen v lymfatických uzlinách a aby se dostatečně namnožily efektorové buňky (podrobněji viz Vesmír 78, 565, 1999/10). Účinná specifická imunitní odpověď se rozvíjí zpravidla 4–7 dní po průniku patogenu do organizmu. Buňky prezentující antigen jsou tedy spojujícím článkem mezi antigenně nespecifickou a antigenně specifickou částí imunitního systému a – jak ukazují výsledky výzkumu z posledních let – jejich důležitým zástupcem jsou dendritické buňky (viz též Vesmír 81, 131, 2002/3). Také již byla objasněna řada mechanizmů, jež buňkám umožní rozeznat přítomnost mikrobu či jiného nebezpečí a zajistí, že je zmíněná informace přenesena do lymfatických uzlin, kde jsou v důsledku toho stimulovány specifické Tlymfocyty. Ty pak proti infekci bojují.
Dendritické buňky na čekané a v akci
O existenci dendritických buněk se vědělo od počátku sedmdesátých let 20. století, ale tenkrát bylo obtížné izolovat je z krve či tkání, v nichž tvoří pouze zlomek buněčné populace. Studium dendritických buněk umožnila až laboratorní příprava velkého množství dendritických buněk z krevních monocytů nebo z kmenových buněk kostní dřeně. Metoda byla popsána r. 1994.
V organizmu se dendritické buňky vyskytují jednak zralé, jednak nezralé. Ty nezralé si lze představit jako senzory, jejichž úkolem je rozpoznat infekci v organizmu. Proto jsou strategicky rozmístěny v tkáních, které jsou na rozhraní organizmu a okolního prostředí. Nejvíc jich je v kůži a ve sliznicích dýchacího a zažívacího traktu, kde tvoří 1–2 % celkového počtu buněk. Ostatní dendritické buňky hlídkují téměř ve všech orgánech a mnoho jich nepřetržitě cestuje mezi krví a lymfou.
- Nezralá dendritická buňka (obr. 1 nahoře a obr. 2) požírá téměř všechno, co se vyskytne v jejím okolí: Dokud v organizmu není žádná infekce, pohlcuje především odumřelé buňky zdravých tkání či jejich části a molekuly rozpuštěné v mezibuněčné tekutině. Během své pouti mezi tkáněmi a lymfatickými uzlinami pak pohlcené molekuly zpracuje, vystaví je na svém povrchu a zpřístupní specifickým T-lymfocytům. Specialitou nezralých dendritických buněk však není stimulace T-lymfocytů, k tomu totiž nejsou dostatečně vybaveny. Jestliže je na povrchu nezralé dendritické buňky rozpoznán antigen, T-lymfocyty jsou tím spíš tlumeny, nebo se z nich dokonce vytvoří regulační T-lymfocyty, které imunitní reakci vůči danému antigenu potlačí (viz Vesmír 80, 667, 2001/12). Neschopnost nezralých dendritických buněk vyvolat imunitní odpověď je životně důležitá – vděčíme jí za to, že náš imunitní systém toleruje své vlastní buňky. Vznik imunitní reakce namířené proti vlastním tkáním mívá vážné důsledky – autoimunitní onemocnění. 1)
Jiná situace nastane, jestliže nezralá dendritická buňka pohltí něco, co představuje pro organizmus nebezpečí. Receptory na jejím povrchu dovedou rozpoznat molekulární struktury spojené s patogeny. V průběhu evoluce se tyto struktury příliš neměnily, a proto se nijak výrazně neliší ani receptory pro jejich detekci (jsou dost podobné u všech druhů). Nedávno byla např. objevena skupina Toll-like receptorů (TLR), které mají strukturu velmi podobnou bílkovině s analogickou funkcí u mušky octomilky (oblíbeného genetického modelu). Různí zástupci těchto receptorů, roztroušení na povrchu i uvnitř dendritických buněk, umějí rozpoznat přítomnost virových i bakteriálních nukleových kyselin, specifických součástí bakteriálních stěn a bakteriálních bičíků. Jakmile receptory rozpoznají přítomnost patogenu, začne dendritická buňka zrát. Během zrání je „přeprogramována“.
- Zralá dendritická buňka (obr. 2 a obr. 3) je nejúčinnější buňkou prezentující antigen. Dokáže aktivovat naivní („panenské“) T-lymfocyty, tj. takové, které se dosud nesetkaly s antigenem; za to si vysloužila přívlastek „profesionální“. Jakmile je dendritická buňka aktivována, přestane se „krmit“. To, co pozřela předtím, rozštěpí a vzorky příslušných komplexů proteinů vystaví na svém povrchu. Komplexy obsahující molekuly MHC I. třídy umožňují aktivaci zabíječských Tc-lymfocytů, komplexy obsahující MHC II. třídy aktivují pomocné Th-lymfocyty (podrobněji viz Vesmír 78, 565, 1999/10). Na povrchu dendritické buňky se objeví množství molekul adhezivních (umožňují pevný kontakt mezi buňkou prezentující antigen a lymfocyty), a především molekul, které zesilují signály zprostředkované dendritickou buňkou a zahajují růst různých druhů T-lymfocytů specifických proti jednotlivým původcům infekce. V průběhu těchto změn se množství zralých dendritických buněk přesouvá do lymfatických uzlin, kde čekají na setkání s lymfocyty specifickými pro vystavené antigeny. Kromě toho, že přítomnost infekce vyvolá zmíněné změny, předává každý typ mikroorganizmu (viry, různé druhy bakterií) dendritické buňce důležitou informaci. Podle toho dendritická buňka vyladí výslednou imunitní reakci. Imunitní reakce musí být mikrobu pronikajícímu do organizmu „ušita na míru“. Jak přesně je tato informace kódována a předávána, není dosud jasné. Je však pravděpodobné, že informaci dendritická buňka obdrží velmi brzo po styku s patogenem, a sdělení potom již nemůže být „odvoláno“.
Buňky, které zahynuly neobvyklou smrtí
Přímé rozpoznání mikroorganizmu není jediným způsobem, jímž dendritická buňka zaznamená ohrožení. Aktivována může být i nepřímo, působením prozánětlivých cytokinů, jež jsou produkovány okolními buňkami (podrobněji viz Vesmír 71, 509, 1992/9), např. makrofágy a leukocyty. Proces zrání dendritické buňky ale nemusí být aktivován infekcí, mohou jej vyvolat také vlastní buňky organizmu, které zahynou „neobvyklou“ smrtí. Za normálních okolností při obnovování tkání hynou buňky apoptózou (programovanou buněčnou smrtí), při které není narušena buněčná membrána. Jestliže ale buňka skončí nekrózou (např. při mechanickém poškození), její obsah se rozloží. Některé studie již prokázaly, že dendritické buňky byly aktivovány právě tímto způsobem, přičemž odpovědné za to mohly být proteiny teplotního šoku (viz Vesmír 78, 372, 1999/7). Nelze vyloučit, že by se touto aktivací dendritických buněk dala vědecky podložit (eventuální) účinnost léčby „devitalizací“ (viz Vesmír 80, 606, 2001/11).
Jestliže ale buňka skončí nekrózou (např. při mechanickém poškození), její obsah se rozloží. Některé studie již prokázaly, že dendritické buňky byly aktivovány právě tímto způsobem, přičemž odpovědné za to mohly být proteiny teplotního šoku (viz Vesmír 78, 372, 1999/7). Nelze vyloučit, že by se touto aktivací dendritických buněk dala vědecky podložit (eventuální) účinnost léčby „devitalizací“ (viz Vesmír 80, 606, 2001/11).
Osud dendritické buňky naplněn
V momentě, kdy je nastartován proces zrání, jsou dny dendritické buňky sečteny. Během 48 hodin dozraje, a poté má už jen dva až tři dny na to, aby aktivovala co největší množství pomocných, cytotoxických a paměťových T-lymfocytů. Přestože dendritické buňky končívají tak bídně, je jich v organizmu konstantní množství. Z kmenových buněk v kostní dřeni (a zřejmě také z krevních monocytů) totiž vznikají další.Z uvedených poznatků vyplývá, že dendritické buňky jsou spojujícím článkem mezi nespecifickou a specifickou imunitou. Díky objevení nezralého a zralého stadia jejich životního cyklu již lze vysvětlit některé způsoby, jimiž imunitní systém dokáže rozlišit vlastní proteiny od cizích a rozhodnout o zahájení imunitní odpovědi namířené proti nežádoucí struktuře. 2)
Poznámky
Ke stažení
 Článek ve formátu PDF [1023,72 kB]
Článek ve formátu PDF [1023,72 kB]



















