Jen počkej, leukemie!
| 1. 12. 2025Řidičů tramvaje nebo popelářů jsou plné mateřské školky. Čas tuhle ranou romantiku setře, díky čemuž občas patentový úřad zaznamená nový vynález nebo lidstvo obohatí své poznání o dosud neznámou zákonitost přírody. Raritní je potkat někoho, kdo, stejně jako hlavní hrdina filmu Vrchní prchni, vždycky chtěl být tím, co vystudoval, a pak se tím i živil. V tomto smyslu Vítězslav Bryja takovou raritou je – už v mateřské školce toužil být biologem. Nevěříte? Zeptejte se jeho maminky.
Jít si od věku pěti let za svým, to předpokládá nějaké silné impulsy. — Pocházím z vesnice, takže jako dítko nehlídané, trávící většinu času v přírodě, jsem chytal pulce, nosil je domů a choval žáby. Na rodiče to valný dojem neudělalo, zejména na maminku ne. Pak mě zlákali motýli, lisoval jsem rostliny pro herbář, dalekohledem sledoval ptáky a někdy na konci základní školy mi táta sehnal mikroskop a já propadl pavoukům. Časem mi rodiče vysvětlili, že pro terénní zoology moc práce není a že existují i jiné biologické obory, což mě nasměrovalo k molekulární biologii a genetice.
Po studiích jste se rozhodl vycestovat za vědou do Švédska. Co vás tam táhlo? — S doktorátem v kapse jsem toužil někde nabrat zkušenosti v místě, které bude ambiciózní z hlediska vědy, a zároveň – protože už jsme měli dvě malé děti – přívětivé k lidem s rodinou. Tato dvě kritéria pro mě splňoval Ústav lékařské biochemie a biofyziky Karolínského ústavu ve Stockholmu. Mám dojem, že to byla zdařilá volba, protože děti i manželka na tamní období vzpomínají v dobrém.
Co jste si odsud přinesl vy? — Přetrvaly asi dvě věci. První je změna náhledu. Do Švédska jsem odjížděl s přístupem: děláme, co se dá, s tím, nač zrovna máme prostředky. Když se na to dívám zpětně, asi šlo o otisk období komunismu, v němž nebylo tolik možností. Jenomže ve Stockholmu jsem se potkal s docela odlišným přístupem: řešíme problém, který je nejdůležitější, a i když to neumíme, naučíme se to, a když na to nemáme zdroje, nějak je seženeme, najdeme spolupracovníky, abychom uspěli.
Praktikovat něco takové chce sebevědomí a odvahu. — Ono to ani jinak nejde v prostředí, kde vás obklopují nositelé jmen, která znáte ze stránek těch nejlepších vědeckých časopisů, jako je Cell nebo Nature. Najednou na chodbě potkáváte lidi, kteří dosáhli úspěchu, o němž se nám tehdy jenom zdálo, a zjišťujete, že jsou docela normální. Každý druhý profesor zasedá v Nobelově shromáždění Karolinského institutu, kde vybírá nositele Nobelových cen za fyziologii a medicínu. V takovém prostředí jsem získal přesvědčení, že i v Česku může jít všechno.
A ta druhá věc, kterou jste si ze Švédska přinesl? — Téma výzkumu, jímž je mezibuněčná kaskáda známá jako signalizace Wnt (podle anglického názvu genu wingless, viz Vesmír 101, 82, 2022/2). Ve Stockholmu jsem ji přijal jako svůj boční projekt a zůstal u ní dodnes.
Jazyk buněk
Čím vás toto téma tak zaujalo? — Když jsem ve Švédsku končil, nebylo jasné, jak tato signální dráha funguje. Její pochopení je přitom mimořádně důležité, protože jde o jakýsi mezibuněčný jazyk, jehož prostřednictvím buňky v mnohobuněčném organismu, jako je ten lidský, dokážou fungovat ku prospěchu celku. A my zatím byli v situaci, že jsme pozorovali nějakou událost na buněčné membráně, a pak jako by se stal „zázrak“ a buňka tuto událost přenesla do svého nitra a my netušili jak.
Říkáte-li, že jde o mezibuněčný jazyk, dal by se přirovnat k tělnímu rozhlasovému vysílání, nebo jde o něco méně centralizovaného? — V tomto příměru by rozhlasové vysílání byly hormony – vstupují do krve a komunikují se všemi buňkami, jež mají ten správný přijímač. Signalizace Wnt je lokálnější a dala by se přirovnat ke komunikaci na pracovišti nebo v rodině, kde nastavuje pravidla a role jednotlivých aktérů, v tomto případě buněk. Pracuje s tím, že jednotlivé buněčné typy mají nějakou hierarchii v rámci tkáně, což umožňuje její obnovu a vývoj. Kalibrace lokálních podmínek a nastavení jejich spolupráce s vnějšími zdroji umožňuje, aby lokální jednotka fungovala ku prospěchu celku. Přeneseně: stejně jako Masarykova univerzita, kde teď sedíme, má nastavená vnitřní pravidla, aby fungovala ku prospěchu České republiky a všech jejích občanů.
A když tento důležitý jazyk nefunguje správně, lokální buněčná jednotka začne sát zdroje a nekontrolovaně růst, aniž by organismu cokoliv přínosného vracela. Vzniká rakovina, která organismus nejprve oslabí a nakonec zabije… — Však také jeden z důležitých proteinů této signalizační dráhy dostal jméno po geneticky podmíněném onemocnění, po adenomatózní polypózní kolitidě (APC). Příčinou této nemoci je mutace genu APC, který je důležitou součástí signalizace Wnt, protože v ní za normálních okolností degraduje protein beta-katenin. Poškození genu APC ale způsobí, že hladinu beta-kateninu nic nereguluje, což vede k nekontrolovanému dělení buněk. Moji skupinu zajímá signalizace Wnt především proto, že kontroluje také přesuny buněk z jednoho místa na druhé, což je vlastnost důležitá v kontextu leukemie, tedy nádorového bujení skupin bílých krvinek. Imunitní buňky se totiž organismem pohybují opravdu hodně a dráha Wnt by mohla být jedním z nástrojů, jak rozvoj leukemie přinejmenším brzdit.
A když už se buňka rozhodne dělit, je chyba spíše v ní, nebo špatně komunikuje signální dráha? — Víme, že v takovém případě je za nekontrolovatelné bujení zodpovědná buňka. Zpravidla má mutaci – třeba výše zmíněnou mutaci v APC –, kterou si můžeme přirovnat k neodbytnému vnitřnímu hlasu, hulákajícímu na ni: „Jsi v oblasti maximálního signálu, tak se děl a nepřestávej! Děl se! Děl se!“
Žer, dokud je co. — Ano, přesně v tom duchu. Signální dráha Wnt vznikla právě proto, aby k tomu nedocházelo a buňky jednaly v zájmu organismu. Tady se však buňka chová sobecky, což ve finále vede ke zničení celku.
Klíčem k léčbě tedy asi bude naše schopnost tomu bránit. — Myslím, že jsme našli jinou mezeru, na kterou se dá zaměřit.
Povídejte, přehánějte! — Předesílám, že náš postup byl v zásadě velmi jednoduchý – zaměřili jsme se na to, co bylo doposud nejméně známo. Na počátku jsme prostudovali literaturu s cílem proces příjmu signálu dráhou Wnt zrekonstruovat na molekulární úrovni a zjistit, co už je o jednotlivých prvcích systému známo. Víme velmi dobře, jak se ligand,1) v tomto případě molekula Wnt, naváže na receptor. Následně nastane v této „kanonické dráze“ útlum (inhibice) systému známého jako destrukční komplex, který kontroluje hladinu zmíněného beta-kateninu. Sekvence událostí mezi receptorem a destrukčním komplexem však do určité míry zůstává záhadou. Do hry vstupuje protein dishevelled, o němž víme, že jeho vyřazení ve všech dosud zkoumaných modelech přerušilo další předávání signálu. Nikdo zatím neví, co přesně se tam děje, proto to zkoumáme jak na úrovni strukturně biologické ve spolupráci s kolegy z CEITEC, tak na úrovni buněčně biologické a na některých složitějších živých modelech. Neříkám, že to rozlouskneme, ale mám dojem, že po téměř 18 letech, kdy funguje má laboratoř, už jsme hodně blízko.
Co zatím bránilo přesně pochopit chování proteinu dishevelled? — Dosavadní technologie, které byly schopné identifikovat interakce mezi proteiny, jen když byl celý komplex stabilní. Neumožňovaly ale přímo v buňce vidět, jak se dishevelled podílí na přechodných interakcích s dalšími molekulami. Bylo jen jasné, že nějak ano. Dále nás posunuly až metody, schopné monitorovat velmi nestálé, krátce trvající a na kontextu závislé interakce mezi proteiny – říká se tomu proximitní interaktomika. Ta umožňuje označit vše, co se v blízkosti sledovaného proteinu dishevelled děje v živé buňce.
V zásadě tedy jako kdybyste vyslali vojáka (protein dishevelled) do noční bojové akce a po rozbřesku pozorovali výsledek jeho činnosti. — Do určité míry nám výsledek akce ukázaly i starší technologie. Nevěděli jsme ale, co k výsledku vedlo, jestli se voják choval slušně a s kým spolupracoval. Nová technologie, kterou používáme také u jiných problémů, ale umí něco zásadního – umožňuje každému, s kým se voják dostal do kontaktu, přidělit značku.
Obarvíte si ho? — Ano. Vojákovi dáme do přílby zařízení, vystřelující do určité malé vzdálenosti barevné paintballové kuličky, které označí každou věc nebo člověka, do jejichž blízkosti voják vstoupí. Paintballová kulička se v našem světě jmenuje biotin. Mezi výhodné biochemické vlastnosti této molekuly patří, že vytváří kovalentní značení čili se nedá smýt. Současně po smrti buněk (lýzi) molekuly streptavidinu2) velmi účinně vychytávají veškerý biotin v roztoku. Analýza všech obarvených proteinů pomocí hmotnostní spektrometrie pak velmi přesně odhalí vše, co se v okolí vojáka, což je náš protein dishevelled, v noci odehrálo. V dalších „nocích“ pak můžeme vojákovi měnit podmínky mise. Jednou mu některé potenciální parťáky odstraníme, jindy mu nedáme pušku. Výsledek mise jsme mohli za takových okolností sledovat i předchozími metodami, nová technologie nám ale dovoluje vidět, jakým způsobem voják změnil taktiku, jak si pomohl, s jakými předměty či lidmi byl v kontaktu. Získáváme obrázek celkové dynamiky děje, umožňující pochopit základní principy vojákova rozhodování.
Zní to velmi elegantně. — Jako většina věcí, které trvají dlouho, než je někdo vymyslí. Což jsme my nebyli, jen je používáme, díky čemuž zvolna pronikáme k podstatě studovaného fenoménu.
Kam se vám díky tomuto přístupu podařilo posunout poznání? — Ne zase tak daleko, jak bychom si přáli. (směje se) Začínáme chápat, kdy a za jakých okolností protein dishevelled, pokud o něm budeme nadále uvažovat v metafoře vojáka, formuje určité typy jednotek. Chápeme situaci u různých mutací, spjatých třeba s chorobami. A chápeme rovněž význam procesu posttranslační modifikace, zejména fosforylace. Zabývá se tím velká část naší laboratoře, pracující s enzymem kasenkináza 1, který posttranslačně modifikuje protein dishevelled.
Tady na chvíli odbočím. Kináza je enzym, který přidává fosfátový zbytek na jiný protein, a je to velmi dobře známý mechanismus buněčné signalizace. Ve chvíli, kdy je fosfát na povrchu proteinu, stává se značkou, kterou rozpozná jiný protein, a signál tím posune dál. V případě proteinu dishevelled to ale vypadá, že popsaný proces funguje odlišně. Pro další signalizaci není tak důležité místo, na které se fosfát připne, ale jeho připnuté množství. Jde vskutku o masivní fosforylace desítek jednotlivých aminokyselin, které dokážou změnit náboj celého proteinu. Co bylo dříve kladné, začne být záporné. Náš voják (protein dishevelled) jako by tím přišel o původní uniformu a převlékl ji za jinou, což má velký vliv na jeho chování. Začne se shlukovat s úplně jinými kamarády. Jde samozřejmě o zjednodušení, vy jste přišel s tím vojákem, ale v tomto případě podle všeho nefunguje princip zámku a klíče, ale vše ovládá biofyzikální funkce přitažlivosti plusu s minusem, přičemž je úplně jedno, kdo náboj dodal. Z mého pohledu začíná svítat, co se tam děje. Je možné, že právě toto je zásadní trik či mechanismus, jakým námi studovaná signální dráha funguje.
Jak tedy? — Pokud by to bylo, jak popisuji, protein dishevelled by se jako nějaký reostat nabíjel, a v případě uvolnění signálu by se vybil. V systému současně existuje nějaká hladina, kdy už je změna náboje (převlečení uniformy) tak masivní, že do určité míry původní spolubojovníci u vojáka (proteinu dishevelled) rozpoznají jinou uniformu, a vyženou ho. A to je ta událost, která zajistí, že se signál posune dál.
Nemoci a jak je léčit
Kdy jste si uvědomili, že by to mohlo mít nějaké využití v léčbě nemocí? — Když jsme dospěli do místa, které jsem právě popsal, rozhodli jsme se prozkoumat, co se stane, když v tkáňových kulturách s chronickou lymfocytární leukemií zablokujeme důležitou součást signální dráhy Wnt, zmíněný enzym kasenkinázu 1. Pokusy ukázaly, že tento krok zastaví putování buněk organismem.
Uvědomil jste si už v tu chvíli, jak je to důležité? — Tehdy jsem o tom uvažoval jako o zajímavém výsledku, naznačujícím, že by leukemie mohla být chorobou buněčné migrace. Což asi bude fakt. Při tomto onemocnění se totiž rakovinou postižené imunitní buňky mohou dělit jen v některých částech těla, třeba v uzlinách, a když se tam dostanou, namnoží se a vydávají se na další pouť krevním řečištěm. Čím lépe tyto buňky dokážou migrovat do uzlin, tím je cyklus rychlejší a choroba agresivnější. V té chvíli jsem si řekl: „Tak pojďme zkusit, jestli leukemii dokážeme zastavit.“
Slyším vliv švédské etapy vaší kariéry a tuším, že jste hned objednal myši, které mají v genetické informaci zakódovanou leukemii. — Přesně tak. Sice to neumíme, ale jsme si jisti, že to musíme udělat, abychom přesvědčili sebe i ostatní, že hypotéza funguje. Naučili jsme se pracovat se svými prvními myšími modely a začali hledat inhibitor dostatečně dobrý, aby účinně fungoval. Teprve zpětně mi dochází, jaké extrémní štěstí jsme měli. Vidím stovky našich dnešních látek, a co vše musí splnit pro správnou funkci v živém organismu. My tehdy vybrali látky dvě, z nichž jedna se ukázala být funkční.
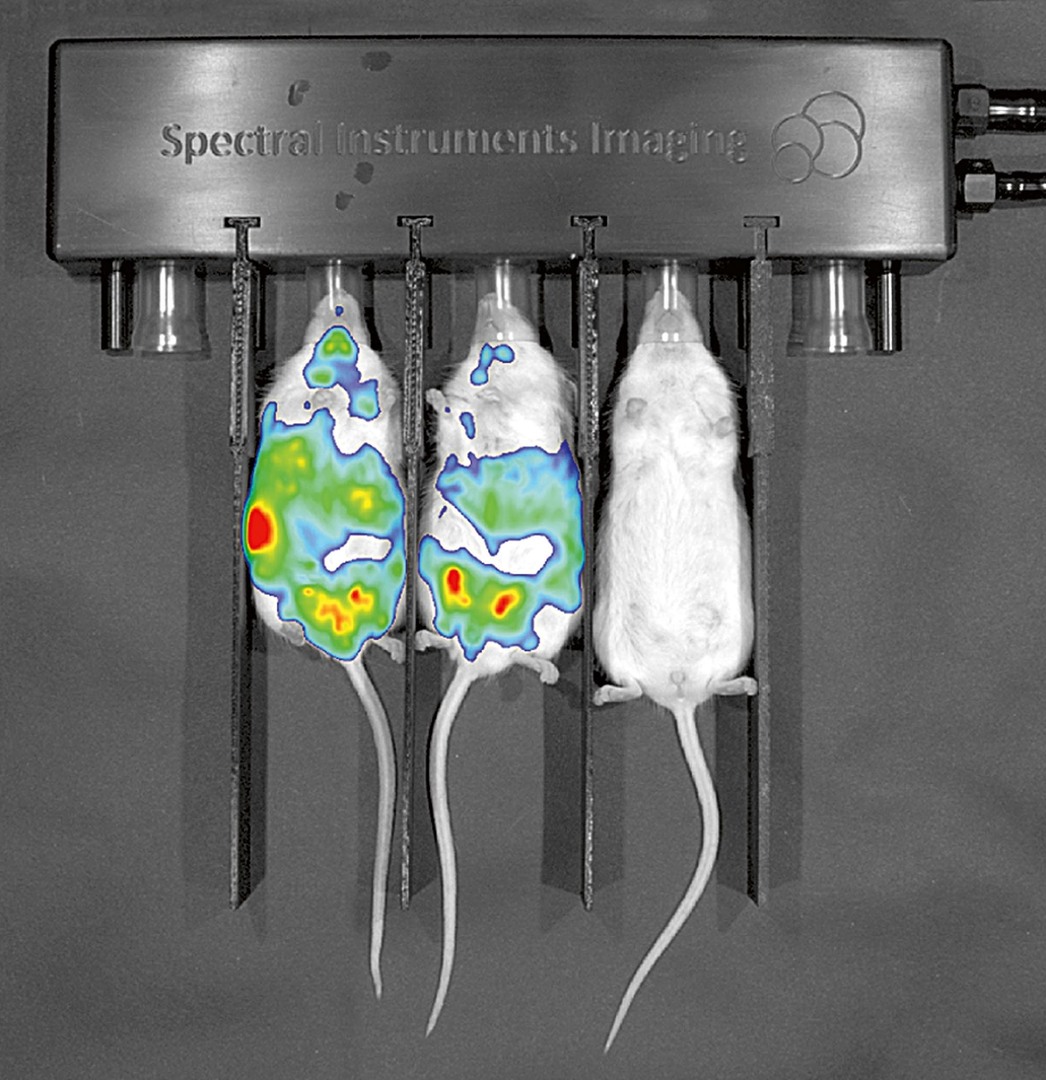
Zajímá mne ten okamžik, kdy jste zjistil, že to funguje. — Než jsme k němu dospěli, uplynul rok, který jsme od etické komise dostali na vykonání experimentu. Zvolili jsme co možná nejfyziologičtější postup, což znamená, že jsme čekali, až se u myší choroba rozvine sama. K tomu dochází po 8–9 měsících života. V této fázi jsme pak jedné skupině myší podávali účinný inhibitor, zatímco druhé, kontrolní skupině, placebo. Po roce se ukázalo, že takřka všechny myši, léčené placebem, umřely, zatímco ty, jež dostaly inhibitor, přežily.
Co přesně blokáda kaseinkinázy 1 v těle dělá? — Látka, aniž by nádorové buňky zabila, jim jednoduše zakazuje migrovat tělem. Jakmile jsme spatřili tento výsledek analýz, v prvním okamžiku jsme si uvědomili, že látky, které nikdo jiný v klinické praxi nepoužívá, mají reálné terapeutické využití. Jde v zásadě o součást celého nového směru vývoje terapeutik, jimž se říká migrastatika – látky, bránící zejména rozvoji metastáz tím, že omezují nebo blokují všechny způsoby invazivního pohybu nádorových buněk mezibuněčným prostředím.
Vaše prace už přesáhla rámec akademického výzkumu. Masarykova univerzita si nechala látky vyvinuté ve spolupráci vaší skupiny a skupiny chemika Kamila Parucha patentovat, založili jste spin- off firmu CasInvent, s cílem převést výzkumy do klinické praxe, a úspěšně jste přilákali spoustu investorů. Kde jste v tomto projektu teď? — Soustředili jsme se na jinou chorobu. Investoři totiž nechtěli jen zabránit rozvoji nějaké nemoci, chtěli úspěšný lék nemoci, u níž dnešní léčebné prostředky selhávají. Vybrali jsme si jinou leukemii – akutní myeloidní leukemii –, pro jejíž léčbu teď své látky připravujeme do první fáze klinické studie. Zatím předběžné výsledky naznačují, že naše látky na zmíněnou chorobu reagují velmi silně, blokují buněčné dělení a vyvolávají programovanou buněčnou smrt. Doufáme, že budou schopny nemoc také vyléčit.
Řekněme si, že akutní myeloidní leukemie je nemoc, která dnes tvoří až 80 % akutních leukemií u dospělých a 15–20 % u dětí. Celosvětově přitom její výskyt soustavně roste; ze 79 372 nových případů za rok 1990 na 144 645 nových nemocných v roce 2021. — Její průběh je navíc velmi agresivní. Kolegové z Fakultní nemocnice Brno nám tvrdí, že jde o jedno z nejhůře léčitelných nádorových onemocnění. Člověk, který akutní myeloidní leukemií onemocní, a není připraven na rychlou transplantaci kostní dřeně, což je jediná opravdu funkční léčebná péče, má naději na život v řádu týdnů, možná několika málo měsíců. Z pohledu celkového léčebného protokolu je proto zajímavá i perspektiva pouhého prodloužení čekací doby na transplantaci o pár měsíců. Cílem však zůstává nemoc popsaným způsobem vyléčit.
Klinické studie jsou běh na dlouhou trať s nejistým výsledkem. Fakt, že jste se přiblížili první fázi klinického testování, se tedy už dnes dá hodnotit jako velký úspěch. Jak odhadujete šance na jeho úspěšné dotažení do podoby léku? — Těžko říci. Aktuálně jsme ve fázi přípravy přihlášky, které se v branži říká „IND filing“, což je žádost o povolení klinické studie, shrnující veškeré dosavadní výsledky a testování. Na nejrůznějších zvířecích modelech teď sledujeme zejména bezpečnost navrženého postupu, stejně jako vlastní účinnost léčebné látky na modelech leukemie u laboratorních myší. Dostáváme se tím tak blízko člověku, jak jen je v laboratorních podmínkách možné. Nikdy také nevíme, kdy se může objevit něco neřešitelného, např. toxicita našich látek. Vstupujeme na neznámé pole, ale jsme optimisté, protože výsledky testů na zvířatech nám dávají mimořádnou naději. Vše ještě musí schválit nějaká regulatorní organizace. U nás to bude pravděpodobně Evropská léková agentura (European Medicines Agency, EMA) nebo Státní ústav pro kontrolu léčiv (SÚKL).
Vědecká část ale není tím jediným, co rozhoduje o úspěchu takového podniku. — V určitém období, kdy se blíží první fáze klinického testování, jsou mimořádně důležité i finance. Většinou jde o investiční částky na pokrytí veškeré agendy. Pro představu: když vyrábíte látku pro tkáňové kultury, potřebujete jí mikrogramy. Když ji vyrábíte pro myš, potřebujete miligramy, a pokud ji testujete na prasatech, nebo dokonce lidech, nejenže potřebujete výrazně větší garanci čistoty chemikálie, ale také řádově větší množství látky. Cílem je prokázat nejen její účinnost, ale zejména bezpečnost na široké baterii modelů. Riziko v průběhu procesu přirozené klesá, ale vyloučit nezdar nelze dopředu nikdy. Jsou látky, které končí v první fázi klinických testů, jiné ve druhé. Dopředu není nic jisté, přesto potřebujete milony až několik desítky milionů euro jen na tuto fázi, a to by spolupráce s týmem Fakultní nemocnice Brno, pokud by se tam případná první fáze klinického testování konala, tuto etapu o něco zlevnila oproti testování v jiné části vyspělého světa. Jde o témata, která aktuálně řeší kolegové. Obchodní část CasInventu se snaží přesvědčit současné investory, ať dají více prostředků, a také hledá další investory, abychom v případě, že dostaneme finální razítko, mohli klinickou studii spustit.
Návod pro následovníky
Před pěti lety jste v jednom rozhovoru říkal, že už budete v roce 2025 firmu prodávat. Jste dnes v této fázi? — Čas ukázal, že rozhodně ještě neprodáváme.
A příčina? — Jde spíše o zpoždění, než že bychom havarovali. Když si zpětně promítnu celý proces, který začal založením CasInventu během pandemie covidu-19, mám dojem, že vidím, čím to asi je. Pravdu měli kolegové, kteří mi už tenkrát říkali, že dokud to nezažiju, plně proces vzniku takové aplikační firmy nedocením. Je kupř. dost naivní si myslet, že lze takovou aktivitu dělat jako bokovku k běžné práci vyučujícího na vysoké škole, anebo nedej bože ještě ředitele akademického ústavu a garanta. Každému bych doporučil, ať přemýšlí především nad osobou, schopnou nově vznikající firmu řídit, neboť právě ona bude muset celý proces zrodu firmy tvrdě odpracovat.
Má to být kamarád, na kterého je spolehnutí, obchodník, nebo snad vědec? — V našem případě padla volba na externího člověka. Vedla nás k tomu potřeba mít v čele někoho, kdo nás trošku zaštítí před evropskými investory, z jejichž pohledu jsme byli neznámá firma z neznámé země. Řízení jsme proto nabídli ve Španělsku žijícímu Němci, který dříve působil ve Francii, a v oblasti vývoje léčiv se pohybuje celý život. Samozřejmě jsme mohli najmout lokálního dříče, třeba bývalého postdoka, ale rozhodli jsme jinak. Která varianta je správná, ukáže čas.
Kdybyste při zakládání CasInventu věděl, co víte o celém procesu dnes, jak byste se zachoval? — Určitě bych do toho šel znovu. Nemám z toho žádnou negativní zkušenost. Samozřejmě někdy na ty věci člověk chvilku kouká, je to jiný svět. Možná podruhé bychom na to – poučeni z chyb – potřebovali třeba jen dva nebo tři roky…
Co byste poradil někomu, kdo právě nosí v hlavě nápad, který, tak jako ten váš, překračuje akademické prostředí? — Pokud bude přemýšlet o komercializaci nebo založení spin-off firmy, radím předem si jasně stanovit a také dobře se svými kolegy vykomunikovat, že vložené peníze, energie a práce členů týmu povedou k výsledkům, které pravděpodobně nepůjdou publikovat. Takže z pohledu našeho akademického systému možná nebude možné nikdy vykázat jakoukoliv činnost. To je past, se kterou se systém snaží nepříliš úspěšně popasovat. Může se totiž stát, že aktivita nakonec skončí nezdarem, a veškerá energie v něm utopená bude neviditelná. Pro člověka, který ví, že si není schopen část výzkumné a výsledkové kapacity dát bokem, to proto může být složité. Z pohledu patentového se výsledky publikovat nesmí. Ve chvíli, kdy budou výsledky známy a publikovány, do vašeho podnikání nikdo investovat nebude, právě proto, že výsledky práce firmy chce vlastnit a nechce, aby někdo věděl, co má. Chcete-li převést svou vědu do byznysu, jsou tato témata nejtěžší a je třeba na ně myslet.
Ke stažení
 článek ve formátu pdf [498,77 kB]
článek ve formátu pdf [498,77 kB]
O autorovi
Marek Janáč