Nenápadný kolega z vedlejší laborky
| 1. 10. 2018Padesát let pracoval v Ústavu organické chemie a biochemie AV ČR. Jím připravené molekuly, odvozené od stavebních kamenů nukleových kyselin, pomáhají vážně nemocným pacientům a vynášejí miliardy dolarů. Ale řeč není o Antonínu Holém. Hrdinu tohoto příběhu téměř nikdo nezná a ústav na jeho molekulách nezbohatl. Organický chemik Alois Pískala se největšího zadostiučinění svého života dočkal letos v dubnu. Tři dny před svou smrtí.
Baltimore, říjen 2005. – „Firmu Guilford Pharmaceuticals, v níž jsem od roku 1998 pracoval, koupila společnost MGI Pharma. Právě v té době se chystala uvést na trh Dacogen, lék proti myelodysplastickému syndromu – onemocnění krvetvorby, které může přejít v akutní myeloidní leukemii. Když jsem se na účinnou látku podíval, ke svému překvapení jsem zjistil, že pochází od nenápadného tichého kolegy, který pracoval na ÚOCHB ve vedlejší laborce,“ vzpomíná chemik Pavel Majer, který v letech 1992 až 2010 působil ve Spojených státech, nejprve v NIH, poté v několika farmaceutických firmách. V roce 2011 se vrátil do Ústavu organické chemie a biochemie AV ČR (ÚOCHB), kde před lety jako doktorand začínal. Dnes tu vede skupinu medicinální chemie.
S kolegyní Marcelou Krečmerovou se začali zajímat jak o další osudy Aloise Pískaly, onoho nenápadného kolegy z časů dávno minulých, tak o možnosti vylepšení a terapeutického využití „jeho“ molekul.
Účinnou látkou Dacogenu je decitabin neboli 5-aza-2'-deoxycitidin, připravený Aloisem Pískalou v roce 1964. O rok dříve syntetizoval i chemicky příbuzný 5-azacytidin, který pod obchodním názvem Vidaza rovněž pomáhá pacientům s myelodysplastickým syndromem a s některými typy leukemie. Jen za loňský rok se tržby z prodeje těchto léků vyšplhaly ke dvěma miliardám dolarů. Ale nepředbíhejme.
Studenti Pískala a Holý
Hlučín, 30. března 1933. – Alois Pískala se nenarodil do zrovna idylických poměrů. „Pro značné neshody mezi rodiči jsem vyrůstal v hornické rodině svých prarodičů,“ napsal o 55 let později do svého životopisu. „Jeho otec šíleně žárlil, Lojzíka odmítl přijmout za svého a odešel od nich, matka na syna neměla čas, musela pracovat. ‚Maminko‘ oslovoval zpočátku svou babičku,“ vypráví Pískalova žena Hana.
Svou skutečnou matku, která pracovala jako dělnice ve Vítkovických železárnách, však miloval, po smrti prarodičů žil u ní a nechtěl ji „jen“ kvůli studiu opustit. „Ona ho však na školu poslala. Zřejmě rozpoznala, že má chytrou hlavu,“ říká Hana Pískalová. Alois nejprve dva roky (1948–1950) pracoval jako pomocná síla v laboratoři Závodů na zpracování dehtu v Ostravě, potom nastoupil na chemickou průmyslovku v Kolíně a v roce 1954 byl přijat ke studiu chemie na Matematicko-fyzikální fakultě UK. Spolu s Antonínem Holým.
„Jsme ze stejného ročníku, společně jsme procházeli zápočty, zkouškami, vojenskou přípravou, semináři, základními i pokročilými laboratorními cvičeními. Se svými diplomovými pracemi jsme se dokonce oba společně účastnili vysokoškolské studentské vědecké soutěže – nejprve jsme oba zvítězili v chemickém předkole v Pardubicích, abychom se nakonec o první místo rozdělili i v celostátním všeoborovém kole v Brně,“ napsal Antonín Holý při příležitosti Pískalových sedmdesátých narozenin v roce 2003 do Chemických listů.1)
Upravené molekuly
Praha, ÚOCHB, 60. léta. – V říjnu 1959 Pískala nastoupil do ÚOCHB. Jiří Gut mu jako téma aspirantury zadal „5-aza analoga pyrimidinových bází“. Zní to složitě, ale je to téma významné pro biologii a medicínu, blízké tomu, na němž pracoval Antonín Holý.
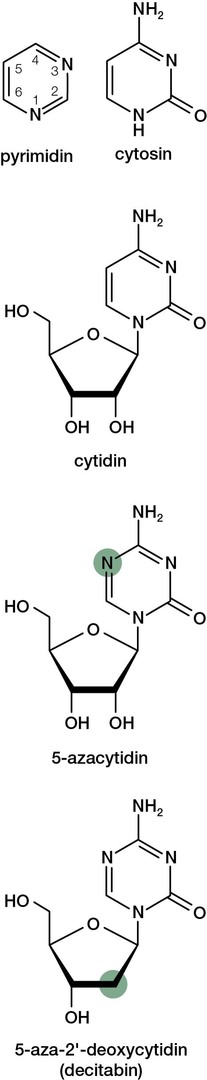
Pyrimidinové báze (uracil – U, thymin – T a cytosin – C) jsou spolu s bázemi purinovými (adenin – A, guanin – G) základními stavebními kameny nukleových kyselin. Předpona aza- značí, že studovaná analoga mají některý z uhlíků základní struktury (spolu s vodíkem) nahrazen dusíkem. A číslovka 5 udává, že tato náhrada se týká pátého atomu v pyrimidinovém cyklu (obr. 3).
Správně zvolená analoga mohou mít terapeutické využití. Dovedou se zapojit do vznikajících nukleových kyselin, ale díky přece jen odlišným vlastnostem se chovají jinak než molekuly, které na jejich místo přirozeně patří. Například si s nimi nemusí rozumět příslušné enzymy. Lze tak zastavit množení viru (jako u látek Antonína Holého), zahubit patogenní bakterii nebo třeba zablokovat dělení nádorových buněk (jako u látek Aloise Pískaly).
Pískalova práce navazovala na výzkum, který v ÚOCHB běžel už nějakou dobu předtím zásluhou otce zakladatele a dlouholetého ředitele ústavu Františka Šorma, který na oddělení organické chemie založil skupinu věnovanou výzkumu nukleových kyselin a jejich složek.
„Šorm byl hluboce přesvědčen, že se musí v nejbližší době najít mezi analogy látka, která by byla účinná proti rakovině. Z tohoto důvodu chtěl, aby se připravilo co nejvíce analogů,“ píše Alois Pískala ve své nepublikované práci Historie 5-azapyrimidinové chemie na ÚOCHB, kterou sepsal (či spíše nadiktoval) na sklonku života v domově důchodců. A dodává v ní: „O čistě chemickou problematiku Šorm nejevil nejmenší zájem. Mně se jednou přiznal: ‚Já už jsem na chemii blbej, tu přenechávám vám.‘“
Pískalovi kolegové nejprve pracovali s náhradou uhlíku v poloze 6. Syntetizovali například 6-azauridin, látku odvozenou od uridinu – nukleosidu přirozeně se vyskytujícího v RNA. Přirozenou formu tvoří uracil navázaný na ribózu, analog se liší onou jednou záměnou CH za N. Vykazoval protinádorové účinky, dokonce ho začala vyrábět Spofa coby lék na leukemii a licenci si koupila britská firma Distillers Co. Ale nebyl příliš účinný, měl výrazné nežádoucí účinky a brzy se přestal používat.
Dalším produktem úsilí organických chemiků byl 6-azauridintriacetát, který byl pod názvem Azaribine v roce 1975 ve Spojených státech schválen proti lupénce. O rok později však byl stažen, protože u malé části pacientů způsoboval trombózu.
Nyní tedy přišel na řadu Alois Pískala s úkolem zaměřit se na substituce uhlíku v poloze 5.
Šormovu zákazu navzdory
„Byly to zcela nové látky. Pískala musel zkoumat jejich fyzikálně-chemické vlastnosti a vypracovat pro ně různé druhy na míru šitých syntéz,“ vysvětluje Marcela Krečmerová.
„Ve zdokonalování metod byl dr. Pískala nedostižný jako experimentátor, schopný měnit reakční podmínky tak dlouho, až byl s postupem spokojen,“ napsal Antonín Holý ve výše citovaném článku v Chemických listech.
Pískala připravil nejprve 5-azauracil, který vykazoval jisté antibakteriální účinky, následně i z něj odvozený nukleosid 5-azauridin. Než se mu to podařilo, musel vyzkoušet řadu cest, které k výsledku nevedly. „Nebylo to úplně jednoduché. Vznikaly jiné produkty, než se čekalo, a když se odstranily chránící skupiny, kruh se úplně otevřel,“ říká Marcela Krečmerová.
Testy biologické aktivity navíc přinesly zklamání. Neodhalily nic, co by znamenalo naději pro budoucí terapeutické využití. Tím se výzkum 5-aza analogů dostal na slepou kolej a nechybělo mnoho, aby na ní i skončil. Pískala ve své „důchodcovské“ práci vzpomíná: „Šorm chtěl poté, co 5-azauridin nejevil žádnou biologickou účinnost, tematiku 5-aza pyrimidinů zrušit a vysloveně mi zakázal se zdržovat ještě přípravou 5-azacytidinu. Zřejmě vycházel z předcházející zkušenosti, která ukázala, že 6-azacytidin nejevil větší účinnost ve srovnání s 6-azauridinem.“
Pískala však věřil (a měl pro tuto víru chemické indicie), že by příprava 5-azacytidinu, tedy obdoby 5-azauridinu s cytosinem místo uracilu v roli výchozí báze (obr. 3), nemusela znamenat ztrátu času. „Takže chodil do laborky po večerech a o víkendech, kdy tam Šorm nebyl. Nakonec uvařil 5-azacytidin a předal ho biochemikům,“ popisuje Pískalovu partyzánštinu Marcela Krečmerová.2)
„Samozřejmě nás nenapadlo, že 5-azacytidin bude nejen účinným kancerostatikem, ale že bude transformovat nádorové buňky na nenádorové, což bylo tehdy v oblasti science-fiction.“
Biochemici zjistili, že látka má jednak antibakteriální, jednak cytostatické účinky. „Šorm, který se dočkal vytouženého vysoce účinného analogu, jenom zářil a hýřil organizační aktivitou. Do biochemického výzkumu 5-azacytidinu zapojil větší skupinu biochemiků a na mně chtěl hlavně větší množství pro biochemický výzkum, který mu nejvíc ležel na srdci, a pak naléhal na napsání především patentové přihlášky a potom také publikace […] Patentovou přihlášku jsem podal v polovině roku 1963,“ vzpomíná ve výše zmíněné práci Pískala a dodává detail, který později sehrál významnou roli v terapeutickém uplatnění 5-azacytidinu: „Samozřejmě nás nenapadlo, že 5-azacytidin bude nejen účinným kancerostatikem, ale že bude transformovat nádorové buňky na nenádorové, což bylo tehdy v oblasti science-fiction.“
Slibné výsledky testování 5-azacytidinu mimo jiné znamenaly impuls pro přípravu jeho derivátu, v němž by místo ribózy figurovala deoxyribóza. Zatímco 5-azacytidin představuje analog jednoho z nukleosidů tvořících RNA, deoxy- forma odpovídá svou strukturou nukleosidům DNA. „Šorm byl rozumný, neurazil se, že ho Pískala neposlechl, a uznal, že si tato problematika zaslouží další výzkum,“ komentuje to Marcela Krečmerová.
Absence jedné z hydroxylových (OH) skupin v molekule sacharidu však s sebou nese dvě nevýhody. Při syntéze mohou vznikat dva anomery (α a β), tedy dvě prostorová uspořádání lišící se polohou OH skupiny na prvním uhlíku deoxyribózy, přičemž žádoucí je pouze tvorba β anomeru (vyskytujícího se v DNA), takže se musí ze směsi separovat. A výsledná molekula je méně stabilní než s ribózou, především je náchylná na degradaci v kyselém prostředí.
Situaci komplikovala i skutečnost, že mnohé chemikálie potřebné pro syntézu nebyly v tehdejším Československu běžně dostupné a chemici si je museli připravovat sami, s vysokými nároky na čistotu produktu. Nakonec se ale syntéza 5-aza-2'- -deoxycitidinu (decitabinu) v roce 1964 podařila a Alois Pískala na tom měl klíčový podíl. Později postup ještě vylepšil. Preklinické studie na myších prováděné v ÚOCHB i klinické zkoušky v Montrealu v dalších letech ukazovaly na možnost využití k léčbě některých typů leukemie.
Ale cesta z laboratoře do klinické praxe bývá i u těch nejnadějnějších sloučenin dlouhá a jen málokdy vede k cíli.
Zájem farmaceutických firem
Zájem o opční smlouvu na využití 5-azacytidinu zpočátku projevily dvě farmaceutické firmy: německý Bayer a americký Upjohn. Bayer nabídl výhodnější podmínky – vyšší opční poplatek, menší množství požadovaných vzorků (100 g), navíc za ně byl ochoten zaplatit dobrou cenu. Upjohn naopak požadoval dodání dvou kilogramů látky zdarma. Roční opční smlouvu proto nejprve získal Bayer.
Pískala se dokonce vypravil do ústředí firmy ve Wuppertalu, kde přednášel o syntéze a vlastnostech 5-azacytidinu, a setkal se i s nejvyšším vedením firmy. Ale nakonec z toho nic nebylo. „Po uplynutí jednoroční opční lhůty firma Bayer nevykonala opci, ale zachovala se naprosto seriózně, vrátila všechny podklady a 5-azacytidin nezavedla do výroby,“ vzpomíná Pískala.
Následovalo uzavření opční smlouvy s firmou Upjohn. Alois Pískala připravil dva kilogramy 5-azacytidinu, které firma koupila za 2000 dolarů. „V podmínkách, v nichž to dělal, to byl mimořádný výkon. Je to obtížná chemie, záleží na kvalitě každého rozpouštědla, nesmí tam být stopa vody, člověk to musí mít opravdu v ruce,“ říká Marcela Krečmerová.
Jenomže v roce 1966 český emigrant L. J. Haňka, který pro Upjohn pracoval, publikoval zprávu o přirozené tvorbě 5-azacytidinu bakterií Streptoverticillium ladakanum. Přestože látku, kterou pojmenoval ladakamycin, neizoloval, znamenalo to ránu pro patentovou ochranu molekuly syntetizované Aloisem Pískalou. Z 5-azacytidinu se rázem stala látka přírodního původu. Americký patent se proto vztahoval pouze na postup syntézy, nikoli na látku samotnou.
„V té době tu nikdo pořádně neznal patentové právo, málokdo uměl dobře anglicky, nebylo reálné soudit se s americkou firmou.“
Upjohn po roce smlouvu neprodloužil s tím, že ve vývoji nebude pokračovat. Ale koncem sedmdesátých let si registroval lékovou formu 5-azacytidinu pod názvem Mylosar. „Zjistil jsem, že firma Upjohn s námi nejednala seriózně, když jako důvod pro nevykonání opční smlouvy uvedla, že tento preparát nebude vyrábět,“ ohlíží se za tou dobou Pískala.
Zástupci firmy tvrdili, že pro další výzkum a klinické zkoušky nepoužívali 5-azacytidin dodaný Aloisem Pískalou (jehož údajně nespotřebovanou část však nikdy nevrátili), ale vlastní ladakamycin získaný z bakterie. „Ten by ale neměl ani desetiprocentní čistotu, biotechnologická cesta získávání této látky ve skutečnosti neexistovala, zřejmě to byl kompletně podvod,“ domnívá se Pavel Majer. „V té době tu nikdo pořádně neznal patentové právo, málokdo uměl dobře anglicky, nebylo reálné soudit se s americkou firmou,“ doplňuje Marcela Krečmerová.
Mylosar nicméně v té době díru do světa neudělal, byť v klinických zkouškách vykázal nadějné výsledky zejména proti akutní myeloidní leukemii. Podával se ve velkých dávkách, při nichž se projevovaly silné vedlejší účinky, takže k jeho nasazení do klinické praxe nakonec nedošlo.
Po ukončení opční smlouvy s firmou Upjohn projevila o 5-azacytidin zájem i další americká společnost, Bristol-Myers. Firma nežádala žádné podklady o výrobě ani žádný vzorek, šlo jí výhradně o patentová práva. Jenomže v té době se už plně projevil patologický přístup tehdejšího Československa k mezinárodnímu využití patentů na objevy a vynálezy československých vědců.
Místo vedoucího Ústředí pro vynálezy o objevy ČSAV zaujal jistý JUDr. Pivrnec, kterého v souvislosti se svým úsilím o využití patentové ochrany na kontaktní čočky zmiňuje ve svých pamětech v nelichotivých souvislostech i Otto Wichterle.3) „Jelikož Šorm byl pro svůj negativní postoj k intervenci v srpnu 1968 […] zbaven všech svých funkcí a byl vystaven tvrdé diskriminaci tehdejším režimem, pro Pivrnce bylo politicky nemyslitelné, aby ČSAV uzavírala na Šormův patent spolupráci s americkou firmou, a proto nabídku striktně odmítl,“ vzpomíná Pískala.
Později projevili zájem ještě zástupci francouzské firmy Sanofi a jedna japonská společnost, ale k uzavření další smlouvy už nedošlo.
Ani decitabin neznamenal pro ÚOCHB zlatý důl, přestože ústav byl jediným dodavatelem materiálu pro klinické zkoušky. „Stojí však za zmínku, že decitabin, kterým se dnes léčí pacienti v USA a Kanadě, a kterého se klinikám dostalo prostřednictvím našeho exportního podniku, stále pochází z vlastních rukou dr. Pískaly,“ psal ještě v roce 2003 Antonín Holý v Chemických listech.
Epigenetická revoluce
University of Southern California, Los Angeles, 1980. – Až do konce sedmdesátých let se k 5-azacytidinu a decitabinu přistupovalo jako ke klasickým cytostatikům, jejichž úkolem je nádorové buňky zabít. Decitabin se inkorporuje do DNA, 5-azacytidin do různých typů RNA a v menší míře také do DNA. Výsledkem je narušené kopírování nukleových kyselin, nefunkční ribozomy a omezená tvorba proteinů. V tomto smyslu slibovaly klinické zkoušky jistou naději na úspěch, překážkou však byly vážné vedlejší účinky spojené s nutností podávat léky ve vysokých dávkách.
Vše se změnilo zásluhou Petera A. Jonese z Univerzity jižní Kalifornie v Los Angeles a jeho doktorandky Shirley Taylor. Pracovali s 5-azacytidinem syntetizovaným podle původní Pískalovy receptury a při pokusech s myšími embryonálními buňkami zjistili, že tato látka v mikromolárních koncentracích indukuje buněčnou diferenciaci a inhibuje metylaci cytosinu v DNA. Své výsledky publikovali v letech 1978 a 1980.4)
Díky tomu vyšlo najevo epigenetické působení Pískalových molekul. V některých typech nádorových buněk je ve zvýšené míře v DNA metylována dinukleotidová sekvence CG. Tím jsou deaktivovány tumor supresorové geny, buňky se nediferencují a pokračují v dělení. Metylaci zajišťuje enzym DNAmetyltransferáza. Pokud se setká s 5-azacytidinem, kovalentně se na něj naváže a nemůže dále pokračovat v metylaci. „Vypnuté“ tumorsupresorové geny se tím opět „zapnou“. Nádorovou buňku lze vrátit do normálního buněčného cyklu a donutit ji k diferenciaci – jinými slovy zbavit ji jejího nádorového charakteru. Není třeba ji zabíjet.
„Ukázalo se, že 5-azacytidin má dvojí mechanismus účinku. Ve velkých dávkách je to klasické cytostatikum, které ale není lepší než jiná, už dříve dostupná cytostatika. V malých dávkách se však projeví epigenetický účinek,“ shrnuje Marcela Krečmerová. Decitabin funguje obdobně.
Peter A. Jones měl v roce 2006 na ÚOCHB zvanou přednášku s názvem Pražská azanukleosidová léčiva a počátky epigenetické terapie. Při té příležitosti se s Aloisem Pískalou setkal a velice si tohoto setkání považoval. Paní Pískalová uchovává zarámovanou společnou fotografii obou vědců, k níž Jones připsal: „Je mi skutečnou ctí a výsadou, že jsem mohl konečně navštívit ústav, kde byly 5-azacytidin a decitabin syntetizovány. Pracuji s těmito látkami třicet let a budou znamenat revoluci v léčbě rakoviny.“
Díky zjištěním Jonesova týmu byly po roce 2000 obě Pískalovy látky konečně schváleny k použití v klinické praxi – 5-azacytidin uvedla v roce 2004 na trh pod názvem Vidaza společnost Celgene, decitabin následoval v roce 2006. Pod názvem Dacogen ho jako léčivo vyvíjela firma SuperGen, která ho ještě před schválením postoupila společnosti MGI Pharma. Tu později koupila japonská Eisai, která později prodala práva další japonské firmě Otsuka Pharmaceutical.
Oba léky se používají především k léčbě myelodysplastického syndromu, Dacogen je v zemích EU registrován i k léčbě akutní myeloidní leukemie. Pomáhají především starším pacientům, u nichž se myelodysplastický syndrom nejčastěji vyskytuje a u kterých nelze nasadit klasickou chemoterapii. Díky epigenetickému působení lze Vidazu i Dacogen podávat v malých koncentracích s menšími vedlejšími účinky.
Hledání nových cest
Praha, ÚOCHB, 2018. – Ale čas se nezastavil ani na Pískalově domovském pracovišti. Marcela Krečmerová s dalšími kolegy ze skupiny Pavla Majera hledá cesty, jak původní molekuly modifikovat ve snaze vylepšit jejich vlastnosti, případně najít pro ně nová terapeutická využití.
Jednou z nevýhod jak Vidazy, tak Dacogenu je jejich značná nestabilita. Poločas eliminace 5-azacytidinu po injekční aplikaci do podkoží je asi 41 minut, u 5-aza-2'-deoxycitidinu pouhých 20 minut.
Do nemocnic se lék distribuuje jako lyofilizát plus všechny přídavné látky. Roztok musí být připraven těsně před podáním pacientovi, který ho pak musí dostat během několika minut,“ vysvětluje Marcela Krečmerová. V České republice je jen několik onkologických center, která s takovými léky umějí zacházet. Staří a vážně nemocní lidé proto musí za léčbou často dojíždět zdaleka.
„Bylo by dobré molekulu upravit, aby byla stabilnější a zároveň neztratila svou účinnost. Připravit proléčivo, s nímž se lépe manipuluje a které se do aktivní formy převede až v organismu. Ale za padesát let se to ještě nikomu nepodařilo,“ říká Pavel Majer.
Vědci z ÚOCHB spolupracují s Johns Hopkins University. Tamní odborníci testují chování „pražských molekul“ v biologickém prostředí. Aktuálně pracují s molekulou, která výše zmíněné problémy řeší, a navíc se zdá, že by mohla najít využití i při léčbě syndromu akutní dechové tísně (ARDS). Výsledky však zatím nebyly ani publikovány, ani patentovány, takže nelze zacházet do detailů. A zdaleka není vyhráno. Může se například ukázat, že látka je až příliš stabilní.
Ocenění na sklonku života
Alois Pískala do ÚOCHB docházel asi do roku 2009. Už předtím prodělal mrtvici, po níž ochrnul na pravou část těla a práce v laboratoři se musel vzdát. „Potkávala jsem se s ním dlouhá léta. Když člověk potřeboval nějakou chemikálii, on všechno měl. A také všechno věděl. Byl z generace lidí, kteří opravdu uměli ‚vařit‘. V jeho době si chemik musel umět udělat leccos sám, nic se pořádně nedalo koupit. Pískala i Holý uměli z organiky všechno,“ vzpomíná Marcela Krečmerová.
Závěr života Alois Pískala trávil v domově pro seniory v Českém Brodě. V roce 2013, ve svých osmdesáti letech, se oženil. Nějakou dobu ještě chodil s hůlkou na procházky, poslední čtyři roky už ale z domova prakticky nevycházel. Tělo ho zrazovalo, mozek však stále pracoval na plné obrátky. „V noci moc nespal, pořád myslel na vylepšení těch svých vzorečků. Žil chemií,“ vypráví Hana Pískalová.
Potvrzují to i Marcela Krečmerová a Pavel Majer, kteří ho od podzimu 2017 navštěvovali. A k jeho 85. narozeninám mu připravili překvapení. Pozvali ho do ÚOCHB, kde mu ukázali nově zařízené laboratoře a uspořádali přednášku o historii jeho molekul. Narozeniny oslavil 30. března letošního roku, setkání na jeho počest proběhlo v ÚOCHB v pátek 6. dubna. Tři dny poté, 9. dubna, Alois Pískala zemřel. „Lojzík se z návštěvy ÚOCHB strašně radoval. I když se z Prahy vrátil unavený a vyčerpaný, říkal mi: ‚Stálo mi to za to.‘ Dostal horečku, snad to radostné vzrušení a zároveň vypětí neuneslo srdíčko. Usnul mi v náručí a už se neprobudil,“ vypráví o jeho posledních okamžicích paní Hana. „Je to tak dobře. On musel vždy všechno dokázat sám, nechtěl s ničím pomoci, a když mu něco nešlo, byl nervózní až vzteklý. Kdyby měl trvale ulehnout, bylo by to pro něj jen trápení.“
Vznik tohoto textu podpořil ÚOCHB AV ČR.
Poznámky
1) Holý A., Chem. Listy 97, 277–278, 2003.
2) Pískalovy tehdejší publikace v Collection of Czechoslovak Chemical Communications.
3) Wichterle O.: Vzpomínky. Academia, Praha 2007, 4. vydání, ISBN 978-80-200-1495-5 (zmínky o Pivrncovi: s. 135, 170).
4) Constantinides P. G., Taylor S. M., Jones P. A., Dev. Biol., 66, 57–71, 1978/1, PMID: 87352; Jones P. A., Taylor S. M., Cell, 20, 85–93, 1980/1, PMID: 6156004.
Ke stažení
 článek ve formátu pdf [565,08 kB]
článek ve formátu pdf [565,08 kB]
O autorovi
Ondřej Vrtiška