Zapojení vědců do projektu česko-norského výzkumu
7. 4. 2016
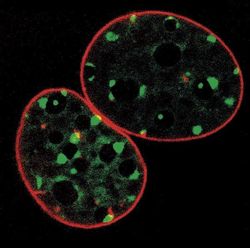 Název projektu: Jaderná architektura během regulace autofagie, reparace DNA a při genové expresi (NuArch)
Název projektu: Jaderná architektura během regulace autofagie, reparace DNA a při genové expresi (NuArch)
číslo projektu: 7F14369
Řešitel koordinátor: doc. RNDr. Eva Bártová, Ph.D.
email: bartova@ibp.cz
Biofyzikální ústav, AV ČR, v. v. i., Královopolská 135, 612 65, Brno
Členové projektu:
Eva Bártová, Philippe Collas, Anne Simonsen, Thomas Küntziger, Stanislav Kozubek, Soňa Legartová, Jana Krejčí, Jana Suchánková, Petra Sehnalová, Alena Kovaříková, Torunn Rønningen, Serhiy Pankiv, Klubhushan Sharma, Michal Franek.
Koordinátor projektu:
Biofyzikální ústav je jedním z ústavů Akademie věd České republiky (AV ČR). Institut má vybudovanou kvalitní infrastrukturu zahrnující nejen vědecké zázemí, ale i ekonomickou a technickou podporu. Technické a přístrojové zabezpečení je získáváno prostřednictvím mnoha národních i mezinárodních projektů a za podpory Akademie věd ČR. Některé laboratoře ústavu však navíc spolupracují s univerzitami, jako je Masarykova univerzita v Brně nebo Univerzita Karlova v Praze.
Partneři mezinárodního projektu:
 Ústav základního lékařského výzkumu (Institute of Basic Medical Sciences) Univerzity v Oslu je jedním z hlavních výzkumných center v Norsku. Zaměstnává více než 400 vědců v přibližně 40 výzkumných skupinách, včetně zaměstnanců Norského centra pro výzkum kmenových buněk (Norwegian Stem Cell Centre). Aktivity norského ústavu jsou propojeny s Národní nemocnicí a jejími klinickými laboratořemi. Hlavní výzkumné aktivity zahrnují vědy o výživě, neurofyziologii, genetice, buněčné signalizaci a regulaci buněčného cyklu u nádorových buněk. Spolupracující skupina se rovněž intenzivně věnuje studiu autofagie (lysozomální rozklad proteinů) a biologie kmenových buněk, se zaměřením na epigenetiku (modifikace histonů a DNA).
Ústav základního lékařského výzkumu (Institute of Basic Medical Sciences) Univerzity v Oslu je jedním z hlavních výzkumných center v Norsku. Zaměstnává více než 400 vědců v přibližně 40 výzkumných skupinách, včetně zaměstnanců Norského centra pro výzkum kmenových buněk (Norwegian Stem Cell Centre). Aktivity norského ústavu jsou propojeny s Národní nemocnicí a jejími klinickými laboratořemi. Hlavní výzkumné aktivity zahrnují vědy o výživě, neurofyziologii, genetice, buněčné signalizaci a regulaci buněčného cyklu u nádorových buněk. Spolupracující skupina se rovněž intenzivně věnuje studiu autofagie (lysozomální rozklad proteinů) a biologie kmenových buněk, se zaměřením na epigenetiku (modifikace histonů a DNA).
Popis projektu:
Je známo, že mnoho proteinů představuje základní stavební jednotky pro architekturu buněčného jádra. Tyto proteiny jsou také zapojeny do dalších klíčových procesů, jako je replikace DNA, transkripce a reparace DNA. Funkční význam proteinů, například laminů tvořících jadernou membránu, dokládá i počet a rozmanitost vzácných onemocnění, souhrnně označovaných jako patologie jaderné slupky (jde například o takzvaný Hutchinson–Gilford progeria syndrom neboli syndrom předčasného stárnutí). Zmíněná onemocnění vznikají následkem mutací v odpovídajících genech, jako je například LMNA gen nebo u mnoha nádorových buněk gen TP53. Náš projekt, zabývající se jadernou architekturou, je založen na předpokladu, že jaderné strukturální proteiny (kódované zmíněnými geny) se kromě jejich role v regulaci genové exprese rovněž zapojují do procesu autofagie a oprav poškozené DNA. Nestandardní funkce vybraných proteinů, jako jsou laminy, protein p53 a nebo HP1 proteiny heterochromatinu, vedou k poruchám autofagie a k chybám v opravných signalizacích genomu. To má významné dopady na buněčnou homeostázu, jejíž porušení může vést i k maligní transformaci buněk. Náš projekt by měl přispět k objasnění nových úloh jaderných proteinů a měl by propojit nové poznatky se známými buněčnými mechanismy tak, aby byl nalezen vztah mezi funkcí studovaných proteinů a vznikem onemocnění, jako je syndrom předčasného stárnutí nebo i nádorová onemocnění.
Řešení projektu během roku 2015:
Během roku 2015 se nám podařilo úspěšně upevnit česko-norskou spolupráci. Český tým uspořádal společnou pracovní schůzku, při které došlo k výměně znalostí mezi studenty, doktorandy a vědeckými pracovníky z obou zemí. Během řešení projektu jsme rovněž získali velmi cenné experimentální výsledky, které jsme publikovali v pěti zahraničních časopisech, jako například britský časopis Biology of the Cell a Epigenetics & Chromatin nebo histochemický časopis, vydávaný v Německu, Histochemistry and Cell Biology. Naše poznatky byly rovněž prezentovány formou zvaných přednášek na několika mezinárodních kongresech, například ve Vídni, Zadaru, japonské Awaji, Praze nebo v Novosibirsku. Náš projekt je však projektem základního výzkumu, tudíž cílem projektového návrhu nebyla přímá aplikace poznatků do klinické praxe, ale zaměřujeme se na studium biologie některých nemocí, včetně již zmíněných laminopatií a nádorových onemocnění. Naše zjištění by mohla potencionálně přispět k vylepšení nových terapeutických postupů, a to zejména v radioterapeutické léčbě. Z tohoto pohledu studujeme mechanismy oprav poškozené DNA po ozáření buněk ionizujícím zářením, a dále v kontextu oprav DNA testujeme účinky klinicky významných inhibitorů enzymů zodpovědných za funkční modifikace histonů.
Ke stažení
 článek ve formátu pdf [220,39 kB]
článek ve formátu pdf [220,39 kB]





















