Jak odstranit běžné potíže při fotometrickém stanovení koncentrace a čistoty biomolekul
Fotometrické stanovení koncentrace a čistoty molekul jako DNA, RNA či proteinů, je jednou z nejjednodušších a nejrozšířenějších metod běžně používaných v laboratořích. Přesto anebo možná právě proto, že „na tom nic není“, lze při fotometrických měřeních narazit na několik úskalí, která způsobí, že uživatel kýžený výsledek, tedy koncentraci biomolekuly, buď vůbec nedostane, anebo získané hodnotě nevěří.
 Jak to tedy udělat, aby bylo možné věřit výsledkům měření koncentrací biomolekul? Z diskuzí s mnoha uživateli spektrometrů vyplynulo, že stačí dodržovat tři základní principy: znát Lambert- Beerův zákon, přemýšlet o tom, co měřím a dodržovat správnou laboratorní praxi. Dovolím si začít s vyjmenovanými principy odzadu. Od jednoduššího ke složitějšímu. Zdá se sice zbytečné to opakovat, ale bublinky v kyvetách či kontaminace méně koncentrovaných roztoků roztoky více koncentrovanými, např. při měření standardních křivek moc spolehlivým výsledkům nenahrávají. Je důležité vědět, co měřím. Samozřejmě měřím proto, abych zjistila koncentraci, ale ve většině případů lze předpokládat, kde se absorbance vzorku, tedy potažmo jeho koncentrace, bude pohybovat. Podle toho lze zvolit správný přístup k měření, tak aby výsledek byl opravdu spolehlivý. Jiný přístup je totiž třeba volit na více koncentrované vzorky a jiný na vzorky s nízkou či velmi nízkou koncentrací.
Jak to tedy udělat, aby bylo možné věřit výsledkům měření koncentrací biomolekul? Z diskuzí s mnoha uživateli spektrometrů vyplynulo, že stačí dodržovat tři základní principy: znát Lambert- Beerův zákon, přemýšlet o tom, co měřím a dodržovat správnou laboratorní praxi. Dovolím si začít s vyjmenovanými principy odzadu. Od jednoduššího ke složitějšímu. Zdá se sice zbytečné to opakovat, ale bublinky v kyvetách či kontaminace méně koncentrovaných roztoků roztoky více koncentrovanými, např. při měření standardních křivek moc spolehlivým výsledkům nenahrávají. Je důležité vědět, co měřím. Samozřejmě měřím proto, abych zjistila koncentraci, ale ve většině případů lze předpokládat, kde se absorbance vzorku, tedy potažmo jeho koncentrace, bude pohybovat. Podle toho lze zvolit správný přístup k měření, tak aby výsledek byl opravdu spolehlivý. Jiný přístup je totiž třeba volit na více koncentrované vzorky a jiný na vzorky s nízkou či velmi nízkou koncentrací.
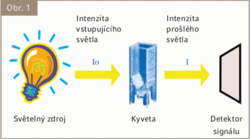
 Pro účely ilustrace si dovolím v následujícím textu zjednodušovat. Co se děje v konvenčním spektrofotometru? Ze zdroje světla vychází paprsek, dosáhne vzorku v kyvetě, kde je část světla absorbována molekulami vzorku. Část světla se pak dostane z kyvety dál a je zachycena detektorem (viz. obr. 1). Vztah mezi absorbancí vzorku a světlem, vstupujícím do kyvety a vycházejícím z kyvety, popisuje zákon pánů Lamberta a Beera (viz. obr. 2), kde Ԑ je extinkční koeficient (udává, jak vzorek absorbuje světlo), l je rozměr kyvety v cm a c je koncentrace.
Pro účely ilustrace si dovolím v následujícím textu zjednodušovat. Co se děje v konvenčním spektrofotometru? Ze zdroje světla vychází paprsek, dosáhne vzorku v kyvetě, kde je část světla absorbována molekulami vzorku. Část světla se pak dostane z kyvety dál a je zachycena detektorem (viz. obr. 1). Vztah mezi absorbancí vzorku a světlem, vstupujícím do kyvety a vycházejícím z kyvety, popisuje zákon pánů Lamberta a Beera (viz. obr. 2), kde Ԑ je extinkční koeficient (udává, jak vzorek absorbuje světlo), l je rozměr kyvety v cm a c je koncentrace.
Z uvedeného tedy vyplývá, že mezi koncentrací a absorbancí je lineární vztah. Je tomu tak ale doopravdy? Ze zmíněného zákona také jednoduše vypočítáme koncentraci. Různé molekuly mají různé extinkční koeficienty resp. konverzní faktory (1/Ԑ). Například široce známý a běžně užívaný konverzní faktor pro dsDNA je 50 (μg/ml)cm.
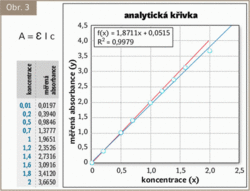 Na grafu obr. 3 je v ynesena koncentrace v z ávislosti na absorbanci. Červená křivka ilustruje vztah mezi veličinami dle zákona Lamberta a Beera. Naměřená data v laboratoři, reprezentovaná modrými body a modrou křivkou, ale ukazují, že linearita mezi veličinami platí zhruba do hodnoty absorbance 1,5. Nad touto hodnotou se křivka naměřených hodnot začíná odchylovat od křivky teoretických hodnot. Co to znamená prakticky? Aby jakékoli fotometrické měření bylo spolehlivé, mělo by se pohybovat v oboru hodnot absorbancí mezi 0,1 a maximálně 1,5. Absorbance pod 0,1 není spolehlivá z důvodu složitého odlišení signálu vzorku od signálu pozadí měřícího systému. (A = 0,1 v 1 cm kyvetě odpovídá koncentraci 5 ng/μl u dsDNA). Toto je také důvod, proč je důležité vidět na přístroji skutečná naměřená data absorbance při měření v použité kyvetě a ne data extrapolovaná na A1cm.
Na grafu obr. 3 je v ynesena koncentrace v z ávislosti na absorbanci. Červená křivka ilustruje vztah mezi veličinami dle zákona Lamberta a Beera. Naměřená data v laboratoři, reprezentovaná modrými body a modrou křivkou, ale ukazují, že linearita mezi veličinami platí zhruba do hodnoty absorbance 1,5. Nad touto hodnotou se křivka naměřených hodnot začíná odchylovat od křivky teoretických hodnot. Co to znamená prakticky? Aby jakékoli fotometrické měření bylo spolehlivé, mělo by se pohybovat v oboru hodnot absorbancí mezi 0,1 a maximálně 1,5. Absorbance pod 0,1 není spolehlivá z důvodu složitého odlišení signálu vzorku od signálu pozadí měřícího systému. (A = 0,1 v 1 cm kyvetě odpovídá koncentraci 5 ng/μl u dsDNA). Toto je také důvod, proč je důležité vidět na přístroji skutečná naměřená data absorbance při měření v použité kyvetě a ne data extrapolovaná na A1cm.
Na trhu existují přístroje, které údajně dokáží měřit A = 30 a dokonce A = 300. Prostým dosazením do rovnice si řekněme, co by to asi znamenalo. Je-li transmitované světlo 100 % (projde všechno světlo), je absorbance rovna 0. Je-li transmitované světlo 10 %, pak je absorbance rovna 1. Projde-li 1 % původního paprsku je A = 2. Teď obráceně, řekněme při A = 6 je světlo, které prošlo, rovno 0,0001 % původního paprsku. Zkusme si jen představit, kolik nul za desetinnou čárkou by mělo číslo odpovídající A = 30 či 300. A je takové měření vůbec k něčemu?
Pokud vás text zaujal, najděte si pokračování v dalším čísle, kde bude ukázáno, jak absorbanci a koncentraci ovlivňuje rozměr kyvety a jaký je správný přístup k měření velmi nízkých či velmi vysokých koncentrací biomolekul.
Zaujaly Vás tyto jednoduché typy z oblasti praktických přístupů ke stanovené koncentrací a čistoty biomolekul? Více se můžete dozvědět na semináři, na který se bude možno přihlásit od září letošního roku na webových stránkách http://www.eppendorf.cz.
Ke stažení
 článek ve formátu pdf [414,5 kB]
článek ve formátu pdf [414,5 kB]















