Cena medicíny
Naše současnost budí dojem, že teprve nyní se kromě odborného a etického hlediska začíná přihlížet k otázkám nákladů spojených s péčí o zdraví. Obecný pohled ilustrují konkrétní údaje o chronické myeloidní leukemii.
Známe cenu zdravotní péče?
Zhruba před dvaceti lety, v době počátků prenatální diagnostiky vrozených a dědičných poruch, jsme se pokoušeli pro tento obor získat nějaké finanční zdroje. Navštívili jsme ministerstvo zdravotnictví v přesvědčení, že by bylo prozíravé investovat do prenatální diagnostiky prostředky, které by se mohly dlouhodobě a mnohonásobně vrátit snížením počtu postižených. K našemu velkému překvapení se ukázalo, že ministerstvo nemá představu o tom, kolik stojí léčení té které nemoci, ani o cenách zdravotní péče vůbec.Občas se mi zdá, že se situace příliš nezměnila. Celkem chápu, že se politici bojí přiznat, že zdravotní péče je drahá a náklady na ni porostou, ať budeme sebehospodárnější. Mají zřejmě dojem, že to není dost líbivé, stejně jako nebylo a není příjemné připustit, že produktivita práce je v našich zemích poměrně nízká ve srovnání s tím, na jakou zdravotní péči si činíme nárok.
 Stejně zarážející a málo pochopitelná je představa pacientů, tedy občanů, kteří tuto péči přijímají, že jediným kritériem je lidskost. Dokonce se domnívají, že z ní vyplývá kvalita zdravotní péče. Lidskost by v péči o zdraví nikdy neměla chybět, avšak její kvalita a bohužel i míra lidskosti významným způsobem souvisejí s množstvím vynaložených prostředků.
Stejně zarážející a málo pochopitelná je představa pacientů, tedy občanů, kteří tuto péči přijímají, že jediným kritériem je lidskost. Dokonce se domnívají, že z ní vyplývá kvalita zdravotní péče. Lidskost by v péči o zdraví nikdy neměla chybět, avšak její kvalita a bohužel i míra lidskosti významným způsobem souvisejí s množstvím vynaložených prostředků.
Drsná ekonomika péče o zdraví
Na hospodárnost nebo jinými slovy na účelné využití nákladů se v péči o zdraví musíme dívat z více stran.Základním hlediskem je, zda je účelné použít část národního produktu k péči o zdraví. Byť se otázka zdá být banální, je poněkud záludná a odpověď se naší křesťanské morálce nemusí zamlouvat. Z čistě ekonomického hlediska jsou náklady na péči o zdraví vynaloženy neúčelně, pokud nevedou k tomu, že se poruchám zdraví vyhneme nebo je bezezbytku odstraníme. Řečeno ještě méně ohleduplně, za nehospodárnou by se dala považovat léčba nevyléčitelně nemocných a starých, kteří již nevytvářejí národní produkt a ani nebudou moci přispět k jeho tvorbě. Ačkoliv se mnou leckdo nebude souhlasit, v přírodě to tak chodí. Smyslem naší biologické existence je tvorba potomstva a ta rozhodně příliš nepřekračuje dobu vzniku nové generace schopné samostatného života.
Faktem je, že u organizmů vytvářejících společenství se vyvinulo něco, čemu lze říkat kolektivní vědomí – určitý způsob někdy asi i vědomé spolupráce a dělby úkolů, s nímž souvisí solidarita a altruizmus. Platí to i pro člověka, který si tyto kategorie zařadil mezi filozofické pojmy a často i návody k chování v rámci mnohých náboženství. Spíše tedy emocionálně připouštíme nehospodárnost systémů péče o zdraví tam, kde by se dostávaly do konfliktu s pocitem solidárnosti. Jestliže tedy myšlenku nestarat se o beznadějně neproduktivní občany zavrhneme, musíme zvážit, jakou část našeho národního produktu na to věnujeme. Chceme-li se srovnávat s vyspělými státy, což patrně z hlediska odborné úrovně naší medicíny můžeme, měli bychom při slabší výkonnosti naší ekonomiky věnovat na péči o zdraví relativně větší podíl prostředků než do ostatních sfér spotřeby (a také větší než země, na jejichž úroveň bychom se rádi dostali).
Demokratičnost systémů péče o zdraví
Demokratičnosti se týká druhá otázka, na niž bychom měli znát odpověď. Pokusím se opět o širší vysvětlení. Má platit v přístupu k vymoženostem zdravotní péče mezi občany rovnost bez jakýchkoliv výsad? Anebo připustíme, že „jsme si všichni rovni, ale někteří z nás rovnější“? Za jednu z kladných tradičních vlastností, kterými se kupodivu nevychloubáme, je vrozená demokratičnost – odpor k těm, kteří se vyvyšují a mají více privilegií (nejsem si jist, zda však nejde o druhou stranu mince, jejíž jednu stranu známe a vyznáváme se z ní – závist). Pokud ustoupíme od zásady rovnosti, musíme připustit i různou míru nehospodárnosti pro jednotlivé občany. Asi je pro společnost užitečné, poskytuje-li některým svým členům určité výhody oproti ostatním. Přijetí diferencovaného poskytování zdravotní péče však vede samozřejmě k nezbytnosti stanovit kritéria, jimiž se budeme řídit. Bude to množství peněz?Chceme pokroky medicíny?
Třetí a zcela základní otázkou je, zda připustíme, nebo dokonce budeme podporovat pokrok v lékařství. Ten totiž vede jak k dosahování lepších výsledků, tak k zvyšování nákladů. Pokusím se to ukázat na následujícím příkladu. Pravda je, že kdybychom se pokroku vzdali, mohli bychom ušetřit spoustu peněz, a to i těch, které vynakládáme na výzkum.Chronická myeloidní leukemie (CML)
Jde o klonální nádorové onemocnění krvetvorby, které vychází z kmenové buňky (Vesmír 71, 511, 1992/9) kostní dřeně a postihuje asi jednu až dvě osoby ze 100 000. Nejvíce postižených je mezi 45.–50. rokem věku, ale máme i dětské pacienty a starší nemocné. Když pacient přichází poprvé k lékaři s obtížemi, které jsou vyvolány rozvojem CML, nemusí být projevy nijak charakteristické, nemusí na tuto chorobu ukazovat.Klinickým vyšetřením lze zjistit zvětšenou slezinu a tento nález patří mezi první, pro které lze již do r. 1845 klást diagnostické ohraničení CML – leukemie se zvětšenou slezinou (splenic leukemia). Laboratorně obvykle nalezneme výrazný nadbytek bílých krvinek. Jejich počty se pohybují okolo 100 000–300 000 na 1 mm3 (u zdravých osob nacházíme hodnoty 5000–10 000). Buňky, které se tak nápadně rozmnožily, patří mezi neutrofilní leukocyty a jejich méně zralé formy. Jsou charakteristické výskytem chromozomální odchylky v podobě přítomnosti Ph-chromozomu. Tento nález, který laboratorní diagnostiku CML výrazně zdokonalil, pochází z r. 1960. Později se ukázalo, že jeho výskyt souvisí s chromozomální přestavbou – výměnou části chromozomu 22 s chromozomem 9. Výměna (translokace) postihuje dlouhá raménka těchto chromozomů a vzniká při ní fúzní gen bcr/abl (spojení částí dvou různých rozlomených genů). Součástí tohoto nově vzniklého genu je úsek genu bcr původně uloženého na chromozomu 22 a onkogenu abl z chromozomu 9. Tak se podařilo charakterizovat CML na molekulární úrovni, a dokonce i ověřit význam této genové fúze pro vznik onemocnění přenosem fúzovaného genu do myši, kde vyvolá stav podobný lidské CML. Zdá se, že se blížíme odpovědi na otázku, co vede nebo alespoň příspívá ke vzniku těchto zlomů a následných fúzí – mohly by to být určité repetitivní sekvence.
Terapie CML
Stejně jako diagnostika a vymezování CML se vyvíjela i léčba a její úspěšnost, která se hodnotí jak podle stavu pacienta, jeho případného zlepšení (dnes říkáme kvality života), tak podle délky trvání nemoci) od okamžiku rozpoznání do úmrtí). V tomto směru dosahujeme různé míry úspěšnosti. Ponechme stranou neúspěšnost, tedy situaci, kdy léčba nemá na průběh choroby ani stav pacienta žádný pozitivní vliv.K nejstarším pokusům o léčbu můžeme počítat podávání Solutio arsenicalis Fowleri (1860), jehož vliv na průběh choroby byl minimální nebo žádný.
Rentgenoterapie, která se začala používat počátkem našeho století, dokázala „normalizovat“ nebo spíše zlepšit stav pacienta, ale jen dočasně, a život nijak zvlášť neprodlužovala (bez léčení byla průměrná doba přežití 3 roky, při rentgenoterapii 3,5). Skutečná chemoterapie, namířená proti dělícím se buňkám, začala být hlavním léčebným prostředkem po druhé světové válce. Z té doby známe mnoho látek, z nichž některé se používají dodnes (busulfan – 1952, hydroxyurea – 1966). Ani chemoterapie však k zásadnímu prodloužení života nemocných nevedla. Za významný úspěch lze považovat až podávání interferonu α (1983), a zvláště pak transplantace kostní dřeně – nejdříve od příbuzných (1981) a později i nepříbuzných dárců (1985). Podávání interferonu (Vesmír 70, 596, 1991/10) může vést k zásadnímu prodloužení života za situace, kdy patologický proces je víceméně utlumen, ale jisté množství nádorových buněk v těle léčeného zůstává.
Transplantace kostní dřeně
Skutečného vyléčení lze zatím dosáhnout jen přenosem kostní dřeně ze zdravého dárce po vyhubení příjemcovy krvetvorby. Úplného úspěchu nedosáhneme vždy, u některých pacientů zůstává tzv. zbytková nemoc, protože se nám nepodaří odstranit všechny nádorové buňky. Do jisté míry se situace podobá stavu zdravých osob, protože některé nálezy ukazují, že jisté minimální množství buněk s fúzním genem bcr/abl lze nalézt i u nich, ovšem ve zcela nepatrném množství. Nicméně i takové pacienty je třeba trvale sledovat, abychom byli připraveni likvidovat přeživší buňky, které by se začaly množit. K tomu nám pomáhají molekulární diagnostické postupy rozeznávající (ve své nejcitlivější podobě) jednu leukemickou buňku mezi milionem zdravých.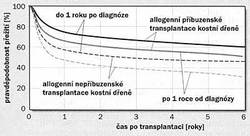 Za této nové situace můžeme odhalit obnovu množení nádorových buněk v době, kdy pacient ještě nemá žádné příznaky svědčící pro nový rozvoj choroby a kdy máme mnohem větší naději ji potlačit. Kdybychom mohli taková vyšetření provádět dostatečně často u „zdravých“ osob, přestalo by platit poněkud ironické tvrzení, že zdravý rovná se nedokonale vyšetřený, a mohli bychom odvrátit propuknutí mnoha chorob. Není vyloučeno, že k tomuto zatím nereálnému stavu dospějeme. Náznaky nových technologií tomu nasvědčují.
Za této nové situace můžeme odhalit obnovu množení nádorových buněk v době, kdy pacient ještě nemá žádné příznaky svědčící pro nový rozvoj choroby a kdy máme mnohem větší naději ji potlačit. Kdybychom mohli taková vyšetření provádět dostatečně často u „zdravých“ osob, přestalo by platit poněkud ironické tvrzení, že zdravý rovná se nedokonale vyšetřený, a mohli bychom odvrátit propuknutí mnoha chorob. Není vyloučeno, že k tomuto zatím nereálnému stavu dospějeme. Náznaky nových technologií tomu nasvědčují.
Stoupající náklady
Použijeme-li CML jako ukázku rozvoje medicíny během uplynulých sto let a minulé století přehlédneme jako nepodstatné, zjistíme, že úspěšnost léčby a diagnostické schopnosti neustále stoupají. Jestliže na začátku století přežívali pacienti v průměru 3 roky, je dnes průměrná doba přežití dvojnásobná a některé ze současných pacientů lze dokonce považovat za vyléčené. I u většiny pacientů, kteří nakonec nemoci stejně podlehnou, lze dosáhnout zásadního zlepšení stavu. Zdůrazňuji, že tyto úspěchy nejsou samozřejmé, dospěli jsme k nim po značném úsilí, které nebylo laciné. Relativně nejlevnějším způsobem léčby bylo ozařování v podobě užívané dříve. Chemoterapie náklady na léčbu příliš nezvýšila mimo jiné proto, že nebyla o mnoho účinnější než ozařování, a tedy nevedla k zásadnímu prodloužení délky života ani doby léčení. K podstatnému zvýšení nákladů vede až používání interferonu. Je to proto, že bývá dlouhodobé a cena léku je značně vysoká. Léčba interferonem (např. Roferonem A) stojí denně asi 735 Kč, měsíčně asi 22 000 Kč.Nejúspěšnější, ale také nejdražší je léčba transplantací. A to nejen pro sám přenos krvetvorných buněk, ale i pro vyšetření související s výběrem vhodného dárce a vzhledem k podpůrné léčbě nahrazující funkci krevních buněk v období vyřazení vlastní krvetvorby. Sem patří např. podávání krevních destiček transfuzí. Podáváním antibiotik se také musí nahradit potlačená obranyschopnost vůči infekcím. Velice přibližný odhad nákladů spojených s transplantací se pohybuje v našich zemích okolo 3 milionů Kč (v USA asi 150 000–200 000 amerických dolarů). Protože zatím nedokážeme docílit absolutní shodu plné vzájemné snášenlivosti mezi štěpem a jeho příjemcem, je součástí léčby po transplantaci podávání látek, které takové imunologické reakce tlumí (viz Vesmír 78, 92, 1999/2). Transplantace také vyžaduje zvláštní režim hospitalizace s vysokými nároky na kvalitu prostředí, v němž je pacient ošetřován.
Lékařova závislost na laboratorní diagnostice
V lékařské diagnostice obecně, a tedy i v případě CML, stoupá závislost lékaře na nejrůznějších přístrojích a laboratorních vyšetřeních. Získáváme tak stále více informací, které jsou jinak nedostupné. Vyšetřování nám nejprve pomáhá stanovit diagnózu – druh nemoci a její stadium – a posléze kontroluje její průběh včetně ověřování vlivu terapie. Počet vyšetření v průběhu poznávání choroby stále stoupá, a i když novější přístupy mohou někdy nahradit starší, není tomu tak vždy. Mikroskopická vyšetření buněk v krevním nátěru a zjištění jejich počtu provádíme stále, stejně jako vyšetření chromozomální, jimiž identifikujeme Ph-chromozom či další možné odchylky. V posledním desetiletí přibyla vyšetření molekulární, která diagnózu CML potvrdí nálezem fúzního genu bcr/abl (viz obrázky).Tato vyšetření, která nám poskytují jen část informací potřebných k léčení, provádíme nejen na počátku při stanovení diagnózy, ale opakujeme je i během léčby a v době, kdy je pacient bez klinických příznaků. Díky molekulárním metodám dokážeme odhalit jednu leukemickou buňku mezi milionem zdravých a zjistit, jak se počet leukemických buněk mění. Molekulárními metodami poznáme návrat onemocnění jinak nezachytitelný.
Nároky na množství vyšetření stoupají také v souvislosti s vývojem nových léčebných metod. Zavedení transplantací kostní dřeně vyvolalo potřebu výběru vhodného dárce z hlediska snášenlivosti tkání. Takové vyšetření se odvíjí od stanovení antigenní výbavy příjemce, pro něhož hledáme vhodného dárce. Čím vzácnější je kombinace příjemcových antigenů, tím nesnadnější je jeho nalezení a musíme vyšetřit větší počet možných dárců. Pokud není čtenáři cizí pojem polymerázové řetězové reakce (PCR; Vesmír 77, 444, 1998/8), pak k určení antigenní výbavy jedince je takových reakcí třeba provést několik desítek (pro každou antigenní jednotku jednu PCR), což podle sazebníku pojišťovny představuje 120 000–160 000 bodů. Vezmeme-li v úvahu množství dárců, které je třeba vyšetřit, abychom sestavili kompatibilní pár dárce-příjemce, dojdeme k počtu několika set takových reakcí a je zřejmé, že každé vyšetření, které není nezbytné, představuje neúčelně vynaložené prostředky. Na druhé straně každé vyšetření, které mohlo být pro pacientovo léčení užitečné a které nebylo provedeno, je možno kvalifikovat jako neposkytnutí potřebné péče.
Současný stav
Dnešní způsob léčení sleduje od okamžiku stanovení diagnózy dva hlavní cíle stejně jako dříve, nicméně s mnohem větším úspěchem. Především se snaží nemocného uzdravit (chorobný proces utlumit, zastavit, popřípadě odstranit) a zadruhé zbavit nemocného obtíží, které mu onemocnění působí. Druhá tendence byla relativně úspěšnější již od počátku století. Patří sem již tehdy používané ozařování a chemoterapie. Oba tyto prostředky tlumí především dělení buněk, bohužel však nejen „nemocných“, ale i zdravých, a proto je nelze používat dlouhodobě. Nemůžeme překročit míru, kterou by pacient nepřežil, a často se pohybujeme po ostří nože. Použití interferonu chorobný proces tlumí, ani to však nemoc neodstraňuje. Na rozdíl od ozařování a chemoterapie lze interferon, jestliže ho pacient snáší, podávat i po několik let. Léčením, které může vést ke skutečnému uzdravení, je zatím jen transplantace kostní dřeně. Podle dostupnosti dárce a s tím spojené kvality vztahu mezi dárcem a příjemcem rozdělujeme transplantace na autologní (použita je vlastní dřeň nemocného) a allogenní (použita je dřeň jiné osoby), které ještě dělíme na příbuzenské a nepříbuzenské. Autologní transplantace se hodí spíše k léčení jiných typů nádorů a nebudeme se jimi zabývat.Úspěšnost transplantace, tj. nahrazení krvetvorby příjemce (nemocného) krvetvorbou dárce (zdravého), se pohybuje mezi 60–80 % a závisí na dalších okolnostech, např. věku nemocného, jeho stavu v době transplantace, stupni vývoje původního onemocnění ad. Pokud pacient nemá sourozence, rodiče, děti ani další příbuzné, kteří jsou s ním z tohoto hlediska shodní, musí se hledat mezi nepříbuznými dárci. Úspěšnost transplantace kostní dřeně od nepříbuzného dárce je poněkud nižší, asi 50 %. Patrně to souvisí s tím, že svou roli hrají i další geny, které vyšetřením nepostihneme. Výběr pacientů pro transplantaci by při použití stroze ekonomického hlediska bral ohled jen na výši pravděpodobnosti úspěšnosti.
Řada lidí je ochotna darovat i kostní dřeň a existují registry, podle nichž lze vhodného dárce vybrat. Počet registrů dárců by měl být úměrný počtu evidovaných dárců a v tomto směru je výhodnější mít méně registrů s velkým počtem dárců. Tak je tomu ve vyspělých státech, kde si na ekonomické pohledy ve zdravotnictví již navykli. Roku 1997 bylo ve světě registrováno 13 500 příbuzenských transplantací a 3500 nepříbuzenských. Většinou šlo o pacienty s různými typy leukemií, přičemž u nás, tj. v Ústavu hematologie a krevní transfuze, bylo od první transplantace v r. 1986 provedeno celkem 163 transplantací, z toho 35 nepříbuzenských.
Vezmeme-li v úvahu počty transplantačních center, kterých jen Evropě bylo r. 1997 kolem 200, nejsou naše aktivity zanedbatelné (např. Itálie jich má 57, Velká Británie 42, Německo 41, Francie 35, Holandsko 16, Belgie 12, Rakousko 11, Polsko 8, Řecko 5, Česká republika 5, Finsko 4, Portugalsko 4, Dánsko 3, Chorvatsko 2, Maďarsko 2, Norsko 2) a s přihlédnutím k počtu obyvatel se do Evropy docela hodíme. 1)
Poznámky
Ke stažení
 Článek ve formátu PDF [179,51 kB]
Článek ve formátu PDF [179,51 kB]



















