Jak mozek přivyká (a odvyká) morfinu
| 31. 5. 2018Drogová závislost je již řadu let řazena mezi chronická onemocnění centrální nervové soustavy. K poznání mechanismu vzniku závislosti a adaptace mozku na morfin slouží i studium souboru bílkovin proteomika.
Morfin je součástí opia, které se získává z pryskyřice máku setého (Papaver somniferum). Poprvé jej izoloval německý lékárník Sertürner v prvním desetiletí 19. století. Substanci pojmenoval podle řeckého boha snů Morfea.
Tento opiát je znám pro své tišící účinky, tlumí i silnou akutní a chronickou bolest. Při jeho opakovaném podání se však účinnost snižuje a pro dosažení stejného efektu je třeba zvýšit přísun drogy.
Na tento jev se můžeme dívat jako na mechanismus působící proti účinku drogy anebo také jako na projev určité biologické adaptace organismu. Mozek se přizpůsobuje opakovanému užití narkotika a nastoluje se forma jakési vnitřní rovnováhy, pro jejíž udržení se musí droga stále dodávat. Její vysazení doprovází nepříjemné abstinenční příznaky.
Obnova původního stavu před podáním drogy je velmi obtížná, ale ne nemožná…
Závislí potkani
Problematikou dlouhodobé adaptace mozku na morfin se zabývá i laboratoř Biochemie membránových receptorů ve Fyziologickém ústavu AV ČR. Komunikace mezi buňkou a okolím se uskutečňuje pomocí specifických bílkovin (membránových receptorů) fungujících jako přijímače signálu z vnějšího prostředí, které jej umí přenést do nitra buňky a vyvolat biologickou odpověď. Fyziologický účinek morfinu vzniká po vazbě na opioidní receptory nacházející se především v mozku.
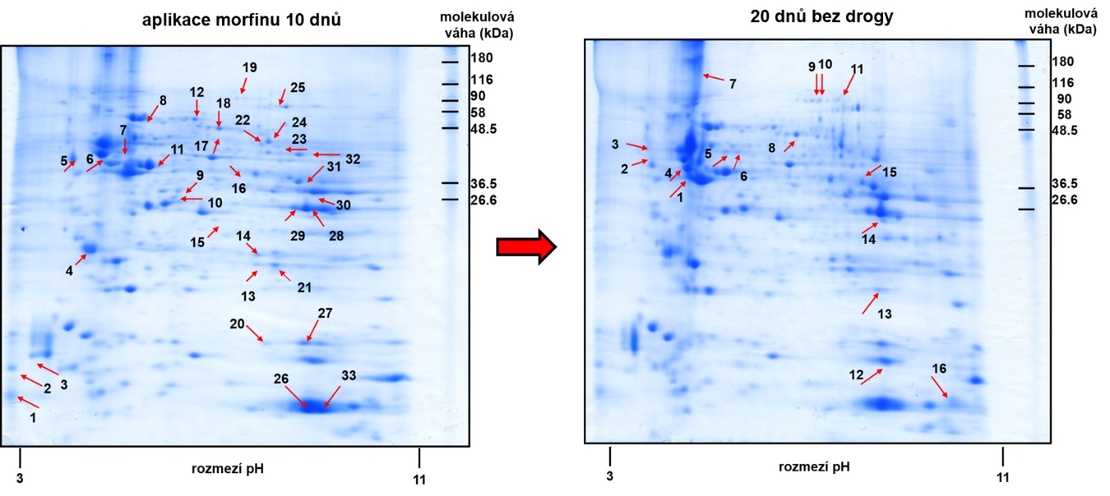
Jako objekt studia nám slouží laboratorní potkani Wistar, kterým aplikujeme po deset dnů zvyšující se dávky morfinu podle následujícího schématu: 10 mg/kg (den 1. a 2.), 15 mg/kg (den 3. a 4.), 20 mg/kg (den 5. a 6.), 30 mg/kg (den 7. a 8.) a 40 mg/kg (den 9. a 10.). Po deseti dnech s drogou sledujeme spektrum změněných bílkovin (proteinů) v přední mozkové kůře potkanů, zároveň nás zajímá, zda je možné pozorovat schopnost návratu k původnímu stavu organismu po dalších dvaceti dnech života bez drogy.
Svým způsobem se pro nás tato druhá skupina dvacetidenních abstinentů stává atraktivnější, protože existuje řada studií zaměřených na dlouhodobé působení morfinu, málo se však ví o stavu po vysazení drogy.
Abychom měli představu, které bílkoviny se vlivem morfinu mění, jak moc je tato změna velká a zda přetrvává i po dvaceti dnech od poslední dávky, využíváme proteomické metody.
Co je to proteomika?
Proteomika se snaží zmapovat kompletní sadu bílkovin v buňce či tkáních při různých fyziologických a patologických stavech organismu. Jednou z metod, při níž je možné rozdělit složité směsi bílkovin, je dvojrozměrná elektroforéza. Jak už vypovídá název, dělení bílkovin se děje ve dvou rozměrech: nejprve podle náboje a poté podle velikosti. První krok probíhá na speciálním proužku gelu s vytvořeným rozmezím pH, na který se nanáší směs bílkovin. Označujeme jej jako izoelektrickou fokusaci (zaostření), děj, při němž bílkoviny putují v rozmezí pH ve směru zleva doprava a zastaví se (zaostří) v místě, ve kterém je jejich celkový náboj roven nule. V druhé fázi se pak tento proužek položí na gel a dělení probíhá podle molekulové váhy bílkovin ve směru seshora dolů. Získáme tak proteinovou mapu, která v ideálním případě vypadá jako hvězdná obloha. Mohou na ní být až tisíce různých bílkovin v podobě kulatých skvrn (spotů). Abychom je však uviděli, musíme gel s mapou obarvit (v našem experimentu jsme zvolili modré barvení).
Mozaiku experimentu pak doplňuje analýza proteinových map. Používají se hodnotící programy porovnávající intenzitu skvrn mezi srovnávanými vzorky. Výrazně odlišné skvrny můžeme z gelu jednoduše vyříznout skalpelem. Finále pokusu pak představuje identifikace proteinů, pro niž využíváme služeb hmotnostní spektrometrie. V současné době se v proteomice stále více uplatňují i negelové metody. Vycházejí ze skutečnosti, že hmotnostní spektrometrie umožňuje kvalitativní i kvantitativní analýzu tisíců různých proteinů. Gelový i negelový proteomický přístup má svá pro i proti, pokud ale využijeme informace získané z obou z nich, můžeme si vytvořit komplexnější přehled o zkoumané problematice.
Co vyčteme z proteinů
Co můžeme přečíst z proteinového profilu závislých potkanů a dvacetidenních abstinentů? Červené šipky na obrázku označují výrazně odlišné skvrny, které jsme vyřízli z gelu pro jejich určení (obě skupiny byly srovnávány s příslušnými kontrolními potkany). U závislých potkanů jsme identifikovali 33 bílkovin, řada z nich byla spojena především se změnou celkového energetického metabolismu. Aktivace opioidních receptorů dávkami morfinu je totiž energeticky náročný proces. Dále se například zvýšila hladina proteinů oxidačního stresu souvisejícím s produkcí volných radikálů, které mají nepříjemnou schopnost poškozovat buňky či tkáně. Za zmínku stojí i vzestup bílkovin cytoskeletu (sítě vláken zajišťujících pohyb a tvar buňky) signalizující přestavbu neuronální sítě v mozku. Vysoká pružnost centrální nervové soustavy, schopnost detekovat nové děje a správně na ně reagovat, je důležitou podmínkou přežití v měnícím se prostředí. Hlavním a snad i pozitivním zjištěním však je, že se počet takovýchto změn po dvaceti dnech od poslední dávky morfinu snížil z 33 na 16. Zdá se tedy, že živý organismus má po vysazení drogy výraznou schopnost návratu k původnímu stavu.
K dalšímu čtení: Ujcikova et al.: J Proteomics, DOI: 10.1016/j.jprot.2016.02.019
O autorovi
Hana Ujčíková