Přečtené genomy – a co dál?
 Anton Markoš na konci svého článku o genomech (Vesmír 75, 685, 1996/12) nadhodil míč diskuse po nahrávce Jamese Lovelocka tak provokativně, že nelze než pokračovat ve hře, anebo odejít ze hřiště a nechat jej potupně spadnout na hlavy všech těch biologů, kteří, jak říká, „tři sta let vypracovávali seznamy živých tvorů a dnes se pouštějí do výroby nových nekonečných telefonních seznamů za pomoci metody sekvencování“. Znamená toto snažení, že jim opět nevybude čas na zodpovězení zásadní otázky „Co je život?“, anebo je všechno jinak? Hrajme však uvážlivě, protože publikum, které vydláždilo hřiště zdánlivě obrovskými finančními prostředky, nečeká tentokrát ani tak na iluzi napínavé hry, jako spíše na chléb praktických uspokojení.
Anton Markoš na konci svého článku o genomech (Vesmír 75, 685, 1996/12) nadhodil míč diskuse po nahrávce Jamese Lovelocka tak provokativně, že nelze než pokračovat ve hře, anebo odejít ze hřiště a nechat jej potupně spadnout na hlavy všech těch biologů, kteří, jak říká, „tři sta let vypracovávali seznamy živých tvorů a dnes se pouštějí do výroby nových nekonečných telefonních seznamů za pomoci metody sekvencování“. Znamená toto snažení, že jim opět nevybude čas na zodpovězení zásadní otázky „Co je život?“, anebo je všechno jinak? Hrajme však uvážlivě, protože publikum, které vydláždilo hřiště zdánlivě obrovskými finančními prostředky, nečeká tentokrát ani tak na iluzi napínavé hry, jako spíše na chléb praktických uspokojení.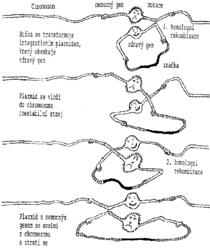
Historie a filozofie nás přesvědčují, že existují nejméně dvě krajní cesty, které míří někam za horizont současného stavu vědeckého poznání. První sleduje směr, v němž rozhodujícím hlediskem jsou konkrétní souvislosti mezi jednotlivými konkrétními jevy. Ta druhá pramení ze zkušenosti, že všechno víceméně souvisí se vším. Když se podíváme z náležitého odstupu, abychom mohli přehlédnout větší celek, první cesta se může zdánlivě proměnit v nedokonalou pěšinu s malichernými zákruty. Pokusy o celostní pohled bývají zase mlhavé. To platí i o Lovelockově knize „Gaia – živá planeta“.  Analýza jednotlivostí se postupně skládá do ostře konturovaných větších celků, ale skutečnost může být mnohem složitější, protože řada „méně významných vlivů“ byla dočasně opomenuta, nebo dokonce vědomě zanedbána. Sekvencování genomů nesporně směřuje k poznání životních procesů právě touto dočasně redukcionistickou cestou; je dílčím cílem, o kterém se ví, že bude překročen dříve, než se telefonní seznam naplní údaji o všech účastnících sítě. Vždyť ani úplný seznam nemůže odpovědět na zásadní otázku o životě, protože se zaměřuje jen na jednu z mnoha stránek tohoto jevu. Sekvencování se týká dědičných dispozic, o jejichž projevu v celkové harmonii nemáme zatím jasnou představu ani u těch modelových organizmů, jejichž genom byl již opsán. Jak ale uvažovat o poselství určité genomové knihy, když jsme ji nepřečetli?
Analýza jednotlivostí se postupně skládá do ostře konturovaných větších celků, ale skutečnost může být mnohem složitější, protože řada „méně významných vlivů“ byla dočasně opomenuta, nebo dokonce vědomě zanedbána. Sekvencování genomů nesporně směřuje k poznání životních procesů právě touto dočasně redukcionistickou cestou; je dílčím cílem, o kterém se ví, že bude překročen dříve, než se telefonní seznam naplní údaji o všech účastnících sítě. Vždyť ani úplný seznam nemůže odpovědět na zásadní otázku o životě, protože se zaměřuje jen na jednu z mnoha stránek tohoto jevu. Sekvencování se týká dědičných dispozic, o jejichž projevu v celkové harmonii nemáme zatím jasnou představu ani u těch modelových organizmů, jejichž genom byl již opsán. Jak ale uvažovat o poselství určité genomové knihy, když jsme ji nepřečetli?
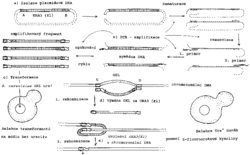 Když jsem loni dopisoval svůj aprílový manifest na obranu pekařské kvasinky (Vesmír 75, 226, 1996/4), netušil jsem, že tak záhy ke všem mým chvalozpěvům na tuto reprezentantku eukaryotických organizmů, ke kterým se hrdě hlásí i příslušníci druhu Homo sapiens, přibude ještě jeden, ten nejvýznamnější pro tuto diskusi. V dubnu 1996 byla zveřejněna publikace o 16 poměrně krátkých kapitolách (co chromozom, to kapitola). Na vytištění této zprávy se spotřebovalo celkem asi 12 milionů písmenek A, C, G a T. Šlo o sekvenci nukleotidů v genomové DNA u prvního eukaryotického organizmu kvasinky Saccharomyces cerevisiae.
Když jsem loni dopisoval svůj aprílový manifest na obranu pekařské kvasinky (Vesmír 75, 226, 1996/4), netušil jsem, že tak záhy ke všem mým chvalozpěvům na tuto reprezentantku eukaryotických organizmů, ke kterým se hrdě hlásí i příslušníci druhu Homo sapiens, přibude ještě jeden, ten nejvýznamnější pro tuto diskusi. V dubnu 1996 byla zveřejněna publikace o 16 poměrně krátkých kapitolách (co chromozom, to kapitola). Na vytištění této zprávy se spotřebovalo celkem asi 12 milionů písmenek A, C, G a T. Šlo o sekvenci nukleotidů v genomové DNA u prvního eukaryotického organizmu kvasinky Saccharomyces cerevisiae. Protože se počet úhozů v „Obyčejném životě“ od Karla Čapka do kvasinkového genomu vejde asi šestačtyřicetkrát, lze předpokládat, že život kvasinky nemůže být až tak obyčejný. V genomové knížce o S. cerevisiae se ukrývá na 5 885 genů kódujících proteiny, 140 genů pro rRNA, 40 genů pro malé jaderné RNA a 275 genů pro tRNA. To znamená, že jeden gen připadá asi na 2 Kbp. Kvasinkový genom je ve srovnání s lidským genomem zahuštěnější. U lidí, jejichž genom je asi 300krát větší, připadá gen na 30 Kbp. Počítačová srovnávací analýza genů kvasinky s geny, jejichž funkce byla již určena, dovolila načrtnout předběžný obraz dělby práce mezi proteiny kvasinky (tab. I). Dokonce se podařilo na základě homologie objevit i proteiny, o jejichž existenci se u S. cerevisiae doposud pochybovalo, např. histon H1. Další dobrou zprávu přineslo zjištění, že většina sekvencí odpovídajících genům u S. cerevisiae má své homology v genomu poměrně vzdálené příbuzné houby Ashbya gassypii, a navíc alespoň čtvrtina klonů genomové knihovny této houby obsahuje páry, nebo dokonce celé skupiny genů kvasinky ve stejném pořadí a vzájemné orientaci. Jaký příslib úspory pro sekvencování „příbuzných“!
Protože se počet úhozů v „Obyčejném životě“ od Karla Čapka do kvasinkového genomu vejde asi šestačtyřicetkrát, lze předpokládat, že život kvasinky nemůže být až tak obyčejný. V genomové knížce o S. cerevisiae se ukrývá na 5 885 genů kódujících proteiny, 140 genů pro rRNA, 40 genů pro malé jaderné RNA a 275 genů pro tRNA. To znamená, že jeden gen připadá asi na 2 Kbp. Kvasinkový genom je ve srovnání s lidským genomem zahuštěnější. U lidí, jejichž genom je asi 300krát větší, připadá gen na 30 Kbp. Počítačová srovnávací analýza genů kvasinky s geny, jejichž funkce byla již určena, dovolila načrtnout předběžný obraz dělby práce mezi proteiny kvasinky (tab. I). Dokonce se podařilo na základě homologie objevit i proteiny, o jejichž existenci se u S. cerevisiae doposud pochybovalo, např. histon H1. Další dobrou zprávu přineslo zjištění, že většina sekvencí odpovídajících genům u S. cerevisiae má své homology v genomu poměrně vzdálené příbuzné houby Ashbya gassypii, a navíc alespoň čtvrtina klonů genomové knihovny této houby obsahuje páry, nebo dokonce celé skupiny genů kvasinky ve stejném pořadí a vzájemné orientaci. Jaký příslib úspory pro sekvencování „příbuzných“!
S. cerevisiae je výjimečným modelem nejen svou jednoduchostí, snadnou experimentální ovladatelností, rychlostí růstu a bohatou minulostí poznávání tohoto věrného souputníka lidí, který nás zásobuje něžně nakypřenými těsty, různými alkoholickými nápoji a v současné době i našimi vlastními proteiny (obrázek). Pekařská kvasinka je navíc vzácně odlišná v jedné obdivuhodné vlastnosti. Má oproti vyšším organizmům neobyčejně výkonnou homologní rekombinaci. Právě tato schopnost, která u S. cerevisiae nápadně převládá nad všemi dalšími způsoby rekombinace, umožnila, že zdánlivě nemožné se u kvasinek již stalo skutkem. Léčení genetických poruch, které je snem lidských genetiků, lze u kvasinek uskutečnit poměrně snadno (obr. obrázek). Tento postup však funguje i obráceně. Původní nepoškozený gen lze nahradit genem, který je definovaným způsobem in vitro pozměněn. V krajním případě lze vybraný gen z chromozomu zcela odstranit (obr. obrázek). Když zmizí gen, zmizí i jeho funkce, a to se projeví navenek změnou vlastností studovaného mutanta. Delece nebo změna jednotlivých genů je základem pro systematickou funkční analýzu jejich uplatnění v genomu. Tato cesta také vede k údajům o funkci jednotlivých proteinů  kvasinkového proteomu. Ztráta genu totiž způsobí vymizení proteinové skvrny na dvojrozměrném elektroforetogramu buněčných proteinů a to je způsob, jak skvrny proteinů přiřadit genům, které je kódují. Izolace a charakterizace struktury a funkce jednotlivých proteinů dovrší cestu, kterou se ubírá analýza proteomu. Pekařská kvasinka se díky ojedinělým možnostem funkční analýzy genomu pomocí cílené mutageneze stává trojským koněm pro vstup do postgenomové éry.
kvasinkového proteomu. Ztráta genu totiž způsobí vymizení proteinové skvrny na dvojrozměrném elektroforetogramu buněčných proteinů a to je způsob, jak skvrny proteinů přiřadit genům, které je kódují. Izolace a charakterizace struktury a funkce jednotlivých proteinů dovrší cestu, kterou se ubírá analýza proteomu. Pekařská kvasinka se díky ojedinělým možnostem funkční analýzy genomu pomocí cílené mutageneze stává trojským koněm pro vstup do postgenomové éry.
Roku 1996 vznikl EUROFAN, nová informační síť zaměřená na funkční analýzu nových kvasinkových genů. Kvasinkáři prosazují nový obří projekt „Kvasinkový proteom“. Všechny tyto aktivity potvrzují, že výzkum S. cerevisiae již do postgenomové éry zcela vážně vykročil.
 Píše se rok 2005. Databáze se prohýbají informacemi o sekvencích genomů mnoha virů a řady prokaryotických organizmů. Přibývají informace o modelových eukaryotických genomech. Projekt „Lidský genom“ je dokončen a projekt „Kvasinkový proteom“ je již také za svým zenitem. Generace dětí odkojených v „Legolandu“ a později vytrénovaných pro bezpečnou jízdu na informačních dálnicích počítačových sítí dorostla, dožaduje se chleba a vymýšlí nové hry. Zobrazovací techniky umožňují pohyb ve virtuální realitě modelů proteinových molekul. Roubování proteinových domén a sestavování nadmolekulárních útvarů v tomto prostoru umožňuje cvičně testovat různé nové funkční celky. Iracionální strach z genových úprav již nepřipomíná hrůzu pračlověka z plamenů keře zapáleného bleskem. Přetrvává již jen přiměřený respekt a zodpovědný přístup k realizaci jednotlivých projektů. V laboratořích genových inženýrů se systematicky pracuje s „legotvárnicemi“ reálných genových a proteinových fragmentů. Molekulární genetika je v pokročilém stadiu těhotenství. Očekává se zrození odpovědí na řadu globálních otázek
Píše se rok 2005. Databáze se prohýbají informacemi o sekvencích genomů mnoha virů a řady prokaryotických organizmů. Přibývají informace o modelových eukaryotických genomech. Projekt „Lidský genom“ je dokončen a projekt „Kvasinkový proteom“ je již také za svým zenitem. Generace dětí odkojených v „Legolandu“ a později vytrénovaných pro bezpečnou jízdu na informačních dálnicích počítačových sítí dorostla, dožaduje se chleba a vymýšlí nové hry. Zobrazovací techniky umožňují pohyb ve virtuální realitě modelů proteinových molekul. Roubování proteinových domén a sestavování nadmolekulárních útvarů v tomto prostoru umožňuje cvičně testovat různé nové funkční celky. Iracionální strach z genových úprav již nepřipomíná hrůzu pračlověka z plamenů keře zapáleného bleskem. Přetrvává již jen přiměřený respekt a zodpovědný přístup k realizaci jednotlivých projektů. V laboratořích genových inženýrů se systematicky pracuje s „legotvárnicemi“ reálných genových a proteinových fragmentů. Molekulární genetika je v pokročilém stadiu těhotenství. Očekává se zrození odpovědí na řadu globálních otázek

Rýsuje se představa o vzniku jakési „tabulky“ funkčních proteinových podjednotek a nukleotidových boxů, které by umožnily odvozovat vlastnosti složených celků (proteinů, regulačních sekvencí v DNA) z vlastností a způsobu propojení podjednotek podobně, jako svého času Mendělejevova tabulka projasnila pochopení chemických vlastností anorganických sloučenin vzniklých spojováním atomů prvků.
Tyto výsledky kolektivní činnosti biologů, které přinášejí zjevně i ovoce praktických aplikací, přesvědčily veřejnost, že vložené investice do této cesty odstartované sekvencováním genomů jsou vratné. Je totiž jasné, že právě genomová sekvence, skladba proteomů a časové rozvrhy řízené transkripce vytvářejí základ pro fundované úvahy o koordinaci, vývoji a provádění komplexních procesů, které skládají život. Diskuse o tom, zda je tato cesta jediná, stále neumlkly. A to je dobře, i když téměř každý již ví, že jediná není. Některé skutečnosti je třeba si připomínat stále znova.
O autorovi
Vladimír Vondrejs





















