Molekulární genetika regulace krevního tlaku
Esenciální hypertenze je vysoký krevní tlak neznámého původu (pozn. red.: esenciální – zde ve významu „nevzniklý jako následek jiné choroby“). Bývá jedním z hlavních rizikových faktorů mozkové mrtvice, infarktu myokardu a selhání ledvin. Krevní tlak je regulován několika vzájemně propojenými systémy, z nichž každý má svou speciální funkci. Lze je zhruba rozdělit na ty, které působí velmi rychle (většinou jde o nervové reflexy, jejichž cílem je např. rychlé zvýšení krevního tlaku při velkém krvácení), a na dlouhodobě účinkující systémy (ty regulují krevní tlak v intervalu měsíců či let). Mezi dlouhodobě účinkujícími faktory hraje dominantní roli krevní objem (přesněji jeho plazmatická část): dlouhodobě se krevní tlak může ustálit pouze na hodnotě, při níž je krevní objem stabilní. Předpokládá se, že právě změny krevního objemu, regulované především vylučováním soli a vody ledvinami, by mohly být nejzávažnějšími příčinami esenciální hypertenze. Schematicky lze kontrolu krevního objemu popsat takto:
- zvýšený krevní objem zvýší množství krve pumpované srdcem,
- zvýšený srdeční výdej zvýší krevní tlak,
- zvýšený krevní tlak zvýší vylučování tekutin a soli ledvinami.
 Ledviny pacientů s esenciální hypertenzí obvykle při normálně vysokém krevním tlaku nejsou schopny vyloučit odpovídající množství vody a soli. Proměnlivost krevního tlaku je podmíněna řadou faktorů prostředí, demografickými faktory (ekonomickými podmínkami a celkovým způsobem života) a do značné míry i geneticky. Ukázalo se to například při srovnání krevních tlaků jednovaječných a dvouvaječných dvojčat. Z epidemiologických studií také vyplynulo, že pro některé rodiny je výskyt vysokého tlaku charakteristický. Toto zjištění dalo podnět k výzkumu genetických faktorů, které jsou za esenciální hypertenzi odpovědné. Jejich identifikace je však nesmírně složitá (viz Vesmír 74, 485, 1995/9). Jako první proto nebyly detegovány geny odpovědné za esenciální hypertenzi, ale geny, které jsou spojovány s monogenně podmíněnými poruchami regulace krevního tlaku. Je to tím, že jejich účinek je podstatně výraznější. V tabulce na této straně jsou uvedeny geny podmiňující dosud popsané syndromy poruch regulace krevního tlaku. Ve všech případech jde o poruchy ve vylučování sodíku ledvinami, způsobené buď abnormální sekrecí aldosteronu, nebo změněnou aktivitou přenašečů (kotransportérů) sodíku či sodíkových kanálů v ledvinách. Všechny patofyziologické fenotypy těchto syndromů lze odvodit od výše zmíněných mutací.
Ledviny pacientů s esenciální hypertenzí obvykle při normálně vysokém krevním tlaku nejsou schopny vyloučit odpovídající množství vody a soli. Proměnlivost krevního tlaku je podmíněna řadou faktorů prostředí, demografickými faktory (ekonomickými podmínkami a celkovým způsobem života) a do značné míry i geneticky. Ukázalo se to například při srovnání krevních tlaků jednovaječných a dvouvaječných dvojčat. Z epidemiologických studií také vyplynulo, že pro některé rodiny je výskyt vysokého tlaku charakteristický. Toto zjištění dalo podnět k výzkumu genetických faktorů, které jsou za esenciální hypertenzi odpovědné. Jejich identifikace je však nesmírně složitá (viz Vesmír 74, 485, 1995/9). Jako první proto nebyly detegovány geny odpovědné za esenciální hypertenzi, ale geny, které jsou spojovány s monogenně podmíněnými poruchami regulace krevního tlaku. Je to tím, že jejich účinek je podstatně výraznější. V tabulce na této straně jsou uvedeny geny podmiňující dosud popsané syndromy poruch regulace krevního tlaku. Ve všech případech jde o poruchy ve vylučování sodíku ledvinami, způsobené buď abnormální sekrecí aldosteronu, nebo změněnou aktivitou přenašečů (kotransportérů) sodíku či sodíkových kanálů v ledvinách. Všechny patofyziologické fenotypy těchto syndromů lze odvodit od výše zmíněných mutací.
Aldosteronizmus
Jde o nadměrné tvoření hormonu aldosteronu v kůře nadledvin. Tato porucha, léčitelná glukokortikoidy, je dědičná a projevuje se vrozeným vysokým tlakem. U zdravého člověka se aldosteron vylučuje ve vnější vrstvě (zona glomerulosa) kůry nadledvin pod kontrolou angiotenzinu II. Aldosteron aktivuje vstřebávání vody a soli v ledvinných trubičkách (tubulech). Syntéza 11-deoxykortokosteronu (DOC) je katalyzována týmiž enzymy ve vnější vrstvě i uvnitř. DOC je pak přeměněn na mineralokortikoidy ve vnější vrstvě a na glukokortikoidy ve vrstvách vnitřních, a to prostřednictvím exprese dvou enzymů, 11β-hydroxylázy a aldosteronsyntázy. Genetické analýzy rodin s postiženými jedinci odhalily asociaci mezi tímto onemocněním a dvěma geny na 8. chromozomu: 11β-hydroxylázou a aldosteronsyntázou. Chromozomy všech dosud studovaných jedinců postižených aldosteronizmem nesly normální geny kódující aldosteronsyntázu a 11β-hydroxylázu, avšak navíc obsahovaly i nové geny, které zdraví jedinci neměli. Tyto nové geny vznikly spojením regulačních sekvencí 11β-hydroxylázy s kódující sekvencí aldosteronsyntázy. Výsledkem je abnormální sekrece aldosteronu, která vede k zvýšenému zpětnému vstřebávání soli a vody, k expanzi plazmatického objemu, a nakonec k zvýšení krevního tlaku.Liddlův syndrom
Podobně jako při aldosteronizmu mají i pacienti s Liddlovým syndromem vysoký krevní tlak již v mládí a rovněž zvýšené vstřebávání soli a vody v ledvinách. Vazebné studie umožnily lokalizovat gen odpovědný za Liddlův syndrom do krátkého segmentu 16. chromozomu, do blízkosti dvou genů, které kódují podjednotky β a γ epiteliálního sodíkového kanálu. Vstřebávání sodíku tímto kanálem je regulováno především hormonem aldosteronem. Sekvenace zmíněných genů u pacientů s Liddlovým syndromem odhalily mutace v genech kódujících obojí podjednotky kanálu (β i γ). Aktivita těchto mutovaných genů se testovala v žabích oocytech, přičemž byla pozorována výrazně vyšší aktivita sodíkového kanálu. U pacientů s Liddlovým syndromem pak tato vyšší aktivita vede k zvýšenému vstřebávání sodíku v ledvinách, a tedy opět k vysokému tlaku.Pseudohypoaldosteronizmus typu I
Jde o onemocnění charakteristické drastickou dehydratací u postižených novorozenců, poklesem tlaku, nadměrným vylučováním sodíku, zvýšenými hladinami sérového draslíku, zvýšenou metabolickou kyselostí, zvýšenou aktivitou plazmatického reninu a hladiny hormonu kůry nadledvin – aldosteronu. Genetická analýza rodin, v nichž se onemocnění vyskytlo, umožnila zmapovat odpovědné geny do krátkého segmentu 16. chromozomu, který obsahuje podjednotky β i γ epiteliálního sodíkového kanálu.Sekvenace obou genů z DNA izolované od jedinců se zmíněnou poruchou odhalily mutace, které vedou ke ztrátě funkce genů buď pro β, nebo pro γ podjednotku epiteliálního sodíkového kanálu. Následkem je velká ztráta sodíku ledvinami, spojená s druhotnými poruchami při vylučování draselných a vodíkových iontů. Tím vzroste aktivita systému renin-angiotenzin, avšak vstřebávání sodíku nemůže být zvýšeno, protože sodíkový kanál je defektní.
Gitelmanův syndrom
Jde o alkalózu (zvýšený výskyt zásaditých látek) spojenou s abnormálními ztrátami soli ledvinami a s poklesem tlaku. První příznaky se objevují brzy po dosažení dospělosti a nápadně se podobají abnormalitám pozorovaným po podání thiazidových močopudných látek, které inhibují NaCl kotransportér, kódovaný genem SLC12A3. Zkoumáním několika rodin trpících Gitelmanovým syndromem byla zjištěna souvislost syndromu s tímto genem na 16. chromozomu. Sekvencováním genu SLC12A3 u postižených jedinců pak byla odhalena řada mutací způsobujících defektní vstřebávání iontů sodíku a chloru v tubulech nefronů.Tři typy Bartterova syndromu
- Typ I: Klinické příznaky postižených jedinců zahrnují dehydrataci, snížený krevní tlak, křeče, svalovou ochablost, u těžce postižených dětí může dojít k poruchám růstu a k mentální retardaci. Na základě studií pacientů s tímto syndromem byla vyslovena hypotéza, že jde o poruchu vstřebávání sodíku v tlusté části vzestupného raménka Henleovy kličky. U postižených ze všech vyšetřovaných rodin pak sekvenační analýza odhalila mutantní alely genu SLC12A1. Všechny mutace způsobovaly změnu kódovaného proteinu odpovědného za vstřebávání sodíku a ztrátu jeho funkce.
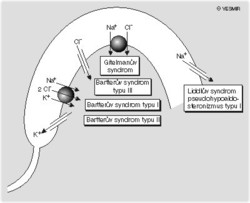
- Typ II: Při vyšetřování dalších rodin s Bartterovým syndromem byla zjištěna vazba mezi klinickými příznaky a genem KCNJ1 na 11. chromozomu, kódujícím draslíkový kanál, který recykluje vstřebaný draslík a tím řídí aktivitu genu SLC12A1 (viz obrázek). Sekvenační analýzy genu KCNJ1, izolovaného z DNA postižených, odhalily mutace odpovědné za podstatnou změnu struktury kanálu, jež vede ke ztrátě jeho funkce.
- Typ III: Mezi vyšetřovanými rodinami s příznaky Bartterova syndromu byly i takové, kde se při genetických analýzách v genech SLC12A1 a KCNJ1 nenašly žádné mutace. Vazebné studie pak prokázaly souvislost tohoto typu Bartterova syndromu s geny CLCNKA a CLCNKB na 1. chromozomu. Tyto těsně svázané geny kódují kanály, které zprostředkují vstřebávání chloridových iontů přes membrány ledvinných buněk a ovlivňují tak aktivitu genu SLC12A1 (viz obrázek). Sekvenační analýzy odhalily řadu bodových mutací a také rozsáhlých ztrát úseků genu CLCNKB.
Esenciální hypertenze
Rozsáhlé studie označily několik genů, které by mohly vysoký tlak dosud neznámého původu ovlivňovat: jde například o geny pro enzym renin, pro antigeny hlavního histokompatibilního komplexu, inzulinový receptor, angiotenzinogen a jiné. U žádného z výše zmíněných genů však nebyly nalezeny mutace, které by vysoký tlak jednoznačně podmiňovaly. U pacientů s esenciální hypertenzí se nenašly ani mutace genů, které podmiňují výše popsané syndromy. Srovnávací genetické analýzy se zvířecími modely (viz rámeček 1 ) navíc potvrdily, že tyto geny nejsou mutovány ani u potkanů s experimentální hypertenzí, snad s výjimkou mutací genu pro 11β-hydroxylázu u kmene SR (viz rámeček 1 ). V tomto případě rozdílné mutace homologních genů mají na regulaci krevního tlaku odlišný vliv, u lidí způsobují vysoký tlak (aldosteronizmus léčitelný glukokortikoidy), u potkanů neobvyklou odolnost vůči soli v potravě. Geny odpovědné za esenciální hypertenzi tedy zatím odhaleny nebyly. Při pátrání po nich se zdá být nejlepším způsobem paralelní výzkum lidského genomu a genomu vybraných modelových organizmů. 1)Poznámky
Srovnávací analýzy se zvířecími modely
- Geny kódující 11 β-hydroxylázu a aldosteronsyntázu: U potkanů kmene SS (salt-sensitive) se zvýšený krevní tlak vyvine v důsledku nadměrného příjmu soli potravou. U kontrolního kmene SR (salt-resistant) nemá zvýšený příjem soli na krevní tlak žádný vliv. Podobně jako u člověka je u potkana gen pro 11 β-hydroxylázu v těsné vazbě s genem, který kóduje hormon aldosteronsyntázu. Jeho sekvencování u kmene SR odhalilo záměny aminokyselin ve srovnání s kmenem SS a dalšími testovanými kmeny. Tento výzkum je prvním důkazem souvislosti mezi mutovaným genem, sníženou aktivitou jím regulovaného hormonu a následným ovlivněním krevního tlaku u laboratorního potkana.
- Geny kódující podjednotky β a γ?epiteliálního sodíkového kanálu: U dvou nejpoužívanějších modelů lidské esenciální hypertenze, u potkanů SS a u spontánně hypertenzních potkanů kmene SHR, vyvolává vysoký příjem soli v potravě zvýšení krevního tlaku. Vazebné studie u obou kmenů podaly důkazy pro asociace s geny kódujícími podjednotky β a γ epiteliálního sodíkového kanálu na 1. chromozomu.
- Geny podmiňující Bartterův syndrom: U potkana byl gen, jehož mutace jsou u lidí odpovědné za Bartterův syndrom typu I, nalezen na 3. chromozomu. Protože u potkana nebyl v této oblasti genomu lokalizován žádný genetický znak spojený s krevním tlakem, je poněkud nepravděpodobné, že by se tento gen významně podílel na předurčení vysokého tlaku u kmenů SS nebo SHR. Geny odpovědné za Bartterův syndrom typu III nebyly dosud u potkanů zmapovány. Naproti tomu vazebné analýzy prokázaly přítomnost genu regulujícího krevní tlak na 8. chromozomu potkana, v oblasti, která je homologní s lidským chromozomem 11q, kam byl lokalizován gen odpovědný za Bartterův syndrom typu II.
Ke stažení
 Článek ve formátu PDF [326,56 kB]
Článek ve formátu PDF [326,56 kB]