Tajemství embryonálního vývoje
Vývojová biologie sleduje cestu od jedné buňky, oplozeného vajíčka, k novorozenci s vyvinutými a funkčními orgány. Snažíme se objasnit biologické principy, jimž embryogeneze, tedy růst zárodku a postupná specializace jeho buněk, podléhá.
Zárodečný vývoj mnohobuněčných organismů je založen na buněčné diferenciaci, při které se buňky specializují na určitou funkci. Funkční specializace vyžaduje nasazení celé armády enzymů a strukturních proteinů, které buňce umožní plnit daný úkol. Například beta-buňky ve slinivce se neobejdou bez sady enzymů pro produkci inzulinu, ale nepotřebují vyrábět neurotransmitery, které jsou pro změnu nezbytné pro funkci nervových buněk.
Všechny buňky lidského těla (s výjimkou bezjaderných červených krvinek) přitom disponují stejnou genetickou výbavou, sestávající z asi 25 000 genů. Pro správný vývoj organismu je proto zcela zásadní přesný výběr genů, které jsou v jednotlivých buněčných typech aktivní.
Lidský genom si lze představit jako knihu s třemi miliardami písmen, v níž jedna kapitola představuje jeden gen. V žádné specializované buňce se však nečtou všechny kapitoly, ale pouze ty, které buňka potřebuje k plnění své specifické funkce. Při vývoji zárodku proto mluvíme o časové a prostorové aktivaci genů vedoucí k produkci proteinů s požadovanou funkcí. Jaké jsou ale mechanismy, které rozhodují o přečtení správných „kapitol“ (genů) a přeskočení těch nedůležitých?
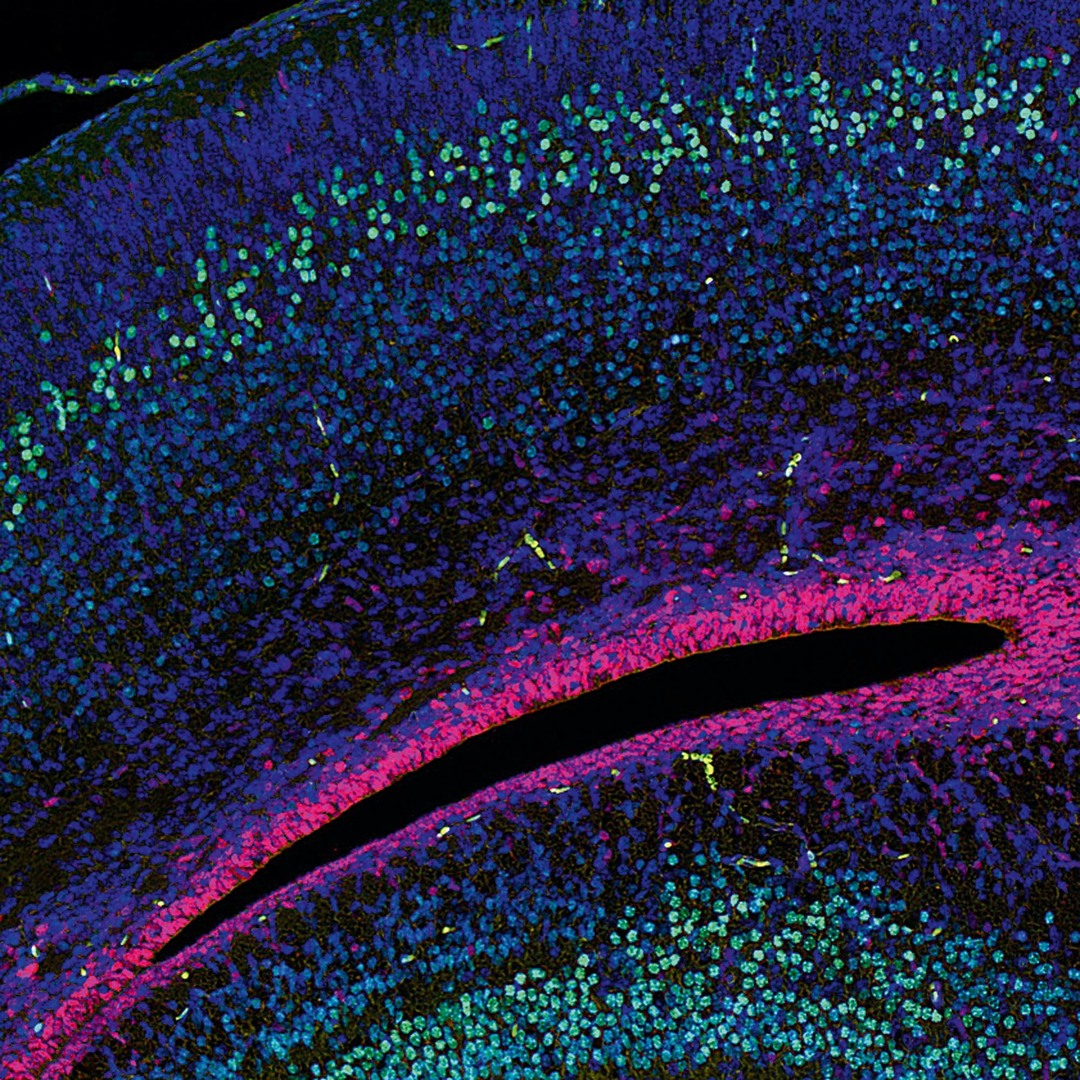
Neurony a pomocné buňky (např. gliové buňky, oligodendrocyty) vznikají z nervových kmenových buněk jejich řízenou diferenciací a specializací. Například v mozkové kůře se nachází během embryogeneze mohutná zárodečná vrstva kmenových buněk, z které nově vznikající neurony a glie migrují do předem daných vrstev mozkové kůry, kde se usazují a začínají tvořit funkční spoje (obr. 1). V dospělém mozku je tato zárodečná vrstva minimální a přetrvává pouze v oblastech postranních ventrikul a v gyru, části hipokampu.
Nervové kmenové buňky lze kultivovat in vitro, namnožit je a navodit jejich diferenciaci. Pochopení jejich vlastností může v budoucnu pomoci v léčbě neurodegenerativních onemocnění. Naše oddělení například popsalo klíčovou roli transkripčních faktorů Tcf na formování hipokampu. Pokud je gen pro jeden z těchto faktorů v experimentálních myších uměle poškozen, aktivace genů se naruší a velká část hipokampu se nevytvoří. Mozek pak není plně funkční a chybí mu i důležitý zdroj nervových kmenových buněk.1)
K zvlášť fascinujícím embryogenetickým procesům patří formování chrupavek a kostí v hlavové a obličejové části (obr. 2). Na rozdíl od dlouhých kostí (např. v končetinách) jsou tvary a velikosti hlavových kostí velmi různorodé. V počátku jsou určovány přesným shlukováním specifických mezenchymálních buněk, z nichž následně vznikají buňky kostní tkáně (osteoblasty) a chrupavky (chondrocyty).
Jak se spolu mezenchymální buňky dohodnou na správném seskupení, aby vznikla chrupavka a kost v požadovaném tvaru? Je podivuhodné, že tyto buňky mají původ v zárodečné nervové tkáni v oblasti neurální lišty, z které migrují do obličejové části. Na buňky neurální lišty můžeme proto nahlížet jako na zárodečné kmenové buňky, z kterých se generují nejen nervy a glie, ale i chrupavky a kosti, pigmentové buňky, chlopně v srdci a další části těla. Nedávno jsme popsali, že transkripční faktor Meis2 řídí aktivaci specifických genů v buňkách neurální lišty tak, aby správně proběhla mezenchymální kondenzace a diferenciace kostních a chrupavkových buněčných prekurzorů. Pokud je tento gen poškozen, ať už uměle v myších, nebo spontánně u některých lidských pacientů, mají tito jedinci malformované obličejové kosti, narušené některé mozkové funkce nebo srdeční patologie.2)
Oddělení vývojové biologie se zabývá genetickou regulací zárodečného vývoje. Využíváme technologie tkáňově specifických knokautů (inaktivace genů) v myších k objasnění funkce některých signalizačních drah a vybraných transkripčních faktorů, které řídí zárodečný vývoj kraniofaciální a vývoj nervové tkáně. Studie na myších modelech jsou doplněny experimenty s embryi modelové rybky dánia pruhovaného (Danio rerio). V těchto experimentálních organismech se snažíme objasnit genetickou podstatu některých lidských vývojových vad.
Vedoucí oddělení: RNDr. Ondřej Machoň, Ph.D.
Poznámky
1) DOI: 10.1186/s13064-018-0107-8.
2) DOI: 10.1242/bio.052043; 10.3389/fcell.2022.951063; 10.1002/dvdy.731.
Ke stažení
 článek ve formátu pdf [343,78 kB]
článek ve formátu pdf [343,78 kB]