Železo nepatří do šrotu
O důležitosti železa (Fe) nás dostatečně přesvědčily už naše maminky, když jsme s bryndáčkem u krku odmítali přijmout lžíci špenátu. K dovršení těchto dětských traumat se později ukázalo, že špenát nijak zvlášť vydatný zdroj lehce využitelného železa nepředstavuje.1) Utrpení bylo zbytečné, spíše by nám tehdy prospěly např. vydatné dávky červeného masa. Možná jsme si vycvičili železné nervy, jinak se však obsah tohoto kovu v našem těle příliš nezměnil.
 Železo je nepostradatelnou součástí hemoglobinu červených krvinek (zde jsou vázány plné dvě třetiny našich železných rezerv), ale důležité je i pro činnost řady enzymů. Ovšem všeho s mírou! Zatímco nedostatek železa působí chudokrevnost (anémii), protože schází potřebné množství materiálu na tvorbu hemoglobinu, přemíra železa může být toxická. O tom by mohli povídat pacienti s dědičnou hemochromatózou, kteří vstřebávají z potravy železa příliš mnoho.
Železo je nepostradatelnou součástí hemoglobinu červených krvinek (zde jsou vázány plné dvě třetiny našich železných rezerv), ale důležité je i pro činnost řady enzymů. Ovšem všeho s mírou! Zatímco nedostatek železa působí chudokrevnost (anémii), protože schází potřebné množství materiálu na tvorbu hemoglobinu, přemíra železa může být toxická. O tom by mohli povídat pacienti s dědičnou hemochromatózou, kteří vstřebávají z potravy železa příliš mnoho.
Na rozdíl od jiných prvků není možné regulovat výdej železnatých a železitých iontů z těla (o železo totiž přicházíme hlavně při ztrátách krve nebo odlupováním odumřelých epiteliálních buněk). Proto musí být obzvláště pečlivě kontrolován příjem železa střevní sliznicí, jeho skladování a recyklace v těle. Za to odpovídají proteiny, jejichž roli naznačují i názvy: feritin,2) transferin či feroportin. K těmto proteinům operujícím se železem můžeme přiřadit i poetický hephaestin, pojmenovaný po řeckém bohu ohně, kovářů a dalších řemeslníků.
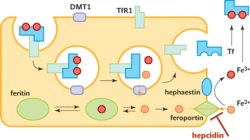
Přehled o koloběhu železa zachycuje schéma 1. Železnaté ionty jsou vstřebávány do buněk střevního epitelu. Zde může být železo uskladněno ve vazbě na feritin nebo vypuštěno do krve přes feroportinový transportér. Přitom je Fe2+ oxidováno na Fe3+ zmíněným hephaestinem. Pro přenos Fe3+ v krvi je určen protein transferin (Tf). V případě potřeby můžou buňky různých tkání vystavit na svém povrchu transferinový receptor (TfR), kterým přenašeč zachytí. Buňka pak transferin i s receptorem pohltí, sníženým pH železo z vazby uvolní, vstřebá je přes DMT1 (divalent metal transporter) do cytoplazmy a prázdný transferin (apo-transferin) opět vypustí ven. Vedle toho se v krvi zejména při krvetvorbě recykluje železo z použitého hemoglobinu. Poškozené červené krvinky jsou pohlcovány makrofágy, které slouží jako další důležitý zásobník železa.
Celotělovou rovnováhu mezi skladováním a recyklací železa udržuje jaterní hormon hepcidin. Jeho funkce byla objevena víceméně náhodou zhruba před deseti lety (o tom viz Vesmír 81, 253, 2002/5). Do té doby byl znám jen jako látka tlumící dělení bakterií. I po deseti letech zůstává kolem hepcidinu řada otázek. Víme však, že působí inhibičně na feroportiny, a tím snižuje výdej železa ze zásobních tkání do oběhu. Železo vázané na transferin zase stimuluje v játrech produkci hepcidinu. Hepcidin tedy jako odpověď na zvýšený obsah železa v krvi brzdí jeho další uvolňování ze zásobních tkání.
Nedostatek kyslíku pro změnu výrobě hepcidinu brání, takže se pak do krve dostává více železa. Tím je zajištěn dostatek železa pro nové erytrocyty, které hladinu kyslíku opět obnoví. Hepcidin je také vytvářen pod vlivem zánětlivých faktorů. Fyziologická funkce této regulace není zcela jasná, nechtěným důsledkem však je skutečnost, že některá zánětlivá onemocnění doprovází pokles koncentrace železa v krvi a potažmo anémie.
 Kromě systémové hormonální regulace toku železa, která je zkoumána v posledních letech, existuje i kontrolní systém zásob železa v každé buňce. Zatímco exprese hepcidinu je ovlivňována na úrovni přepisu DNA do mRNA, buněčný kontrolní systém využívá spíše změn stability mRNA. Čím stabilnější mRNA je, tím více proteinu podle ní může být na ribosomech syntetizováno. Na svém 3'-konci obsahuje mRNA pro receptor transferinu několik tzv. IRE (iron responsive element) – sekvencí tvořících vlásenky, na něž se můžou vázat IRP (IRE-binding proteins, viz obr. 2). Díky této vazbě stoupá stabilita mRNA a tím i produkce receptoru. Do buňky díky tomu může být přijímáno více železa. Železo samotné ovšem brání vazbě IRP na mRNA. Produkce transferinového receptoru je tak stimulována pouze v podmínkách nedostatku železa. Stejně je ovlivňována i syntéza DMT1, který se na importu železa rovněž podílí.
Kromě systémové hormonální regulace toku železa, která je zkoumána v posledních letech, existuje i kontrolní systém zásob železa v každé buňce. Zatímco exprese hepcidinu je ovlivňována na úrovni přepisu DNA do mRNA, buněčný kontrolní systém využívá spíše změn stability mRNA. Čím stabilnější mRNA je, tím více proteinu podle ní může být na ribosomech syntetizováno. Na svém 3'-konci obsahuje mRNA pro receptor transferinu několik tzv. IRE (iron responsive element) – sekvencí tvořících vlásenky, na něž se můžou vázat IRP (IRE-binding proteins, viz obr. 2). Díky této vazbě stoupá stabilita mRNA a tím i produkce receptoru. Do buňky díky tomu může být přijímáno více železa. Železo samotné ovšem brání vazbě IRP na mRNA. Produkce transferinového receptoru je tak stimulována pouze v podmínkách nedostatku železa. Stejně je ovlivňována i syntéza DMT1, který se na importu železa rovněž podílí.
Podobné IRE, ovšem umístěné na druhé straně mRNA (na jejím začátku čili 5'-konci), obsahuje i transkript genů např. pro feritin a feroportin. Tady vazba IRP nezvyšuje stabilitu, ale naopak brání nasednutí ribozomu. Pokud buňce schází železo, bylo by zbytečné vyrábět proteiny pro jeho skladování nebo dokonce export. Je proto výhodné, že nedostatek železa tlumí prostřednictvím IRP translaci feritinu a feroportinu.
Zatímco posttranskripční regulace prostřednictvím sekvencí IRE se již stala klasickým příkladem z molekulárně biologických učebnic, hormonální řízení metabolismu železa je stále poměrně horkou novinkou. Víme, že se buněčný a celotělový regulační systém vzájemně ovlivňují. Transferinový receptor je syntetizován v závislosti na dostupnosti železa v buňce (IRE/IRP regulace) a jeho prostřednictvím je pak v hepatocytech stimulována produkce hepcidinu. Podobně je feroportin syntetizován pod vlivem IRP, ale na jeho další aktivitu má vliv hepcidin. Souhra obou mechanismů je v současnosti předmětem intenzivního výzkumu.
Detailnější porozumění procesům řídícím nakládání se železem by mohlo přinést i efektivnější léčebné postupy pro pacienty s některými anémiemi nebo hemochromatózami. Nevhodná míra železa zkrátka dělá zlou krev. Maminky to s tím špenátem myslely dobře, i když neměly přesné informace.
Literatura
Hentze M. W., Muckenthaler M. U., Galy B., Camashella C.: Two to Tango: Regulation of Mammalian Iron Metabolism. Cell 142, 24–28, 2010.
Poznámky
1) Pozn. red.: Při analýze a výpočtu obsahu železa ve špenátu se totiž vědci dopustili matematické chyby a posunuli desetinnou čárku o jedno místo. A tak se lidé dlouho domnívali, že tmavě zelené listí obsahuje desetkrát více železa, než v něm skutečně je. Nadto využitelnost železa z rostlin je kolem 1 %, maximálně 7 %, z červeného masa až 20 % (Sci. Am. 265, 46–52, 1991/4).
2) Feritin byl poprvé popsán už r. 1935 známým fyziologem Vilémem Laufbergrem.
Ke stažení
 článek ve formátu pdf [343,38 kB]
článek ve formátu pdf [343,38 kB]
O autorovi
Petr Zouhar





















