Nádory mohou ke své obraně používat apoptózu
| 5. 4. 1997Jedním z perspektivních přístupů léčby nádorů je nesporně imunoterapie, která nabízí možnost specificky zacílit a zničit nádorovou buněčnou populaci. Tento přístup mimo jiné umožňuje využít schopnosti lymfocytů T rozeznat abnormální buňky a zlikvidovat je. Jeden z cytolytických mechanizmů, jímž jsou lymfocyty T k tomuto úkolu vybaveny, používá k eliminaci cílové buňky apoptózu (programovanou buněčnou smrt), kterou navodí aktivací povrchového proapoptotického receptoru Fas (označovaného též jako Apo-1 nebo CD95), v případě, že jej daná buňka exprimuje. Aktivovaný lymfocyt T nese totiž na svém povrchu ligand FasL, který se může na protein Fas vázat. Interakce FasL-Fas spustí v cílové buňce sled nitrobuněčných událostí vedoucích k apoptóze. Buňka nesoucí ligand FasL, v tomto případě imunokompetentní buňka, zůstává při celém procesu nepoškozena a může zahájit útok proti dalším cílům.
Na konci imunitní odpovědi, po likvidaci všech cílových antigenů, musí být klon již nepotřebných aktivovaných lymfocytů T zredukován. Patrně pro tento účel jsou aktivované lymfocyty vybaveny také receptory Fas, jejichž prostřednictvím lze v nositelských lymfocytech navodit buněčnou smrt. Avšak právě přítomnost receptoru Fas v plazmatické membráně aktivovaných lymfocytů umožňuje jiným buňkám, nesoucím na svém povrchu FasL, použít jejich ligand jako zbraň proti útoku lymfocytů T. Za fyziologických okolností jsou takovou obranou vybaveny buňky některých imunologicky privilegovaných tkání jako např. Sertoliho buňky varlete, buňky přední komory oční nebo centrálního nervového systému.
Velice překvapivé bylo zjištění publikované nedávno švýcarským výzkumným týmem, které dokládá, že stejného mechanizmu mohou k úniku před imunitním útokem použít buňky jednoho z nejzhoubnějších kožních nádorů – melanomu. Buňky melanomu na svém povrchu exprimují ligand FasL, ale postrádají proapoptotický Fas (viz schéma). Z tohoto důvodu, ačkoli je melanom často rozpoznán imunitními buňkami a je jimi infiltrován, nemohou aktivované lymfocyty T navodit buněčnou smrt v neoplastických buňkách. Naopak nádor předkládající ligand FasL indukuje v aktivovaných lymfocytech T buněčnou smrt podobně, jako to dělají při obraně svého teritoria zmíněné imunologicky privilegované tkáně. Apoptóza imunokompetentních buněk proběhne bez jakéhokoli zánětlivého poškození tkáně a současně zabrání dalšímu rozvoji imunitní odpovědi.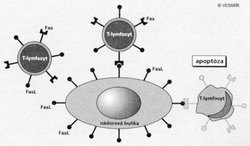
Podle předběžných nálezů exprimují ligand FasL, který pro aktivované lymfocyty T představuje smrtící signál, i některé jiné typy nádorových buněk. Pochopení mechanizmu, jenž se uplatňuje při ochraně nádoru proti vpádu imunokompetentních buněk, nabízí možnost cíleného léčebného zásahu do celého procesu. (Hahne, M. et. al.: Science 274, 1363–1366, 1996.)




















