Struktura a anomálie vody
| 16. 7. 2014Voda vykazuje překvapující řadu fyzikálních vlastností, některé zjevně jedinečné, které slouží k definici její neobvyklé „osobnosti“.
F. H. Stillinger, Adv. Chem. Phys. 31, 1, 1975
Voda je často označována přívlastkem „anomální“. Podíváme-li se do slovníku, zjistíme, že „anomálie“ je „nepravidelnost, výjimečnost; odchylka či úchylka od normálu“. Jenže co je to ten „normál“, není-li to voda, pro běžný lid nejobvyklejší kapalina? Pro někoho je normální kapalinou řekněme alkohol (ethanol), pro jiného benzín… Jako člověk živící se podivnou naukou zvanou statistická termodynamika mám zde jasno: normální je kapalný argon. Jeho molekuly jsou pěkně kulaté, což zjednodušuje teoretický popis. Ostatní vzácné plyny už tak normální nejsou: ty větší (krypton, xenon, radon) jsou moc velké a měkké, polarizují se, o relativistických elektronech poblíž těžkého jádra nemluvě (a o ceně vůbec). Ty menší (neon, helium) jsou moc lehké, pak musíme i v kapalině používat kvantovou teorii – o podivnostech supratekutého helia jste asi slyšeli.
Zkusme se podívat na pár „anomálií“ vody zblízka.
Led plave na vodě
Vědecky řečeno to znamená, že hustota vody je větší než ledu, a to v poměru 12:11. Toto chování není příliš časté, běžné látky (vosk, kovy) mají poměr hustot opačný – jistě víte, že hladina vosku se ve vychladlé svíčce propadne, podobně lité vánoční olovo. Z cca 100 prvků ho najdeme u germania, bismutu, galia, ceru a prý i plutonia (pozor při výrobě atomových bomb). U vody je však poměr hustot poměrně velký. Tato vlastnost má několik důsledků, z nichž některé znáte: dáte‑li do mrazáku pivo a zapomenete na ně, láhev praskne. Tlak za teploty –22 °C může dosáhnout až 210 MPa (2000 atmosfér), což s přehledem roztrhne ocelový granát. Na netu najdete pěkná videa tzv. ledové bomby (googlujte „ice bomb“, např. http://youtu.be/erlZb8QiPkg).
Regelace ledu
Méně dramatickou ukázkou důsledků nižší hustoty ledu vůči vodě je regelace ledu. Najdeme tenký, nejlépe měděný drátek a zatíženou smyčku pověsíme na kus ledu o teplotě blízko 0 °C (nikoliv rovnou z mrazáku – nutno hodinku „ohřívat“ v ledničce). Drátek se ledem „protaví“, ale kus ledu zůstane celý. Jev je důsledkem toho, že led plave na vodě. Při zvýšení tlaku je totiž stabilnější fáze o vyšší hustotě (voda), a proto led pod drátkem taje. Skupenské teplo, které je pro tání potřeba, se získá opětnou krystalizací vody v místech s menším tlakem, tedy nad drátkem. Teplo proudí drátkem seshora dolů (proto je vhodná měď, která má velkou tepelnou vodivost) a voda okolo drátku nahoru, kde opět mrzne. Rozdíl teplot při běžném uspořádání je několik setin stupně, a proto se pokus nepovede, pokud je led příliš studený. (Více na těchto stránkách VŠCHT, kde najdete i vzorečky pro výpočet doby řezání.) Tavení ledu pod tlakem však není odpovědné za snadné bruslení či lyžování. Za malý koeficient tření může především tzv. premelting – tenká vrstvička se strukturou podobnou vodě na povrchu ledu – a vznik malého množství kapalné vody na povrchu třením.
Jakousi anti‑anomálií je, že těžký led (z těžké vody, kde byl vodík nahrazen těžším isotopem vodíku – deuteriem) na obyčejné vodě neplave, jeho hustota je totiž o necelá 2 % větší než lehké vody. Vhodíme‑li tedy kus těžkého ledu do obyčejné vody, potopí se, ale jak se část roztaví a zahustí vodu okolo, led se (po zamíchání) vynoří. Pokus je zvlášť efektní, pokud si těžkého ledu předem lízneme, aby si divák myslel, že se jedná o led obyčejný (několik gramů je neškodných, ekvivalentní množství deuteriem značených sloučenin se používá při výzkumu metabolismu).
Maximum hustoty
Ochlazujeme‑li horkou vodu, zmenšuje objem (jinými slovy zvyšuje se hustota). Toto je zcela normální chování, na lihovém (i na zakázaném rtuťovém) teploměru vidíme, že se kapaliny při zahřívání roztahují. Ale pokračujeme‑li v chlazení pod 4 °C, začne se voda opět roztahovat – jako by se studená voda chystala na zmrznutí na led (o větším objemu). Vodní teploměr nejen že by nefungoval pod teplotou 4 °C, kdy má voda maximální hustotu, ale měl by i nerovnoměrné dílky. Maximum hustoty je u těžké vody dokonce až při 11 °C. Za vyšších tlaků se maximum hustoty posunuje do nižších teplot, až jev vymizí – stačí dostatečně zatlačit a výstřelky jsou pryč.
Důsledkem je, že rybníky, moře a jezera zamrzají odshora. Při ochlazování nejprve studená voda klesá ke dnu; pokud však teplota vody klesne pod 4 °C, zůstává studená voda nahoře a u dna jsou pro kapry příjemné čtyři stupně. Rybník se přestane promíchávat a zamrzne od hladiny. Obě anomálie mají význam pro biosféru a možná pomohly k zachování života na Zemi před 650 miliony let, kdy (podle hypotézy zvané “snowball Earth”) celá Země zamrzla.
Tepelné vlastnosti
Ono je trochu divné už jen to, že voda je za běžných podmínek kapalná, neboť podobné malé molekuly jsou plyny: např. methan CH4 (známý jako zemní plyn) se stejnou elektronovou strukturou, sulfan H2S (má v molekule místo kyslíku těžší síru, dříve se nazýval sirovodík) aj. To znamená, že mezi molekulami vody působí silné přitažlivé síly. Dále má voda velkou tepelnou kapacitu (ohřát litr vody trvá déle než litr oleje). To by nebylo až tak divné, ale kapalná voda má větší tepelnou kapacitu než stejné množství ve formě páry nebo ledu.
Viskozita
Viskozita je míra odporu kapaliny proti pohybu (vrstev kapaliny proti sobě). Med je viskózní, tedy naléván z nádoby teče pomalu. Pod vyšším tlakem se viskozita normálních kapalin zvyšuje, neboť molekuly jsou natlačeny blíže k sobě a při pohybu si více překážejí. Ne tak voda, ta má opět něco extra – viskozita vody (za teplot pod 30 °C) při zvýšení tlaku klesá.
Teplotní závislosti a podchlazená voda
Již jsme se zmínili o hustotním maximu. Ukazuje se, že podobným způsobem, tj. „normálně“ za vyšších teplot a „anomálně“ za nižších teplot, s minimem nebo maximem, se chová i mnoho dalších veličin: např. rychlost zvuku má maximum při 73 °C, tepelná kapacita (za konstantního tlaku) má minimum při 35 °C aj.
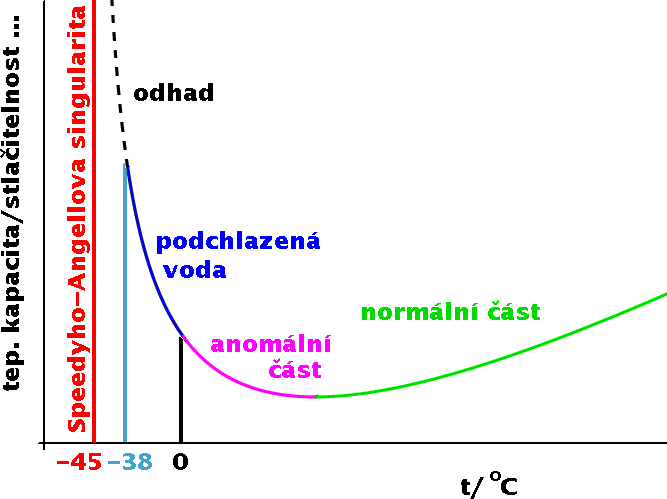
Tedy studená voda je anomálnější. A ještě anomálnější je pod nulou – tedy pokud nezmrzne. Naštěstí pro zvědavé vědce není až tak obtížné si (mírně) podchlazenou vodu vyrobit (viz např. http://youtu.be/jouKXytWD8g, jen se nedivte stupňům – jsou ve °F). Použijeme jakoukoliv měkkou balenou vodu (nesycenou, ne minerálku) a dáme ven za klidného mrazivého počasí; mrazák není vhodný, protože mu vrčí motor, a jakékoliv vzruchy či nečistoty podporují vznik zárodků ledu. Pokud pak do láhve o teplotě řekněme -5 °C cvrnkneme, uvidíme, jak od místa poruchy roste sníh (zásoba chladu nestačí na promrznutí na kost). Ve speciálních laboratorních podmínkách (tenké čisté kapiláry ap.) lze vodu podchladit na cca -40 °C, ovšem čím nižší teplota, tím obtížnější je jakékoliv měření. Nicméně výsledky ukazují, že anomální chování se při podchlazení zvýrazňuje; dokonce bylo navrženo [viz sa76 v seznamu literatury], že za teploty cca -45 °C či níže by (kdyby voda nezmrzla) došlo k tzv. singularitě, tj. hodnoty některých veličin by byly rovny nekonečnu. (To neznamená, že by voda přestala existovat, tzv. kritických bodů známe hodně, např. ochlazujeme‑li žhavé železo, je tepelná kapacita singulární v tzv. Curiově bodě, kde se stane železo feromagnetickým.)
Hypotetické dvě vody
Když nalijeme olej na vodu, dostaneme vrstvu oleje na vrstvě vody. Obě vrstvy jsou zcela zřetelně odděleny rozhraním. Dovedete si ale představit, že nalijeme vodu na vodu a vzniknou dvě vrstvy vody oddělené rozhraním, spodní s vyšší hustotou než horní? Přesto není vyloučeno, že se voda takto chová, ovšem za vyšších tlaků a hlavně velmi nízkých teplot. Pokud vodu ochladíme extrémně rychle pod cca -140 °C, takže se molekuly vody nestihnout uspořádat do krystalové mřížky ledu (voda nezmrzne), dostaneme pevný, ale neuspořádaný stav – sklo. (Podobně když ochlazujeme roztavené sklo třeba při výrobě oken, je jeho viskozita čím dál tím větší, až od určité teploty je tak velká, že sklo je tuhá látka, ovšem není krystalická a má strukturu podobnou kapalině.)
Výsledná látka se nazývá LDA (low density amorphous) led. Na krystalický led se nezmění proto, že pohyby molekul jsou pod -140 °C velmi pomalé, a proto i viskozita je obrovská. Pokud tento LDA ohřejeme nad cca -120 °C, začnou se molekuly trochu hýbat a voda zkrystalizuje (na trochu jiný led, než známe, totiž kubický led Ic). Nyní pozor: pokud toto LDA sklo stlačíme, změní strukturu a stane se HDA (high density amorphous). Zdá se, že obě struktury jsou dostatečně odlišné na to, abychom mohli spekulovat o tom, že za o něco vyšších teplot bychom (za vhodného tlaku) mohli mít dvě kapaliny, hustší a řidší, v rovnováze – jen kdybychom mohli zabránit krystalizaci. Při dalším zvyšování teploty by se hustoty obou kapalin vyrovnávaly, až by se ztotožnily v tzv. kritickém bodě; nad touto teplotou by pak byla jen jedna voda. Dalším experimentálním náznakem platnosti tohoto scénáře je, že onen hypotetický kritický bod „vidíme“ z druhé strany (od podchlazené vody) jako (neméně hypotetickou) Angellovu singularitu. Nejnovější simulace [d14] s modelem vody ST2 tvrdí, že ano, že vody jsou dvě; jiné [lc13], že ne. To jsou ovšem jen modely (a ještě ne nejlepší); jestli existují dvě reálné vody, nevíme, a nevíme ani, jestli má vůbec smysl uvažovat o „vodě, která nemrzne“, když ona mrcha mrzne. Minimálně je to velmi nepozitivistické.
Příliš mnoho ledů
Kdo četl Vonnegutův román Kolíbka (Cat’s Cradle), vzpomene si na led č. IX. Tento zlořečený led byl sice stabilní za běžného tlaku a teploty, ale jen velmi, opravdu velmi nerad vznikal při podchlazení (na rozdíl od obyčejného ledu výše), tj. bylo potřeba do vody vhodit zárodek, od nějž pak led IX rostl, až vyrostl. Skutečný led IX je stabilní jen za nízkých teplot a vysokého tlaku. Voda totiž může krystalovat v mnoha modifikacích, viz fázový diagram níže. Když připočteme krystaly vody s něčím (plyny, soli), dostaneme další obrovské množství možných struktur.
Zajímavou skupinou směsných krystalů jsou klatráty nebo také hydráty plynů. Vznikají za nižších teplot a vyšších tlaků. Struktura obsahuje dutiny, ve kterých hnízdí různé molekuly. Např. na dně chladnějších moří nebo také v trubkách plynovodů vzniká „hořící led“, hydrát methanu se strukturou typu I.
Za normálního tlaku mrzne voda na hexagonální led Ih. Jeho krystalová soustava je nejlépe patrná z šesterečné symetrie sněhových vloček. Za nižších teplot je stabilní led s kubickou mřížkou. Všechny ledy mají sice atomy kyslíku uspořádané v pravidelné mřížce, ale to vždy neplatí pro vodíky. Jistě, ke každému kyslíku patří dva vodíky, a zároveň mezi dvěma sousedícími kyslíky smí být právě jeden vodík zajišťující vodíkovou vazbu, ale stále máme spoustu možností, jak vodíky rozmístit. Počet těchto možností spočítal nositel Nobelovy ceny Linus Pauling a vyřešil tak rozpor mezi entropií stanovenou klasickou termodynamickou cestou a hodnotou spočtenou ze spektroskopických dat a nově vzniklé kvantové teorie. Protože však existují nepatrné rozdíly mezi energiemi různých konfigurací vodíků, za velmi nízkých teplot je stabilní led XI se strukturou Ih, ale s uspořádanými vodíky. To, že je stabilnější, neznamená, že snadno vzniká; naopak za tak nízkých teplot musíme používat různé triky, abychom usnadnili přechod jedné struktury na jinou. Za vyšších tlaků existuje spousta dalších ledů, které mají více či méně smáčklou a zborcenou mřížku.
Entropie je veličina, která se špatně popularizuje. Obvykle se říká, že je „mírou neuspořádanosti systému“. Ale historicky byla zavedena v polovině 19. století jako výsledek úvah o účinnosti parních strojů. Dobře se tehdy vědělo, že je snadné mechanickou energii přeměnit třením na teplo, ale opačný proces, výroba mechanické (nebo dnes elektrické) energie z tepla je mnohem obtížnější. Teplo je jaksi méně hodnotná forma energie.
Je možné si ale představit idealizované děje, při kterých k žádné zbytečné přeměně mechanické energie na teplo nedochází; takové děje se nazývají vratné. Např. pokud budeme pod pístem ve válci stlačovat plyn (bez tření, vše dokonale izolované aj.), bude se plyn ohřívat (to znáte – pumpička k jízdnímu kolu se zahřívá). Ke stlačování musíme dodat mechanickou energii, při opětném rozpínání plynu na původní stav získáme zpět přesně stejné množství mechanické energie. Pokud bychom nyní plyn ve válci něčím ohřáli nebo nějakou mechanickou energii změnili na teplo, dostaneme jiný stav plynu. Z něj můžeme také provozovat vratné děje. Rozdíl je ten, že žádný stav plynu v tomto ohřátém systému nebude stejný (tj. nebude mít stejnou kombinaci tlaku a teploty) jako v předchozím případě, tj. křivky na obrázku se neprotnou; kdyby tomu tak bylo (viz škrtnuté schéma), mohli bychom libovolně obíhat přes toto protnutí a při každém oběhu získat práci jen z tepla, což je tzv. perpetuum mobile druhého druhu, které nebylo nikdy pozorováno. Křivky, které se neprotínají, si můžeme očíslovat, a toto očíslování (udělá‑li se chytře) je entropie.
Entropie jako míra neuspořádanosti systému byla zavedena Ludwigem Boltzmannem o dvacet let později. Klíčem k pochopení ekvivalence obou formulací je poznatek, že dodané teplo zvyšuje tepelný pohyb molekul, a proto se zvyšuje míra chaosu v systému. Jakýkoliv chaos vzniká snadno spontánně (nedáme‑li si pozor a neprovádíme děje vratně). Naopak, cokoliv uklidit či uspořádat vyžaduje práci.
Struktura
Při jevech popsaných výše jsme neuvažovali chemické reakce, molekula vody se tedy nerozpadá na atomy či ionty. To samozřejmě není pravda, v čisté vodě za běžných podmínek je řádově jedna molekula z miliardy rozložena na proton (H+) a hydroxyl (OH−). To by však byla jiná kapitola, při vysvětlení většiny anomálií se obejdeme bez chemických reakcí.
My fyzikální chemici víme, že základem k vysvětlení čehokoliv je znalost mikrostruktury, tj. jak jsou jednotlivé molekuly vody uspořádány. Jak se ale dopídit struktury, když je molekula vody tak malá? Naštěstí máme k dispozici sofistikované experimenty, které strukturu „vidí“. Nejprve však potřebujeme vědět, jak strukturu vůbec popsat. Používá se k tomu tzv. radiální distribuční funkce.
Uvažujme nejprve velmi malé (prakticky bodové) molekuly plynu létající prostorem. Počet molekul je N a objem nádoby V. Pravděpodobnost toho, že naleznu vybranou molekulu č. 1 v malé krychličce o objemu dV, je p=dV/V; pravděpodobnost, že tam naleznu jednu z Nmolekul, je pak p=NdV/V. Pokud chci popsat korelace mezi molekulami, budu uvažovat tuto pravděpodobnost v závislosti na vzdálenosti r od vybrané (červené) molekuly. Pravděpodobnost pak bude p=(N−1)dV/V, neboť jednu molekulu jsem už vybral.
Pokud nebudeme mít řídký plyn, ale kapalinu, nebude vztah pro pravděpodobnost platit – např. zjevně nenajdeme žádnou molekulu velmi blízko jiné molekuly, protože molekuly se silně odpuzují, jsou‑li blízko u sebe. Vzorec proto opravíme zavedením bulharské konstanty g(r), což je ona slíbená radiální distribuční funkce: p=g(r) (N−1)dV/V. Jinými slovy, g(r) udává, kolikrát je pravděpodobnější (ve srovnání s ideálním plynem), že ve vzdálenosti r od nějaké vybrané molekuly najdeme jinou.
Na obrázku vidíte radiální distribuční funkce ideálního plynu a kapalného argonu, který máme tak rádi; na vodorovné ose je vzdálenost molekul r v nanometroch (1 nm = miliontina milimetru). Hodnota g(r) je jednička pro ideální plyn podle definice. Pro argon je radiální distribuční funkce nula pro malé r, vzroste na asi 3 ve vzdálenosti, která odpovídá první slupce sousedů; je to vzdálenost, kde se molekuly nejvíc přitahují. Ve zhruba jeden a půl násobku vzdálenosti maxima je minimum, kde nalezneme v průměru méně molekul, protože jim překážejí molekuly v první slupce. Následuje méně výrazná druhá slupka. Molekuly daleko od sebe už o sobě nevědí, tedy g(r)=1 jako v plynu.
Měření radiální distribuční funkce
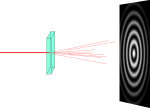
Podstatné ovšem je, že umíme radiální distribuční funkce měřit. Používáme k tomu rentgenové, (lepší, ale dražší) neutronové, případně elektronové záření. Chápu, že k pochopení čehokoliv je nejlepší pokus. K rentgence nebo jadernému reaktoru se člověk doma nedostane, naštěstí ale existují levnější náhražky – laserová ukazovátka. Vezměte jemný kapesník nebo dámskou punčochu a v zatemněné místnosti prosviťte látku. (Abych neloudil v zatemněné posluchárně od studentek punčochy, vytiskl jsem si na blánu na laserové tiskárně různé vzory.) Na stěně uvidíte kolem největší skvrny (přímého paprsku) menší skvrny rozptýlených paprsků.
Použití látky s pravidelnou sítí vláken ilustruje difrakci na krystalech, při difrakci v kapalině neuvidíme skvrny, ale soustředné kružnice. Zbývá z difrakčního obrazce extrahovat to, co nás zajímá – radiální distribuční funkci. To se provádí matematickou operací nazývanou inverzní Fourierova transformace; pokud vás termín vyděsil, vzpomeňte si na absolutní sluchaře, kteří ve zvuku orchestru poznají jednotlivé tóny – jejich hardware (uši) i software (mozek) vlastně také provádějí inverzní Fourierovu transformaci.
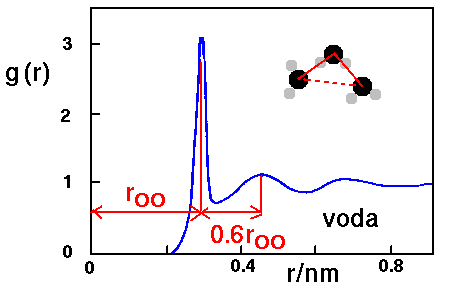
Podíváme‑li se na radiální distribuční funkci (kyslík-kyslík, tj. za střed molekuly považujeme atom kyslíku) kapalné vody (obr. vpravo), vidíme, že se neskládá ze slupek jako u argonu, ale vrstva druhých sousedů je blíž než je dvojnásobek nejbližších sousedů (asi 1,6krát). Klíčem k pochopení je chemie H2O. Kyslík má šest valenčních elektronů, vodík dva. Osm elektronů okolo atomu kyslíku vytvoří čtyři páry, které si nejméně překážejí, pokud se uspořádají do směrů odpovídajícím vrcholům čtyřstěnu (tzv. hybridizace sp3). Ideální úhel je 109,5°, úhel HOH ve vodě je jen 104,5°, protože kladně nabité vodíky zmenšují odpuzování elektronových párů. Můžeme si tedy zjednodušeně představit, že kolem kyslíku jsou dva laloky obsahující vodíky (jsou kladně nabité) a dva laloky bez vodíků (záporně nabité).
Vodík (resp. lalok s vodíkem) se pak přitahuje k zápornému laloku jiné molekuly vody. Tomu se říká vodíková vazba. V porovnání s ostatními silami je středně silná – je silnější než třeba interakce dvou atomů argonu, ale slabší než kovalentní vazba držící vodík u kyslíku v molekule. Tato vazba je také (na rozdíl od kulově symetrického přitahování dvou atomů argonu) úzce směrová. Kolem jedné molekuly vody je naděje, že budou čtyři jiné molekuly, dvě vázané svým vodíkem k elektronovým párům dané molekuly, a dvě vázané svými páry k vodíkům, a to vše plus minus v čtyřstěnovitém uspořádání. V krystalu ledu jsou všechny vazby nasyceny a každá molekula má čtyři sousedy. Ve vodě je druhé maximum ve vzdálenosti odpovídající geometrii, ale není příliš špičaté, což znamená, že zmíněná čtyřstěnovitost není úplná. Nesmíme si to ale představovat tak, že se molekuly vody drží sebe jak klíště. Naopak, vodíkové vazby jsou tak slabé, že neustále vznikají a zanikají. A to velmi rychle – zhruba bilionkrát za sekundu.
Vodíkové vazby se vyskytují nejen mezi molekulami vody. Jsou běžné mezi biologickými molekulami. Drží jimi DNA pohromadě. Sekundární a vyšší struktura proteinů je dána jednak vodíkovými vazbami, jednak tím, že ty postranní řetězce bílkovin, které vodíkové vazby netvoří (jsou hydrofobní) se skládají ve vodném roztoku k sobě, čímž má okolní voda víc možností, jak se sama pospojovat vodíkovými vazbami.
Molekulové simulace
Z experimentu získáme globální strukturní veličiny – radiální distribuční funkce kyslík-kyslík kyslík-vodík a vodík-vodík. To je ale málo. Co takhle zjistit, jak se molekuly vážou vodíkovými vazbami? K tomu nám slouží molekulové simulace. Nejprve potřebujeme popsat síly mezi dvěma molekulami vody matematicky, tj. vzorcem. Máme‑li molekul hodně (aspoň několik set), sečteme síly přes všechny dvojice molekul. Pak na počítači simulujeme vývoj tohoto souboru molekul v čase; tomu se říká molekulová dynamika. Alternativní simulační metodou je Monte Carlo používající náhodná čísla. (Chcete‑li si pohrát s oběma metodami, instalujte si SIMOLANT.)
Hladina vody zvětšená asi desetmiliardkrát a zpomalená půlbilionkrát, simulace metodou molekulové dynamiky, model vody SPC/E, teplota 25 °C. (Doporučujeme přepnout video na HD rozlišení.)
Síť vodíkových vazeb
Abychom mohli studovat vodíkové vazby, potřebujeme poznat, kdy jsou jimi dvě molekuly vázány. Je několik možností, např. můžeme použít vzájemnou energii molekul, nebo vzdálenost vodík-kyslík. Podstatné je, že následující výsledky na přesné definici nezávisí:
- Síť vodíkových vazeb je nepravidelná, lokálně přibližně čtyřstěnovitá (nejbližší sousedi molekuly jsou často uspořádáni do čtyřstěnu).
- Systém vodíkových vazeb je propojen (nevázané molekuly se téměř nevyskytují).
- V průměru připadají 3 až 4 vazby na molekulu, molekuly se 3–4 vazbami jsou nejčastější.
- Síť vodíkových vazeb obsahuje kruhy, kruhy délky 5 a 6 jsou nejčastější.
- Síť je výraznější a čtyřstěnovitější při nižších teplotách.
- Za nízkých teplot lze rozeznat polopravidelné mnohostěny složené z pěti‑, případně šestiúhelníků (obdobně jako třeba v klatrátech, které jste viděli na videu).
- Pětiúhelníky (a v menší míře i šestiúhelníky) jsou samoopakující se struktury [s84]. Všimněte si, že úhel v pravidelném pětiúhelníku je 108°, což je velmi blízké vazebnému úhlu mezi trojicí molekul vody. Máme‑li pětiúhelník, vyskytují se v jeho okolí s větší pravděpodobností další pětiúhelníky (viz obr.).
Homeopatie? Příliš krátká paměť
Struktury složené z mnohoúhelníků se někdy (poněkud nevhodně) nazývají „klastry“. Jsou‑li takovými strukturami obaleny rozpuštěné látky, pak „ledovce“. Nelze to však interpretovat tak, že ve vodě volně plují tyto klastry nebo ledovce jako medúzy v moři. Jedná se o velmi dynamický jev – klastry vznikají a zanikají. Pokud si voda „pamatuje“, že jí nějaký rozpuštěnec vnutil určitou strukturu, jedná se o velmi krátkou paměť, jen několik biliontin sekundy. Dlouhodobá paměť vody předpokládaná homeopaty není možná, protože síly mezi molekulami vody nejsou dost silné.
Vysvětlená hustota vody a ledu
Již víme, že okolí molekuly vody je čtyřstěnovité. Ale to také znamená, že v okolí takové molekuly je hodně prázdného místa, protože zkrátka molekuly navzájem vázané úhlem zhruba 110° se neumí úsporně poskládat. Nemáte‑li prostorovou představivost, můžete vzít zavděk dvourozměrným obrázkem vpravo. V ledu jsou všechny molekuly přesně čtyřstěnovité a prázdného místa je mnoho, proto je led lehčí. U vody je čtyřstěnovitost pouze přibližná, a tak se občas nějaká molekula (s menším počtem vodíkových vazeb) do volného místa nacpe. Za nižších teplot je síť čtyřstěnovitější, a proto hustota vody klesne. Zároveň ale tepelný pohyb, jako u každé slušně vychované kapaliny, způsobuje při ohřívání zvětšení objemu (snížení hustoty) – tento jev převládne nad 4 °C.
Obdobné výsledky dostaneme z úvah o pětiúhelnících. V okolí pětiúhelníků (které jsou častější za nižších teplot) je více prázdného prostoru.
Vysvětlená viskozita
Stlačíme‑li vodu, natlačíme molekuly do prázdných prostor okolo čtyřstěnovitých molekul. Tím se síť zbortí, přeruší se nebo se oslabí některé vodíkové vazby, které brání vrstvám vody v pohybu. Důsledkem je, že viskozita klesne. Voda se přiblíží „normální“ kapalině.
Vysvětlené tepelné vlastnosti
Víme, že vodíkové vazby mají hodně energie. Proto je bod varu vody vysoký. Ohřejeme‑li vodu, vodíkové vazby rozbijeme – je jich méně a jsou slabší. K tomu je ovšem potřeba energie, a proto je tepelná kapacita vody anomálně vysoká. Naopak v páře vodíkové vazby téměř nejsou (a není co rozbíjet), v ledu sice jsou, ale nerozbíjejí se, a proto je tepelná kapacita ledu i páry nižší. Tuto anomálii sdílí voda s ostatními asociujícími kapalinami.
Podchlazená voda
V podchlazené vodě se anomálie dále zvýrazňují, protože pomalejší tepelný pohyb tolik nerozbíjí vodíkové vazby. Ve studené vodě je hodně pětiúhelníků a kolem nich hodně prázdného prostoru. Pětiúhelníky nejsou slučitelné se strukturou ledu, který obsahuje šestiúhelníky, a proto je možno vodu poměrně hodně podchladit, aniž zmrzne na led, který obsahuje šestiúhelníky (viz kroupa vpravo).
Druhý citát místo závěru
„Stalo se populárním zdůrazňovat „anomální“ aspekt vlastností vody. Tato móda směřuje k zakrytí faktu, že tyto „anomálie“ jsou většinou pouze malými odchylkami od normálních vlastností asociujících kapalin.“
C. M. Davis & J. Jarzynski ve sborníku Water and Aqueous Solutions (red. R. A. Horne), Wiley, NY (1972)
[s84] RJ Speedy: Self-Replicating Structures in water, J. Chem. Phys. 88, 3364 (1984).
[sa76] RJ Speedy, CA Angell: Isothermal compressibility of supercooled water and evidence for thermodynamic singularity at −45 °C, J. Chem. Phys. 65, 851 (1976).
[w] Water structure and Science, http://www1.lsbu.ac.uk/water/anmlies.html.
[ice] Ice Structure, https://www.uwgb.edu/dutchs/Petrology/Ice%20Structure.HTM
[kn89] J Kolafa, I Nezbeda: Struktura a anomálie vody z hlediska statistické termodynamiky, Čs. čas. fyz. A39, 345–368 (1989) a literatura tam uvedená.
[kn00] J Kolafa, I Nezbeda: Effect of short- and long-range forces on the structure of water. II. Orientational ordering and the dielectric constant, Mol. Phys. 98, 1505 (2000).
[d14] JC Palmer, F Martelli, Y Liu, R Car, AZ Panagiotopoulos, PG Debenedetti: Metastable liquid–liquid transition in a molecular model of water, Nature 510, 385 (2014), doi: 10.1038/nature13405
[h13] V Holten, DT Limmer, V Molinero, MA Anisimov: Nature of the anomalies in the supercooled liquid state of the mW model of water, J. Chem. Phys. 138, 174501 (2013)